1 UNIVERSIDAD NACIONAL DE ASUNCIN FACULTAD DE CIENCIAS
































- Slides: 53

1 UNIVERSIDAD NACIONAL DE ASUNCIÓN FACULTAD DE CIENCIAS QUÍMICAS CÁTEDRA DE INMUNOLOGÍA CLÍNICA UNIDAD TEMÁTICA: INMUNIDAD DE LAS MUCOSAS

OBJETIVOS Describir los componentes del sistema inmune común de las mucosas Detallar los sitios inductores y los sitios efectores Relacionar las funciones de la Ig. A de las secreciones, como uno de los principales componentes efectores

CONTENIDOS 2. 1 Introducción 2. 2 Sitios inductores y efectores en el GALT 1. Sitios inductivos: placas de Peyer 2. 3 Ingreso del antígeno en los sitios inductivos y efectores del GALT 2. 4 Activación de Linfocitos T vírgenes en el GALT y asentamiento de células T efectoras y Tme 2. 5 Activación de Linfocitos B vírgenes en el GALT y asentamiento de Plasmoblastos 2. 6 Propiedades de los anticuerpos Ig. A 2. 7 Linfocitos T presentes en la mucosa intestinal 2. 8 Funcionalidad de las células dendríticas y perfil de diferenciación de las células T en el GALT

El sistema inmunitario de las mucosas, en particular si el asociado con el tubo digestivo es el más complejo y numeroso. No sólo se enfrenta a una gran diversidad de antígenos y microorganismos sino que debe diferenciarlos de antígenos inocuos de la dieta y flora comensal.

Inmunidad en las mucosas Objetivo de la respuesta inmunitaria en las mucosas Inducción de tolerancia local frente a antígenos inocuos. Generación de una vigorosa respuesta frente a organismos patógenos

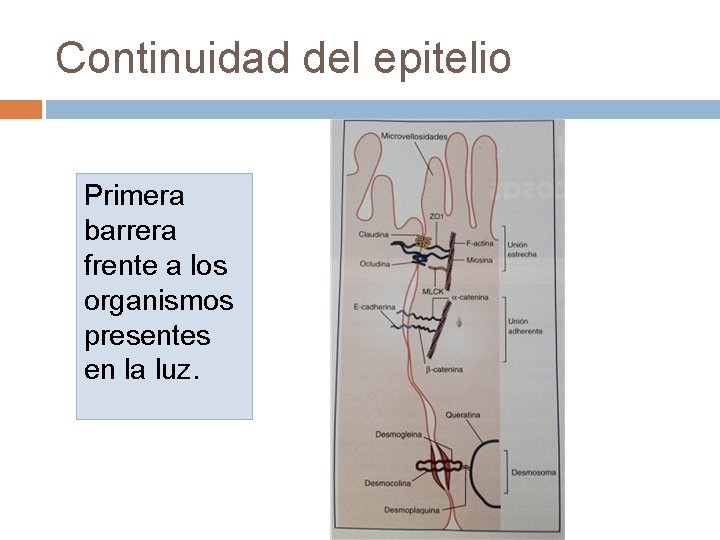
Continuidad del epitelio Primera barrera frente a los organismos presentes en la luz.

Continuidad del epitelio La permisividad de las uniones al pasaje de componentes microbianos presentes en la luz es modulada por citocinas. INF gamma y TNF alfa ------- relajan las uniones TGF beta y IL-10 -------disminuyen la permeabilidad

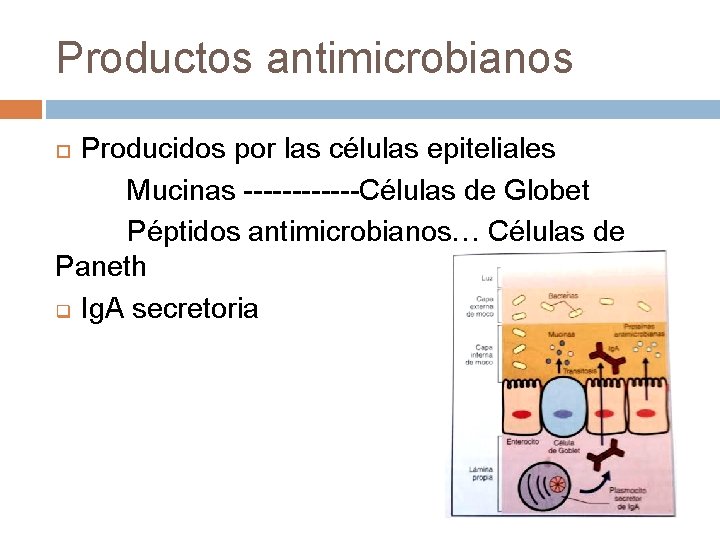
Productos antimicrobianos Producidos por las células epiteliales Mucinas ------Células de Globet Péptidos antimicrobianos… Células de Paneth q Ig. A secretoria

Otra defensa importante La flora comensal v v v Compite por nichos y nutrientes con M. O. Patógenos Activan mecanismos inmunitarios que controlan su desarrollo y actúan frente a patógenos. Participa en el desarrollo del sistema inmunitario de las mucosas

Además Los enterocitos expresan receptores de reconocimiento de patrones (RRP). Sobre todo TLR. La estimulación de TLR por PAMP conducirá a: Mayor producción de mucinas y péptidos antimicrobianos Producción de quimiocinas y citocinas inflamatoria La respuesta inflamatoria desencadenada frente a la infección tendrá como protagonistas a los neutrófilos y macrófagos primero, y a las células NK y linfocitos T gamma-delta.

Sistema inmunitario adaptativo Los linfocitos y tejido linfoide presente en la mucosa recibe el nombre de MALT En el individuo contiene el 80% del total de linfocitos presentes en el organismo.

El MALT en diferentes localizaciones GALT : asociado al tubo digestivo BALT: asociado al árbol bronquial NALT: asociado al tracto nasofaríngeo Tejido linfoide asociado a la glándula mamaria Tejido linfoide asociado a los órganos genitourinarios Tejido linfoide asociado al oído interno.

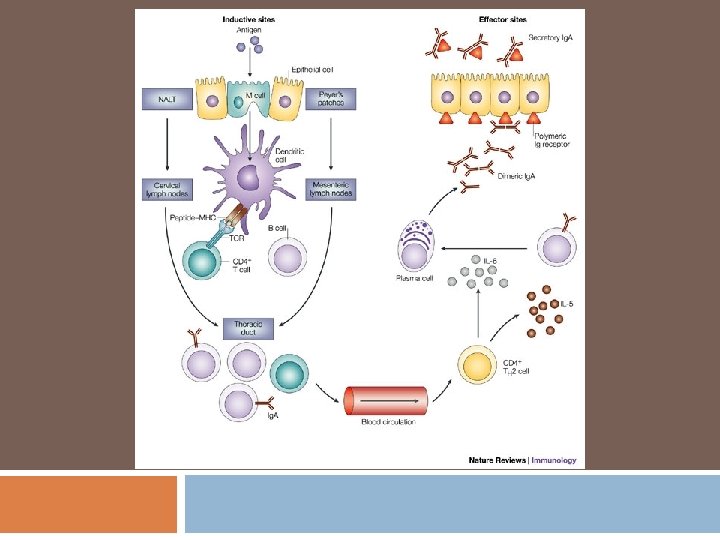
Sitios inductivos y efectores en el GALT Sitio inductor: aquel en el cual los linfocitos T y B virgenes se activan, se expanden y se transforman en células efectoras o de memoria. Placas de Peyer Ganglios Mesentéricos Folículos linfoides aislados que están en la lámina propia.

Sitios efectores Comprenden el Epitelio y la lámina propia, donde se ubican en forma difusa las células T CD 4+ y CD 8+ efectoras y las celulas T de memoria efectoras.

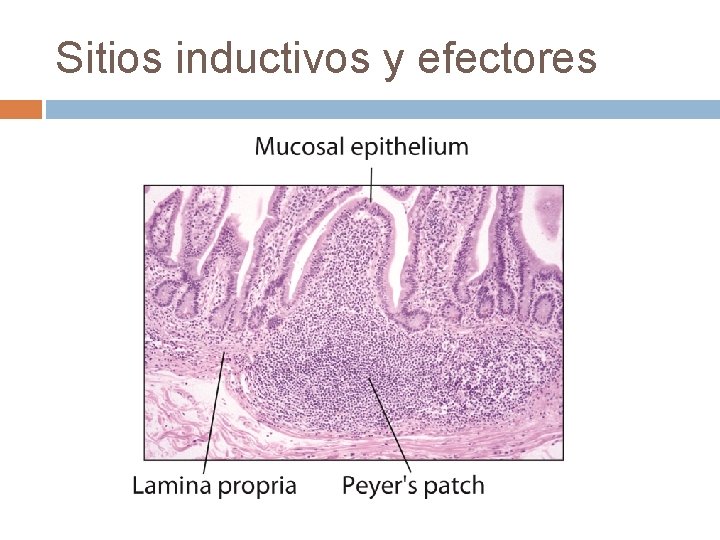
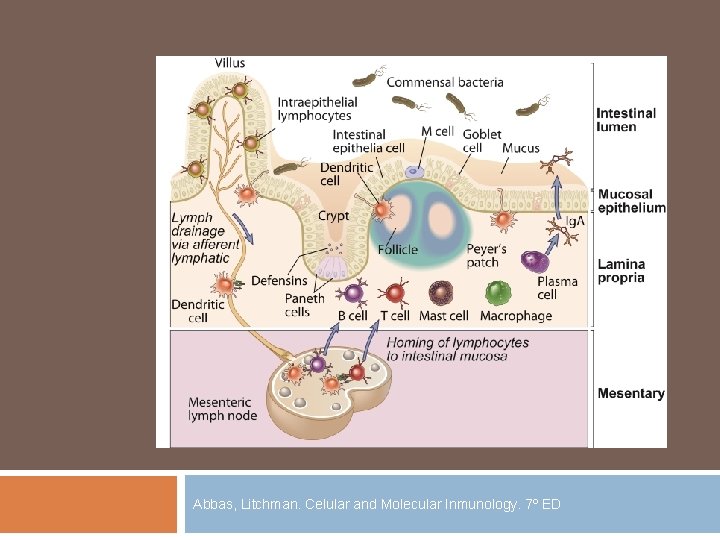
Sitios inductivos y efectores

Abbas, Litchman. Celular and Molecular Inmunology. 7º ED

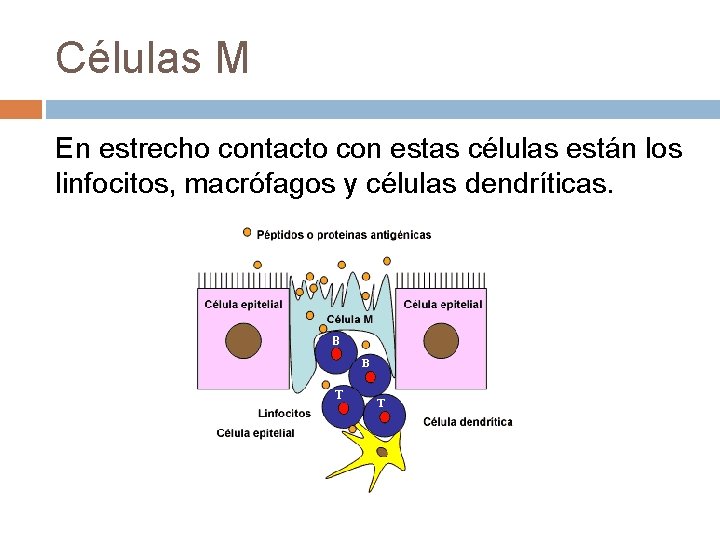
Los folículos linfoides se ubican en el intestino, en la lámina propia y están en contacto estrecho con las células epiteliales. Las células epiteliales vecinas a los folículos conforman el epitelio asociado a folículos FAE, entre las cuáles se encuentran las células M (microfold). Las células M traslocan Ags desde la luz hacia la lámina propia.

Células M En estrecho contacto con estas células están los linfocitos, macrófagos y células dendríticas.

Propiedades de las células M Alta capacidad endocítica Escasa actividad degradativa en su compartimiento endosómico Glucocádiz escaso No expresan receptores para Ig. A, por lo cual reducen la concentración de Ig. A secretoria en su región apical favoreciendo la endocitosis de microorganismos y productos microbianos

Captura de Ag por las células M Internalización de macromoléculas y virus reconocidos por receptores mediante la formación de vesículas endocíticas. Endocitosis en fase fluida, para moléculas no reconocidas por receptores. Fagocitosis Abbas, Litchman. Celular and Molecular Inmunology. 7º ED

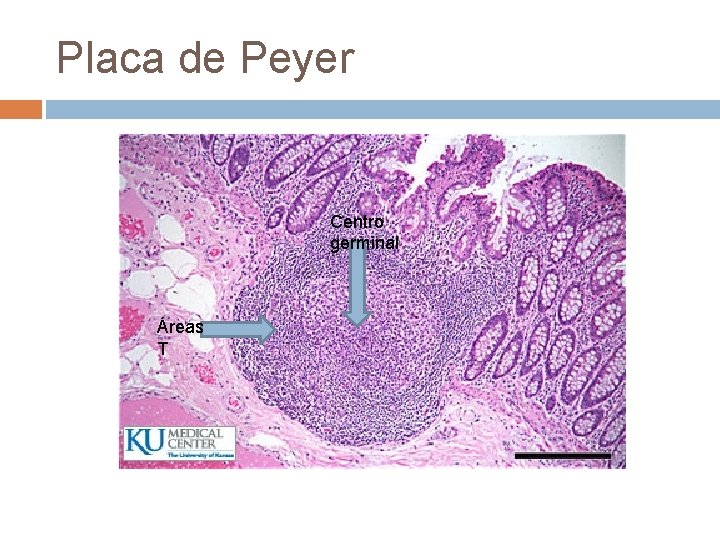
Placas de Peyer Distribución de linfocitos semejantes al ganglio linfático v v Zona germinal (células foliculares dendríticas y células B, también células Tfh) Áreas T : donde se activarán las células T vírgenes a través del reconocimiento de péptidos antigénicos presentados por moléculas de Clase I y Clase II del CMH

Placa de Peyer Centro germinal Áreas T

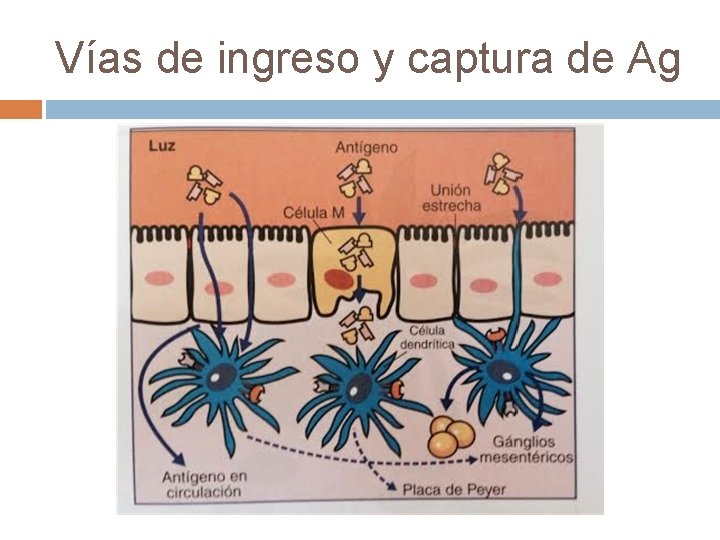
Ingreso del antígeno Puede realizarse por 3 caminos v A través de los enterocitos (transporte transcelular, paracelular). v A través de las células M. v A través de ser capturados en la propia luz por las células dendríticas.

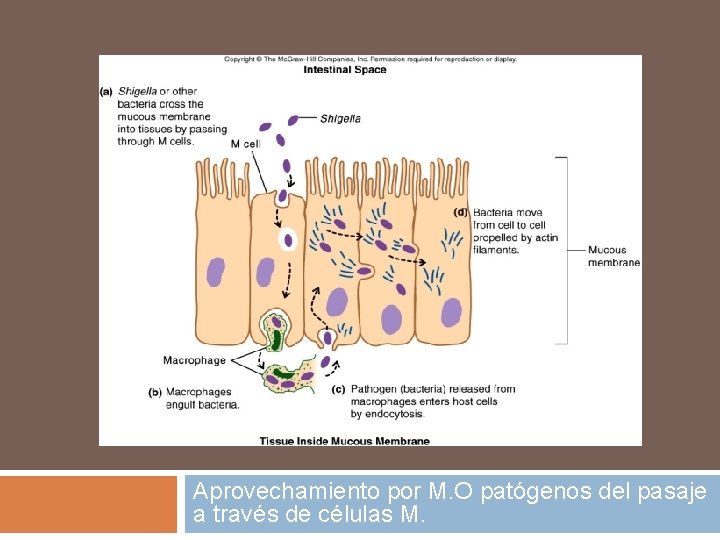
Aprovechamiento por M. O patógenos del pasaje a través de células M.

Destino de los antígenos Ø Ø Ø Ag atrapados por las células dendríticas Son procesados y dirigidos a las placas de Peyer o ganglios mesentéricos a fin de activar a los linfocitos T vírgenes. Las células dendríticas cercanas a las células M van a migrar a las placas de Peyer Las lejanas a los ganglios mesentéricos por vía aferente linfática.

Ag translocados por los enterocitos y células M Pueden acceder a las placas de Peyer a los folículos linfoides aislados o transportarse por vía aferente linfática hasta los ganglios mesentéricos regionales. Estos antígenos no capturados por las células dendríticas y no procesados serán reconocidos por los linfocitos B en los folículos primarios. O bien los Ag serán capturados por las células dendríticas de la lámina propia, procesados y transportados por ellas.

Vías de ingreso y captura de Ag

Activación de linfocitos T vírgenes Al ser activados por las células dendríticas en las Placas de Peyer o en los ganglios mesentéricos, las células T pueden diferenciarse en distintos perfiles efectores. Una fracción de las células T activadas se diferenciará posteriormente en células T de memoria centrales y efectoras.

Particularidades en el GALT La activación de linfocitos T vírgenes presenta un patrón de migración o de asentamiento (Homing). Las células T efectoras y de memorias diferenciadas a partir de linfocitos T vírgenes activadas en la placa de Peyer o ganglios mesentéricos expresarán la integrina α 4ß 7 y el receptor de quimiocinas CCR 9, que mediarán su reclutamiento en la lámina propia intestinal.

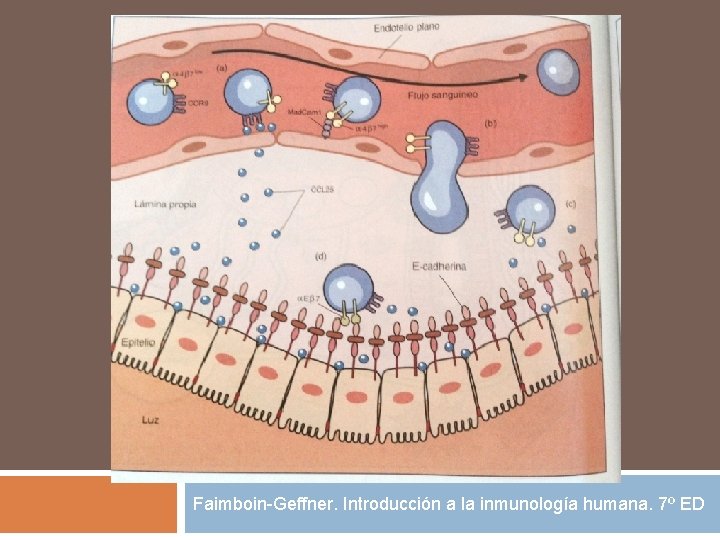
Homing El sitio en el cual la célula dendrítica capturó el Ag que será presentado a la célula T virgen determinará, el patrón migratorio a las células T efectoras y T de memoria. Esto es particularmente cierto para las células T tanto CD 4 como CD 8 activadas en las Placas de Peyer y en los ganglios mesentéricos que expresarán el código de entrada que permitirá su acceso a la lámina propia a traves del endotelio de las vénulas que expresan los ligandos de las moléculas α 4ß 7 y CCR 9.

Homing Una importante fracción de linfocitos T CD 8 activados expresará además la integrina αEß 7 que permitirá su unión firme a los enterocitos, que expresan su ligando ( E-Cadherina). A estos linfocitos se les denomina Linfocitos intraepiteliales (LIE).

Que determina el asentamiento de los linfocitos T efectores en la lámina propia? Son las células dendríticas determinan el patrón de migración de las células T. Las células dendríticas de la mucosa intestinal, producen ácido retinoico. El mismo estimula en la célula T activada un patrón de asentamiento que le direcciona a la mucosa intestinal al inducir la expresión de α 4ß 7 y CCR 9.

Faimboin-Geffner. Introducción a la inmunología humana. 7º ED

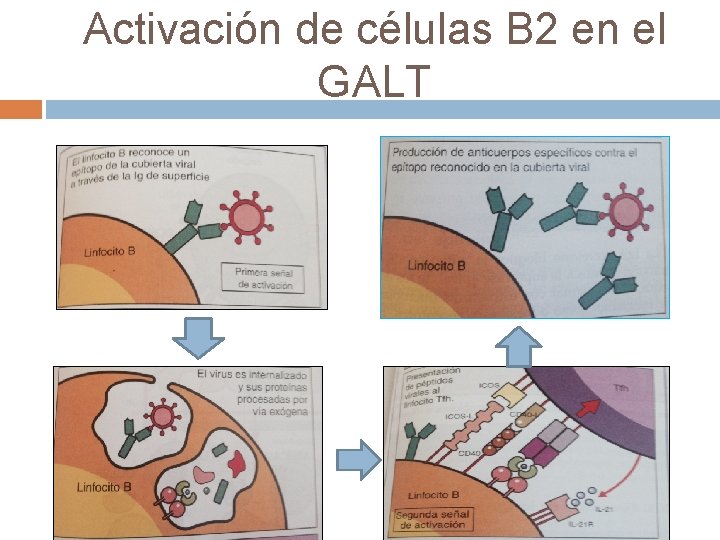
Activación de células B 2 en el GALT

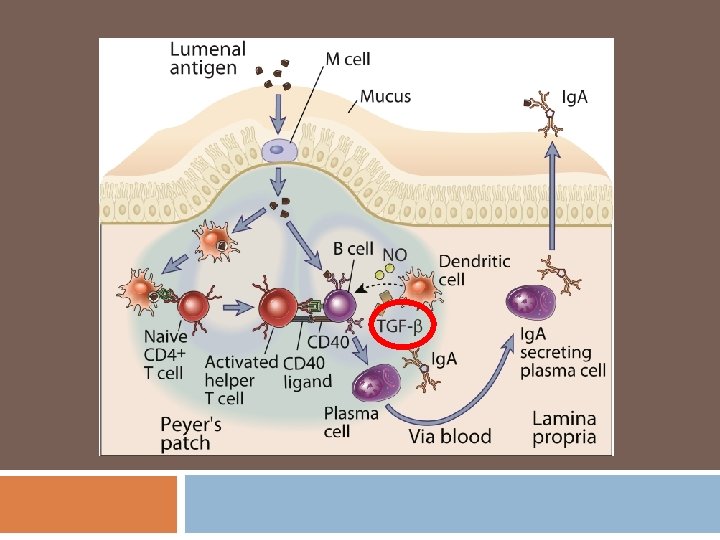
Particularidades de esta activación en GALT Promueve el cambio de clase a la producción de Ac. tipo Ig. A. (TGF-ß) Ø Favorece el asentamiento de plasmoblastos Ig. A+ en la lámina propia intestinal, mediante el código de entrada α 4ß 7 y CCR 9. Los plasmoblastos producidos en las placas de Peyer y ganglios regionales se vuelcan a la cirgulación general y estas moléculas expresadas las reclutan a la lámina propia. Ø


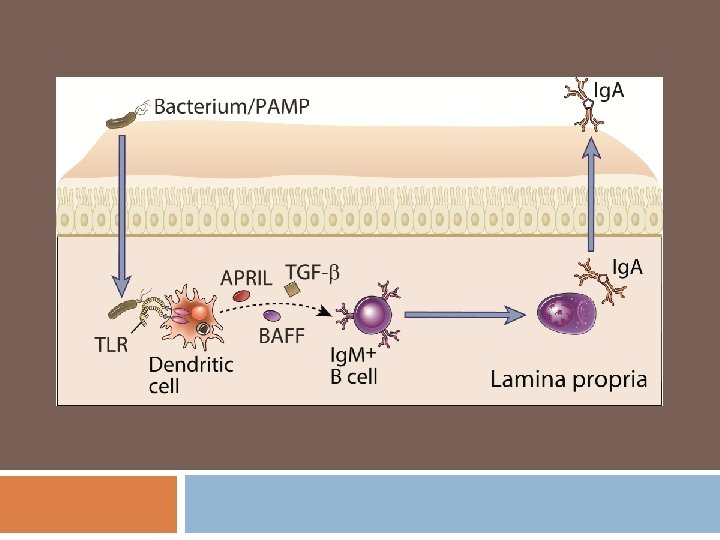
Activación de linfocitos B 1 (T ind) Activación por parte de las células dendríticas a los linfocitos B Ig. M+Ig. D+. Las células dendríticas activadas por los ligandos TLR (receptores toll) secretan factores que inducen el cambio de clase a Ig. A, como el BAFF, APRIL y TGF-ß, además de IL 6 y ácido retinoico. Esta activación da lugar a anticuerpos Ig. A con afinidad relativamente baja frente a las bacterias intestinales comensales.


LA Ig. A SECRETORIA PRODUCIDA POR LAS CELULAS B 1 CUMPLEN UNA FUNCION RELEVANTE EN EL CONTROL DE LA FLORA COMENSAL AL IMPEDIR QUE LAS BACTERIAS COMENSALES TRANSGREDAN LA BARRERA EPITELIAL.

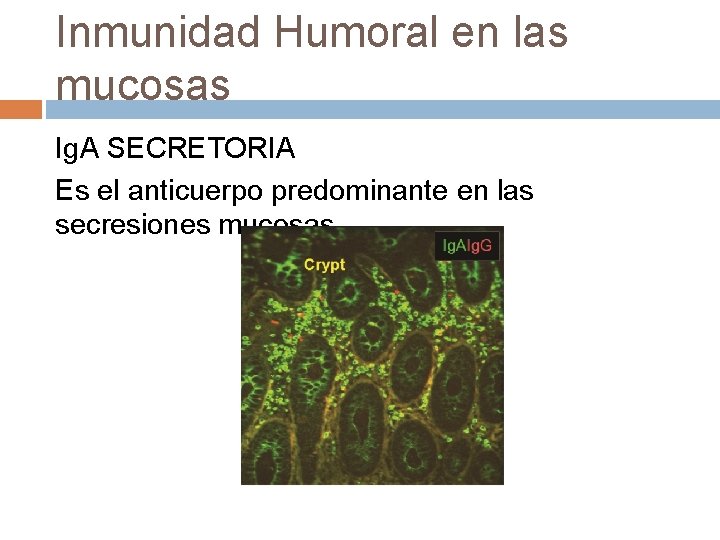
Inmunidad Humoral en las mucosas Ig. A SECRETORIA Es el anticuerpo predominante en las secresiones mucosas

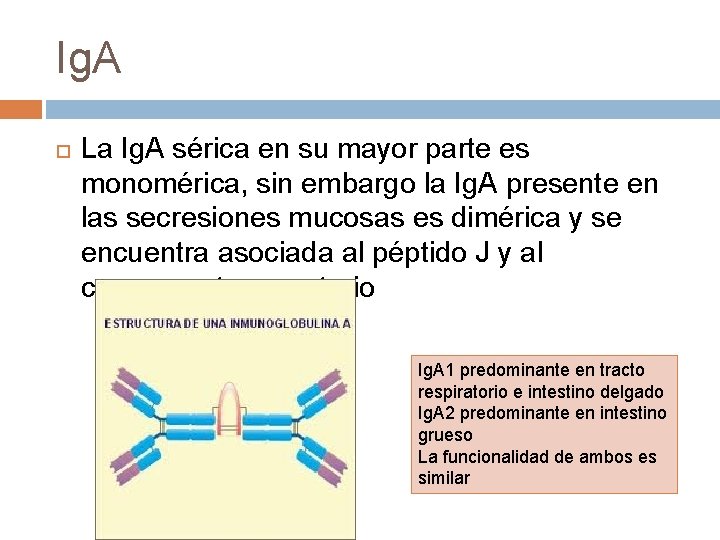
Ig. A La Ig. A sérica en su mayor parte es monomérica, sin embargo la Ig. A presente en las secresiones mucosas es dimérica y se encuentra asociada al péptido J y al componente secretorio Ig. A 1 predominante en tracto respiratorio e intestino delgado Ig. A 2 predominante en intestino grueso La funcionalidad de ambos es similar

Funciones de la Ig. A secretoria Actúa como un anticuerpo neutralizante. El componente secretorio le protege de la alta actividad proteolítica de la luz intestinal. Bloquea la adhesión de M. O a la superficie apical de los enterocitos al interactuar con las estructuras microbianas que funcionan como adhesinas o receptores y neutraliza toxinas microbianas. Exclusión inmune. Inhibe también la absorción de Ag y alergenos La actividad antimicrobiana desencadenada por Ig. A no se acompaña de rta. Inflamatoria puesto que no activa el complemento.

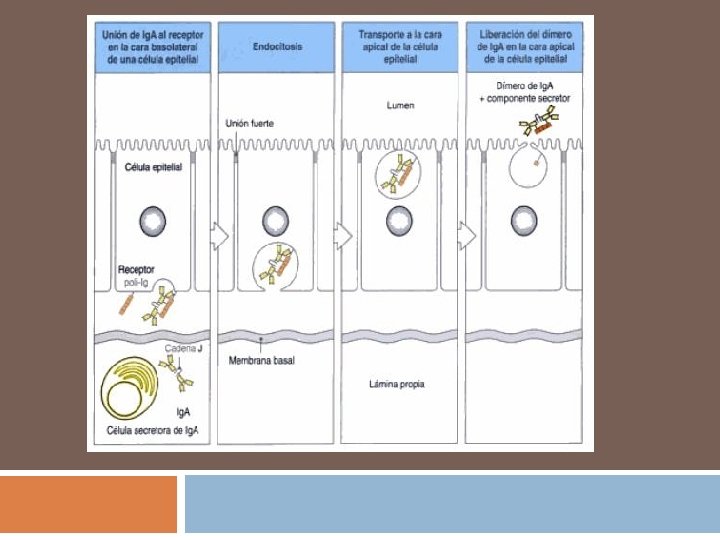
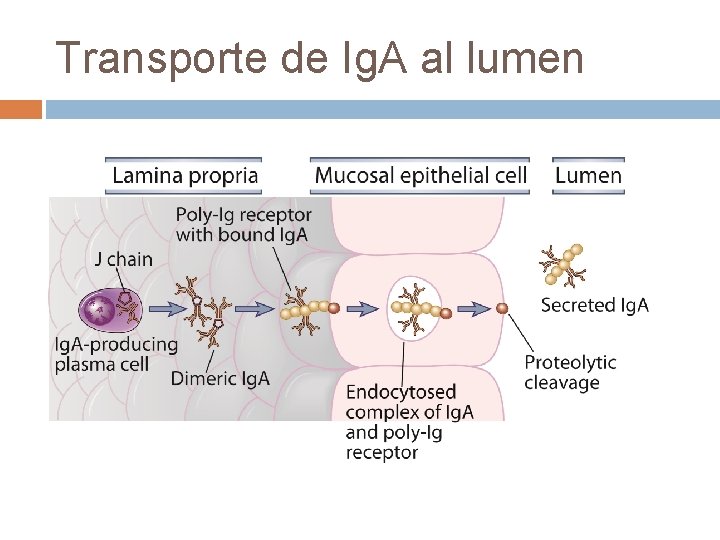
Transporte de Ig. A al lumen El componente secretorio está formado por 5 dominios de tipo Ig. El N-terminal, establece una unión covalente con Ig. A a traves de un SS. La Ig. A se une al p. Ig. R y el complejo es internalizado, transportado en una vacuola y liberado en la región apical Finalmente la escición del p. Ig. R libera a Ig. A que retiene la porción extracelular del componente secretorio. La porción transmembrana y citoplásmica del p. Ig. R es endocitada y degradada.


Transporte de Ig. A al lumen

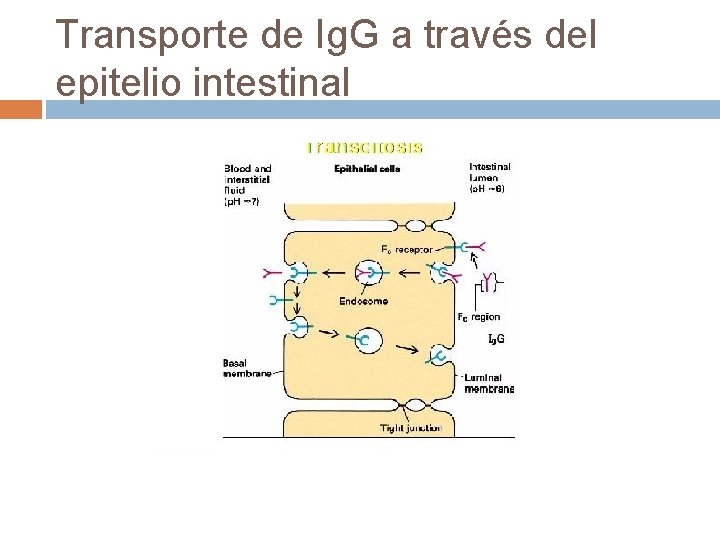
Transporte de Ig. G a través del epitelio intestinal


Inmunidad mediada por linfocitos T Los linfocitos T presentes en el intestino se distribuyen en tres localizaciones Ø Sitios inductivos: se activan linfocitos T virgenes Ø Lámina propia: se encuentran linfocitos T efectores y de memoria Ø Epitelio: Linfocitos T intraepiteliales. LIE

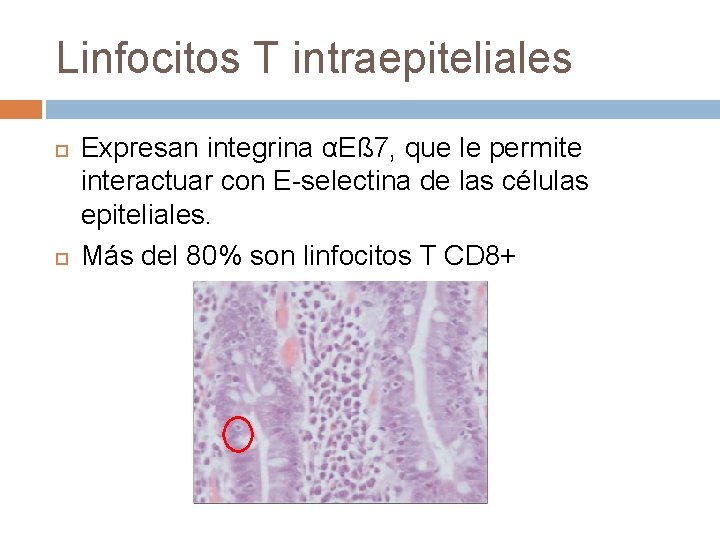
Linfocitos T intraepiteliales Expresan integrina αEß 7, que le permite interactuar con E-selectina de las células epiteliales. Más del 80% son linfocitos T CD 8+

Función de los LIE Promueven una primera línea de defensa en el intestino, al destruir células estresadas o dañadas, con lo que contribuyen a preservar la integridad de la barrera epitelial. Producen citocinas antiinflamatorias que contribuyen al desarrollo de mecanismos de tolerancia frente a la flora comensal y frente a Antígenos dietarios.

Linfocitos T Los linfocitos T presentes en la lámina propia son casi todos CD 4+ y son efectores y de memoria efectores Los linfocitos de las placas de Peyer y sitios inductores son CD 4 cooperadores y linfocitos T reguladores. En ausencia de infección las células T del GALT tienden a diferenciarse en un perfil Th 2 o regulador, mientras que en presencia de procesos infecciosos se favorece la producción de células Th 1 o Th 17. Los linfocitos T reguladores evitan las reacciones

Porque la flora comensal no induce respuesta inflamatoria Debido a la baja expresión de RRP tipo TLR, en ausencia de fenómenos inflamatorios que comprometan la mucosa. Se expresan en su mayor parte en la región basolateral, puesto solo aquellos PAMP que logren acceder a la superficie basolateral del enterocito podrán activar una respuesta inflamatoria.

BIBLIOGRAFIA Fainboim Geffner. Introducción a la Inmunología Humana 6 edición. Editorial Panamericana. 2011. Abbas AK, Lichtman AH. Basic Immunology. Functions and disorders of the immune system, 3 rd edition. Saunders (Elsevier); 2009 Kenneth Murphy, Paul Travers, Mark Walport. Inmunobiología de Janeway. 7 edición. Editorial Mc Graw Hill. 2008