1 Subdomnio Unidade Equilbrio qumico 1 1 Aspetos

1 Subdomínio Unidade Equilíbrio químico

1. 1 Aspetos quantitativos das reações químicas 1. 1. 1 Equações químicas

O carbono e o oxigénio interagem para formar dióxido de carbono.

O ferro interage com o oxigénio, dando origem a óxido de ferro.

A interação entre o iodeto de potássio e o nitrato de chumbo origina nitrato de potássio (amarelo) e iodeto de chumbo.

Na Natureza, ocorrem inúmeras transformações que resultam na formação de novas substâncias. Essas transformações são denominadas reações químicas.

Numa reação química. . . parte-se de uma ou mais substâncias — reagentes . . . originam-se novas substâncias — produtos de reação

Para representar uma reação química, escreve-se a sua equação química. Uma equação química obedece ao esquema: Reagentes Produtos de reação

Exemplo A reação do carbono com o oxigénio origina dióxido de carbono. Reagentes Produtos de reação Carbono Dióxido de carbono Oxigénio

Exemplo A reação do carbono com o oxigénio origina dióxido de carbono. Reagentes C(s) + O 2(g) Produtos de reação CO 2(g)

O químico Antoine Lavoisier concluiu que, numa Antoine Lavoisier (1734 -1794) reação química, . . . o número total de átomos de cada elemento presente no sistema reacional se mantém constante. . a massa total do sistema se conserva durante a reação — Lei de Lavoisier ou Lei da Conservação da Massa.
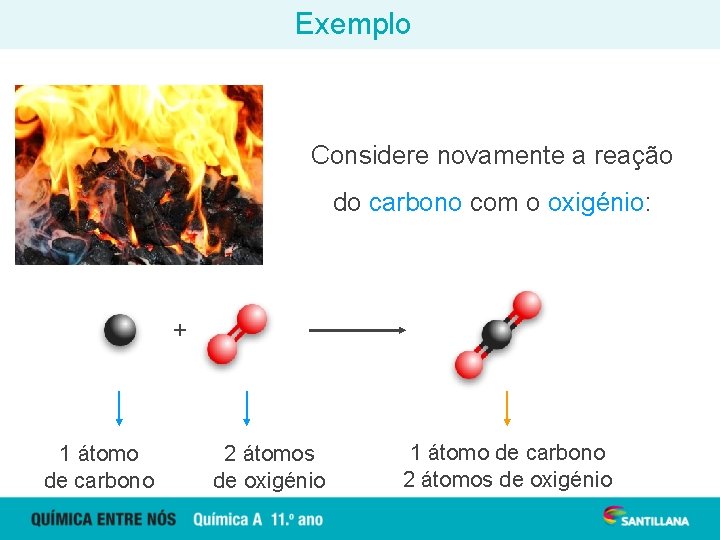
Exemplo Considere novamente a reação do carbono com o oxigénio: C (s) + O 2 (g) 1 átomo de carbono 2 átomos de oxigénio CO 2 (g) 1 átomo de carbono 2 átomos de oxigénio
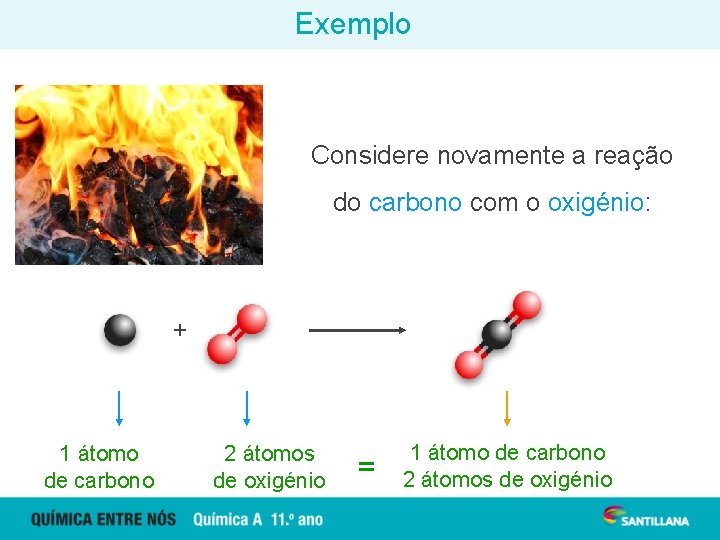
Exemplo Considere novamente a reação do carbono com o oxigénio: C (s) + O 2 (g) 1 átomo de carbono 2 átomos de oxigénio CO 2 (g) = 1 átomo de carbono 2 átomos de oxigénio

Exemplo Considere novamente a reação do carbono com o oxigénio: C (s) + O 2 (g) CO 2 (g) O número total de átomos de cada elemento presente no sistema reacional mantém-se constante.

Exemplo Considere novamente a reação do carbono com o oxigénio: C (s) + O 2 (g) CO 2 (g) A massa total do sistema conserva-se durante a reação.

1. 1 Aspetos quantitativos das reações químicas 1. 1. 2 Balanço de equações químicas

As equações químicas fornecem informação quantitativa e qualitativa sobre as reações químicas. A escrita de equações químicas deve obedecer à Lei de Lavoisier. Deve garantir-se que o número total de átomos de cada elemento no sistema reacional permanece constante.

Exemplo O amoníaco é utilizado como gás refrigerante em frigoríficos e outros sistemas de arrefecimento. O amoníaco é produzido pela reação Produção industrial de amoníaco entre o nitrogénio e o hidrogénio, de acordo com o esquema: Nitrogénio + Hidrogénio Amoníaco

Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . N 2(g) + H 2(g) NH 3(g) . . . verifica-se que o esquema não respeita a Lei de Lavoisier; por isso, está errado.
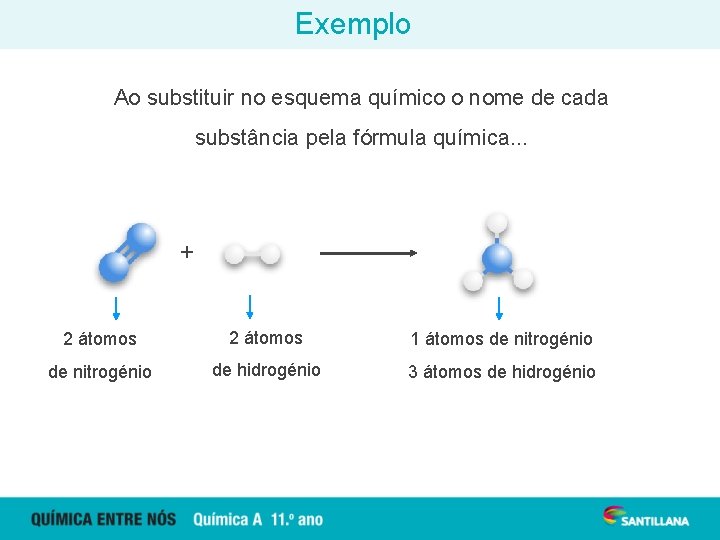
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . N 2(g) + H 2(g) NH 3(g) 2 átomos 1 átomos de nitrogénio de hidrogénio 3 átomos de hidrogénio

Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . N 2 (g) + H 2 (g) 2 átomos de nitrogénio de hidrogénio NH 3 (g) ≠ 1 átomos de nitrogénio 3 átomos de hidrogénio O número total de átomos de cada elemento é diferente nos reagentes e produtos, o que não é possível.
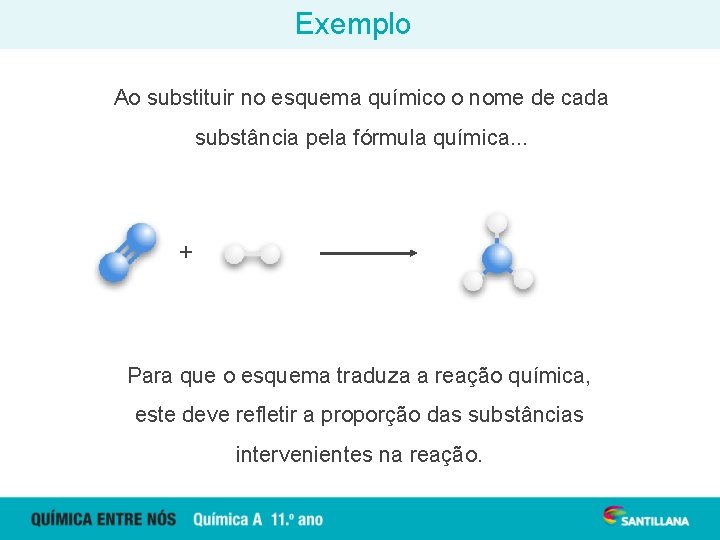
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + NH 3 (g) Para que o esquema traduza a reação química, este deve refletir a proporção das substâncias intervenientes na reação.
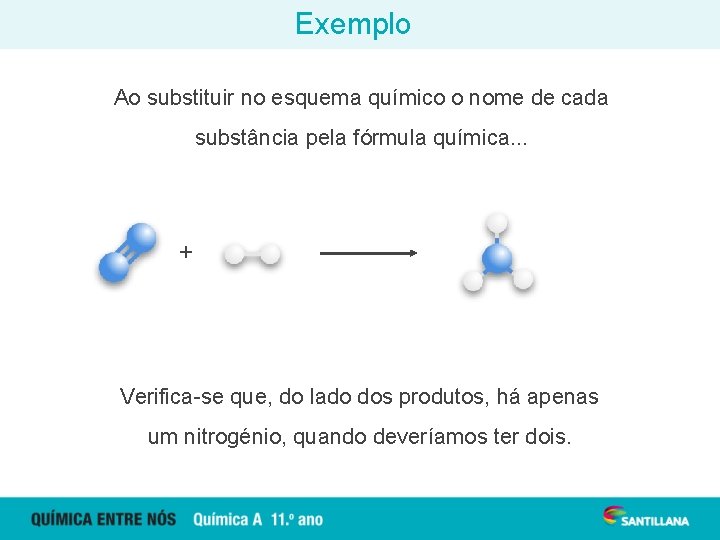
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + NH 3 (g) Verifica-se que, do lado dos produtos, há apenas um nitrogénio, quando deveríamos ter dois.
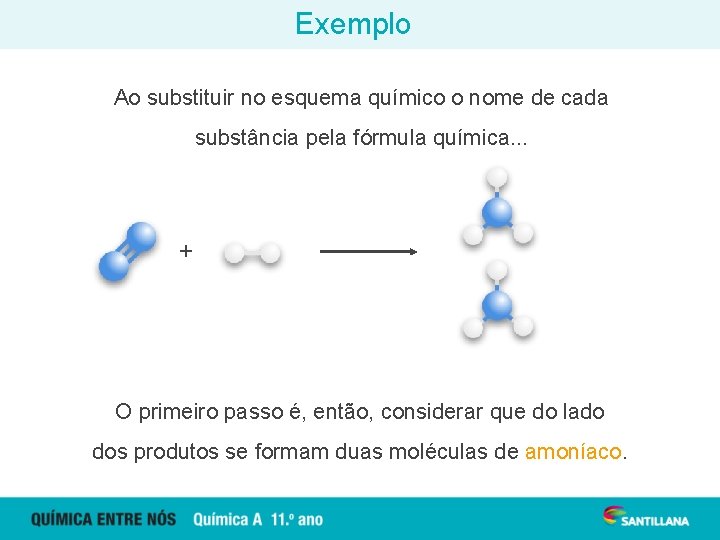
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + NH 3 (g) O primeiro passo é, então, considerar que do lado dos produtos se formam duas moléculas de amoníaco.
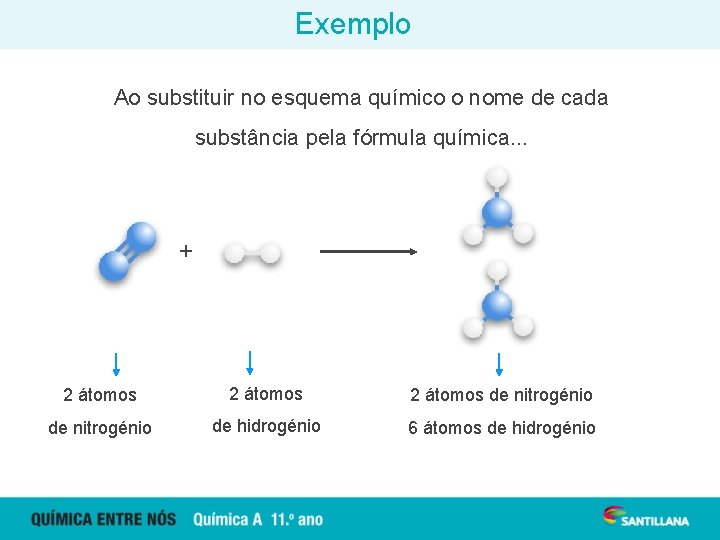
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + 2 átomos de nitrogénio de hidrogénio 6 átomos de hidrogénio
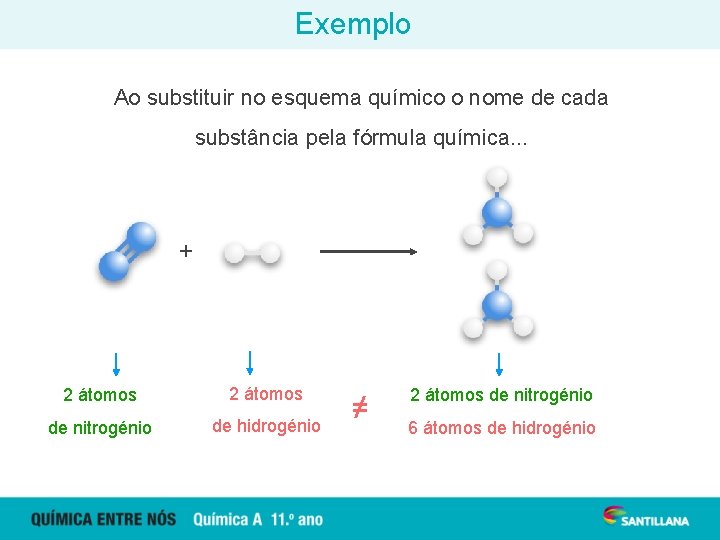
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + 2 átomos de nitrogénio de hidrogénio ≠ 2 átomos de nitrogénio 6 átomos de hidrogénio
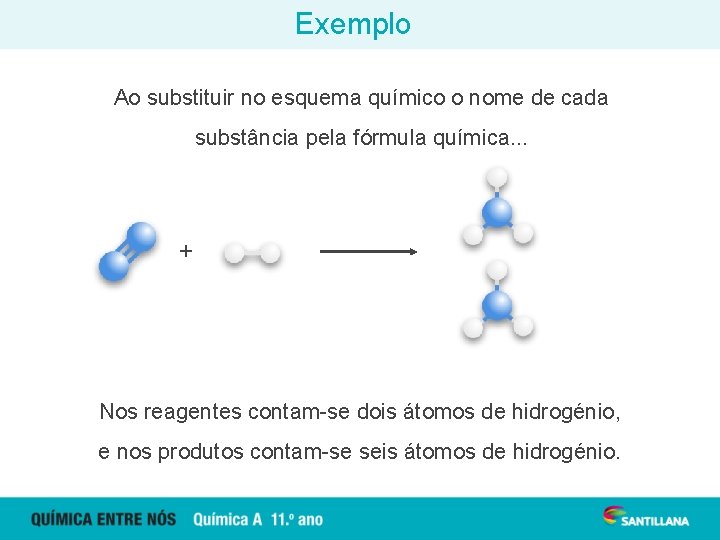
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + Nos reagentes contam-se dois átomos de hidrogénio, e nos produtos contam-se seis átomos de hidrogénio.
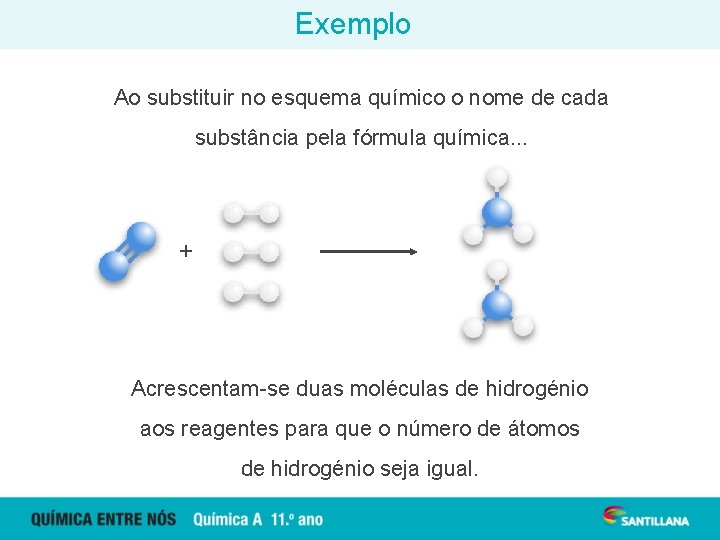
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + Acrescentam-se duas moléculas de hidrogénio aos reagentes para que o número de átomos de hidrogénio seja igual.
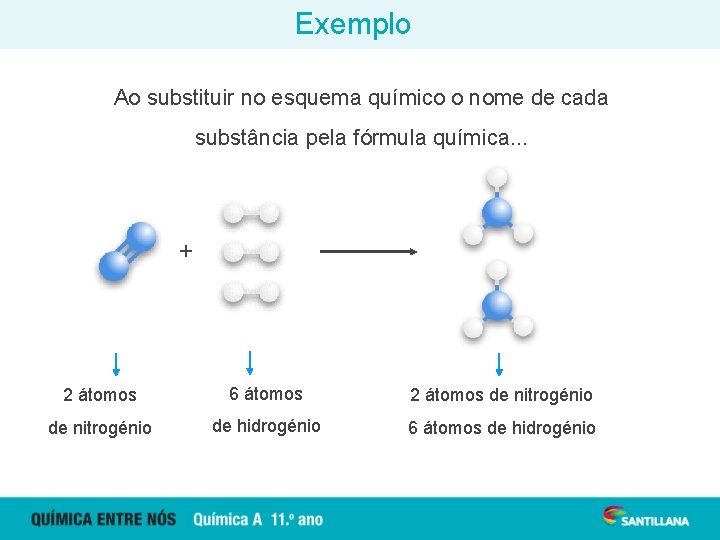
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + 2 átomos 6 átomos 2 átomos de nitrogénio de hidrogénio 6 átomos de hidrogénio
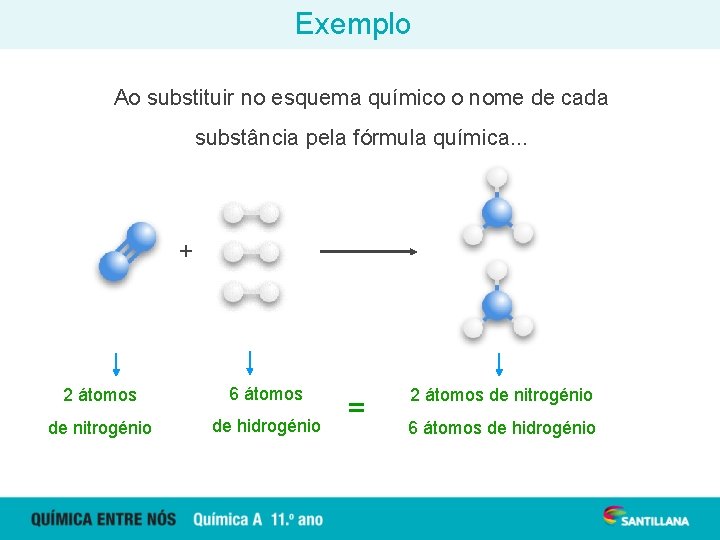
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + 2 átomos 6 átomos de nitrogénio de hidrogénio = 2 átomos de nitrogénio 6 átomos de hidrogénio
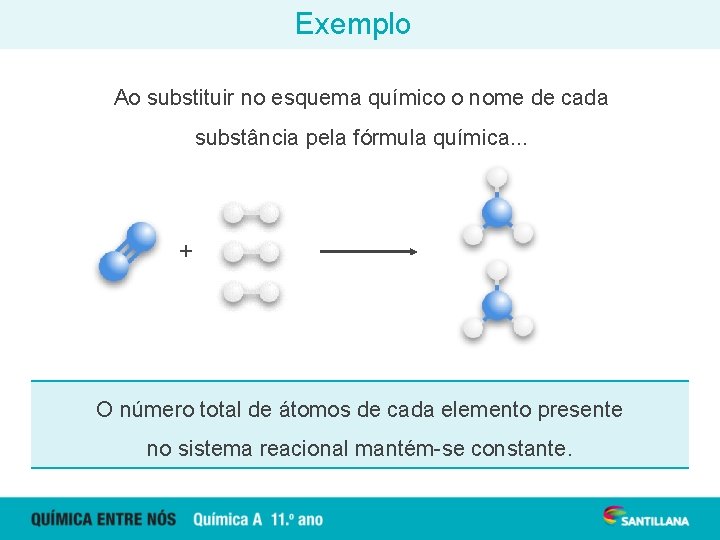
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + O número total de átomos de cada elemento presente no sistema reacional mantém-se constante.
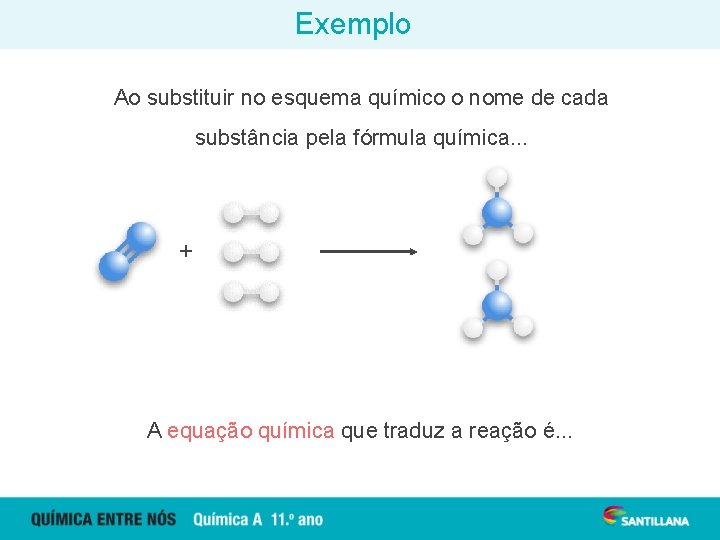
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + A equação química que traduz a reação é. . .
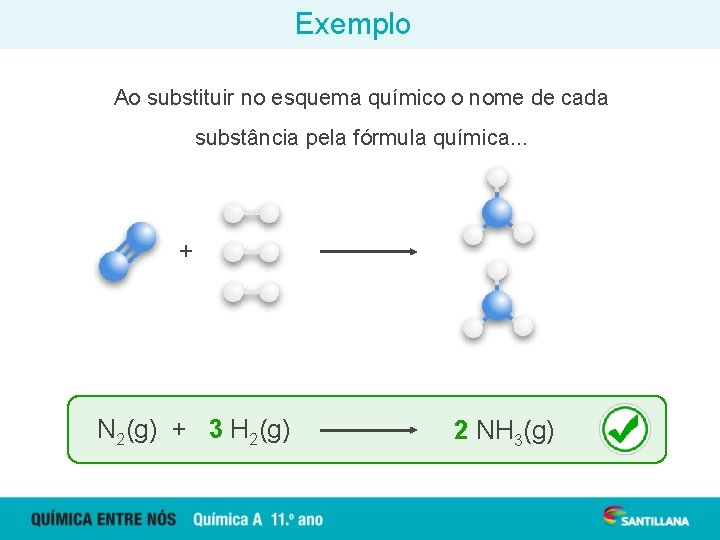
Exemplo Ao substituir no esquema químico o nome de cada substância pela fórmula química. . . + N 2(g) + 3 H 2(g) 2 NH 3(g)

Exemplo Os valores indicados antes da fórmula química de cada substância dão informação quantitativa sobre a reação. 1 N 2(g) + 3 H 2(g) 2 NH 3(g) Estes valores são denominados coeficientes estequiométricos.

Exemplo Os valores indicados antes da fórmula química de cada substância dão informação quantitativa sobre a reação. 1 N 2(g) + 3 H 2(g) 2 NH 3(g) Os coeficientes estequiométricos traduzem a proporção em que reagem e se formam todas as substâncias.

Exemplo Os valores indicados antes da fórmula química de cada substância dão informação quantitativa sobre a reação. 1 N 2(g) + 3 H 2(g) 2 NH 3(g) Os coeficientes estequiométricos desta equação são: 1: 3: 2.

Exemplo Os valores indicados antes da fórmula química de cada substância dão informação quantitativa sobre a reação. 1 N 2(g) + 3 H 2(g) 2 NH 3(g) 1 molécula de N 2 reage com 3 moléculas de H 2, originando 2 moléculas de NH 3.

1. 1 Aspetos quantitativos das reações químicas 1. 1. 3 Relações estequiométricas

Uma equação química expressa a quantidade química equivalente de reagentes e produtos. A estequiometria envolve o cálculo da quantidade das substâncias intervenientes na reação. O cálculo é feito com base na equação química e na quantidade de pelo menos uma substância.
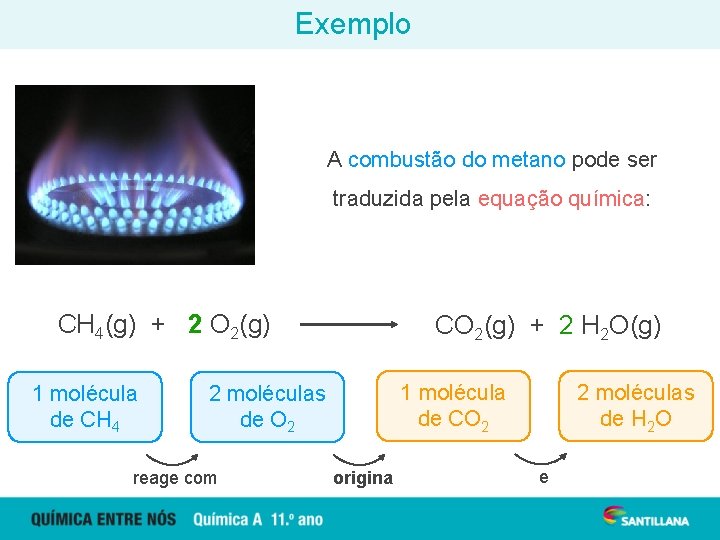
Exemplo A combustão do metano pode ser traduzida pela equação química: CH 4(g) + 2 O 2(g) 1 molécula de CH 4 CO 2(g) + 2 H 2 O(g) 1 molécula de CO 2 2 moléculas de O 2 reage com origina 2 moléculas de H 2 O e
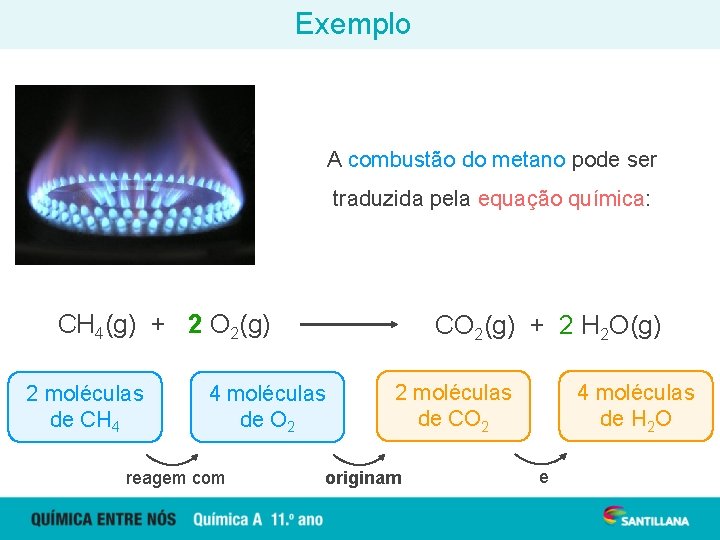
Exemplo A combustão do metano pode ser traduzida pela equação química: CH 4(g) + 2 O 2(g) 2 moléculas de CH 4 CO 2(g) + 2 H 2 O(g) 4 moléculas de O 2 reagem com 2 moléculas de CO 2 originam 4 moléculas de H 2 O e
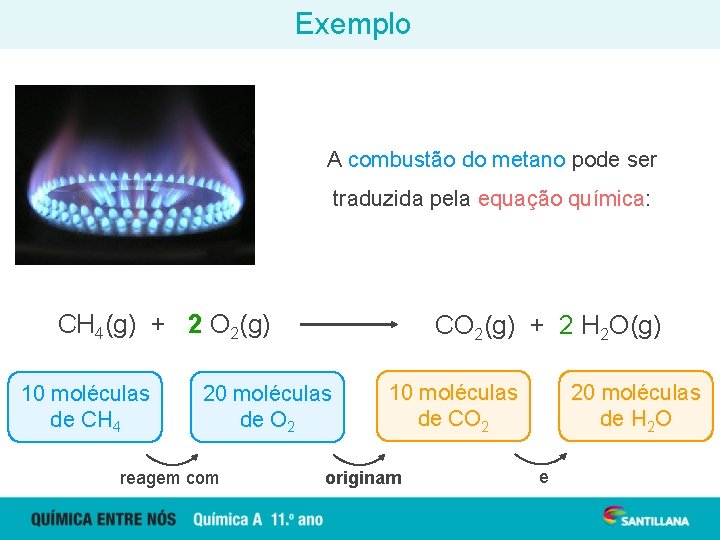
Exemplo A combustão do metano pode ser traduzida pela equação química: CH 4(g) + 2 O 2(g) 10 moléculas de CH 4 CO 2(g) + 2 H 2 O(g) 20 moléculas de O 2 reagem com 10 moléculas de CO 2 originam 20 moléculas de H 2 O e
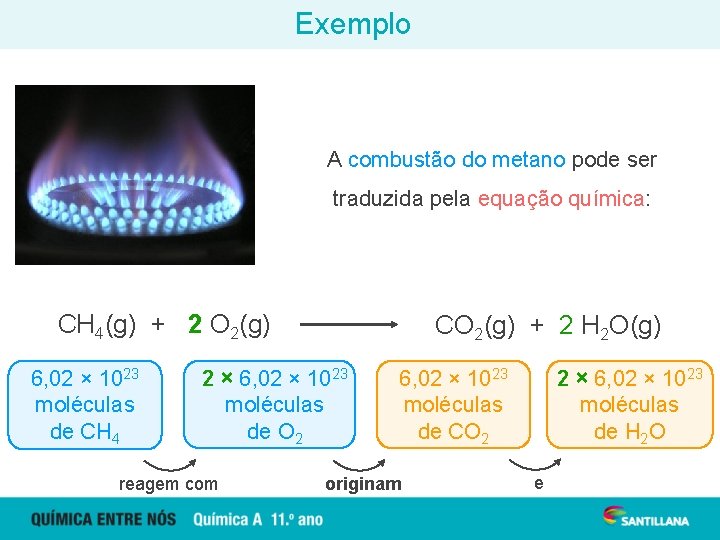
Exemplo A combustão do metano pode ser traduzida pela equação química: CH 4(g) + 2 O 2(g) 6, 02 × 1023 moléculas de CH 4 CO 2(g) + 2 H 2 O(g) 2 × 6, 02 × 1023 moléculas de O 2 reagem com 2 × 6, 02 × 1023 moléculas de H 2 O 6, 02 × 1023 moléculas de CO 2 originam e
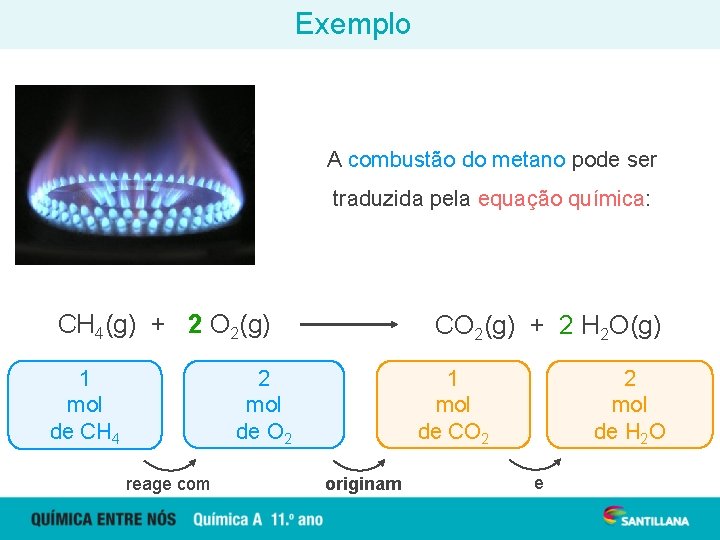
Exemplo A combustão do metano pode ser traduzida pela equação química: CH 4(g) + 2 O 2(g) 6, 02 1 x 1023 moléculas mol de CH 4 CO 2(g) + 2 H 2 O(g) 2 x 6, 02 2 x 1023 moléculas mol de O 2 reage com 2 x 1023 2 x 6, 02 mol de moléculas de. HH 2 O 2 O 6, 02 1 x 1023 moléculas mol de CO 2 originam e

1. 1 Aspetos quantitativos das reações químicas 1. 1. 4 Marcos históricos das reações químicas

Em 1828, o químico alemão Friedrich Whöler (1800 -1882) sintetizou a ureia. Até então, julgava-se que a ureia, presente na urina, apenas podia ser produzida pelos seres vivos.
![Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH](http://slidetodoc.com/presentation_image_h/03f7dde8c771f502c65ab9b595f32805/image-47.jpg)
Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH 4 CNO + Pb Hidróxido de amónio NH 4 CNO Cianato de amónio ∆ Chumbo (NH 2)2 CO Ureia Whöler foi o primeiro a verificar que dois compostos podiam ter a mesma fo rmula molecular e apresentar propriedades diferentes.
![Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH](http://slidetodoc.com/presentation_image_h/03f7dde8c771f502c65ab9b595f32805/image-48.jpg)
Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH 4 CNO + Pb Hidróxido de amónio Cianato de amónio ∆ NH 4 CNO Cianato de amónio Ureia NH 4 CNO (NH 2)2 CO Fórmula molecular CH 4 N 2 O (NH 2)2 CO molecular = CH 4 N 2 O Chumbo
![Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH](http://slidetodoc.com/presentation_image_h/03f7dde8c771f502c65ab9b595f32805/image-49.jpg)
Síntese de Whöler [Pb(CNO)2] + 2 NH 4 OH Cianato de chumbo 2 NH 4 CNO + Pb Hidróxido de amónio NH 4 CNO Cianato de amónio ∆ (NH 2)2 CO Ureia Whöler abriu o caminho para a descoberta da relac a o entre estrutura e propriedades, ta o importante atualmente. Chumbo

Em 1856, o britânico William Perkin produziu o primeiro William Perkin (1838 -1907) corante artificial. Perkin pretendia sintetizar quinina, utilizada no tratamento da malária. Em vez de quinina, sintetizou mauveína, de cor púrpura.
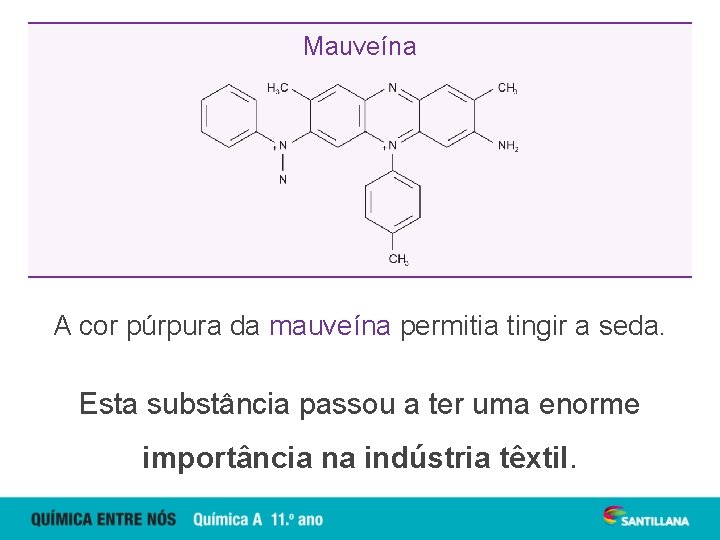
Mauveína A cor púrpura da mauveína permitia tingir a seda. Esta substância passou a ter uma enorme importância na indústria têxtil.

Todos os dias são descobertos novos compostos, sendo já conhecidos mais de 100 milhões. O conhecimento das reações químicas permite desenvolver novos compostos e materiais, que contribuem para o bem-estar da sociedade.

A Química avança constantemente, gerando novos benefícios para o desenvolvimento económico e a qualidade de vida das populações. Graças à Química, o Homem dispõe atualmente de medicamentos que permitem superar doenças até há pouco consideradas mortais.
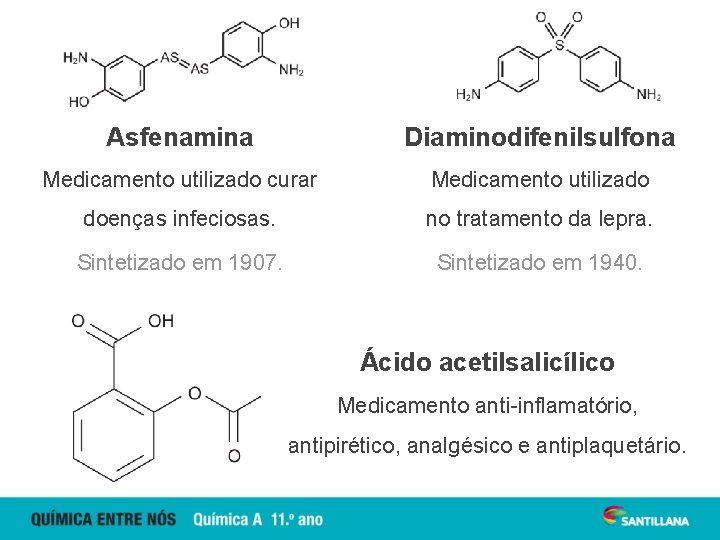
Asfenamina Diaminodifenilsulfona Medicamento utilizado curar Medicamento utilizado doenças infeciosas. no tratamento da lepra. Sintetizado em 1907. Sintetizado em 1940. Ácido acetilsalicílico Medicamento anti-inflamatório, antipirético, analgésico e antiplaquetário.

Conclusão • Numa reação química, há formação de novas substâncias. • Numa reação química, o número total de átomos de cada elemento presente no sistema reacional mantém-se constante.

Conclusão • No decorrer de uma reação química, há conservação da massa total do sistema — Lei de Lavoisier.
- Slides: 56