1 Quanti sono gli orbitali contenenti elettroni in

1 - Quanti sono gli orbitali contenenti elettroni in un atomo il cui numero atomico è Z = 16 ? A 9 B 8 C 7 D 6

2 A B C D Qual è la configurazione elettronica dell'elemento con numero atomico Z = 23 ? 1 s 2, 2 s 2 p 6, 3 s 2 p 6, 4 s 2 1 s 2, 2 s 2 p 6, 3 s 2 p 6 d 3, 4 s 2 1 s 2, 2 s 2 p 6, 3 s 2 p 6 d 4 1 s 2, 2 s 2 p 6, 3 s 23 p 6, 4 s 1

1. Il legame di coordinazione o dativo è un legame: A ionico B a idrogeno C covalente D dipolo-dipolo E doppio

3 A B C D A quale gruppo della tavola periodica appartiene l'elemento con numero atomico Z = 9 ? 2° 13° 15° 17° 1 H 2 He 1 s 1 s 2 3 4 Li Be 2 s 5 B 7 N 8 O 9 F 10 Ne 2 s 2 p 2 2 s 2 p 3 2 s 2 p 4 2 s 2 p 5 2 s 2 p 6 2 s 2 13 14 15 16 17 18 Al Si P S Cl Ar 11 12 Na Mg 3 s 6 C 3 s 2 p 2 3 s 2 p 3 3 s 2 p 4 3 s 2 p 5 3 s 2 p 6 3 s 2 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 4 s 4 s 2 3 d, 4 s 2 3 d 2, 4 s 2 3 d 3, 4 s 2 3 d 5, 4 s 2 3 d 6, 4 s 2 3 d 7, 4 s 2 3 d 8, 4 s 2 3 d 10, 4 s 2 p 2 4 s 2 p 3 4 s 2 p 4 4 s 2 p 5 4 s 2 p 6 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 5 s 5 s 2 4 d, 5 s 2 4 d 2, 5 s 2 4 d 3, 5 s 2 4 d 5, 5 s 2 4 d 6, 5 s 2 4 d 7, 5 s 2 4 d 8, 5 s 2 4 d 10, 5 s 2 p 2 5 s 2 p 3 5 s 2 p 4 5 s 2 p 5 5 s 2 p 6

4 - Quale fra i seguenti elementi ha più spiccato carattere metallico ? A L'elemento con numero atomico Z = 11 B L'elemento con numero atomico Z = 12 C L'elemento con numero atomico Z = 13 D L'elemento con numero atomico Z = 14 1 H 2 He 1 s 1 s 2 3 4 Li Be 2 s 5 B 7 N 8 O 9 F 10 Ne 2 s 2 p 2 2 s 2 p 3 2 s 2 p 4 2 s 2 p 5 2 s 2 p 6 2 s 2 13 14 15 16 17 18 Al Si P S Cl Ar 11 12 Na Mg 3 s 6 C 3 s 2 p 2 3 s 2 p 3 3 s 2 p 4 3 s 2 p 5 3 s 2 p 6 3 s 2 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 4 s 4 s 2 3 d, 4 s 2 3 d 2, 4 s 2 3 d 3, 4 s 2 3 d 5, 4 s 2 3 d 6, 4 s 2 3 d 7, 4 s 2 3 d 8, 4 s 2 3 d 10, 4 s 2 p 2 4 s 2 p 3 4 s 2 p 4 4 s 2 p 5 4 s 2 p 6 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 5 s 5 s 2 4 d, 5 s 2 4 d 2, 5 s 2 4 d 3, 5 s 2 4 d 5, 5 s 2 4 d 6, 5 s 2 4 d 7, 5 s 2 4 d 8, 5 s 2 4 d 10, 5 s 2 p 2 5 s 2 p 3 5 s 2 p 4 5 s 2 p 5 5 s 2 p 6

6. Il legame è ionico nel composto di formula: A CH 3 COOH B KCl C CO 2 D NH 3 E H 2 O

5 - Quale tra gli elementi proposti possiede il Potenziale di Ionizzazione più elevato? A A Z=3 B Z = 11 C Z = 19 D Z = 37 H 1312 Li 520 Be 899 Na 496 Mg 738 K 419 Ca 599 Sc 631 Ti 658 Rb 403 Sr 550 Y 617 Zr 661 Cs 377 Ba 503 La 538 Hf 681

6 A B C D D Il numero atomico dell'elemento (M) il cui anione M- ha configurazione elettronica 1 s 2, 2 s 2 p 6, 3 s 2 p 6, è 14 15 16 17 1 H 2 He 1 s 1 s 2 3 4 Li Be 2 s 5 B 7 N 8 O 9 F 10 Ne 2 s 2 p 2 2 s 2 p 3 2 s 2 p 4 2 s 2 p 5 2 s 2 p 6 2 s 2 13 14 15 16 17 18 Al Si P S Cl Ar 11 12 Na Mg 3 s 6 C 3 s 2 p 2 3 s 2 p 3 3 s 2 p 4 3 s 2 p 5 3 s 2 p 6 3 s 2 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 4 s 4 s 2 3 d, 4 s 2 3 d 2, 4 s 2 3 d 3, 4 s 2 3 d 5, 4 s 2 3 d 6, 4 s 2 3 d 7, 4 s 2 3 d 8, 4 s 2 3 d 10, 4 s 2 p 2 4 s 2 p 3 4 s 2 p 4 4 s 2 p 5 4 s 2 p 6 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 5 s 5 s 2 4 d, 5 s 2 4 d 2, 5 s 2 4 d 3, 5 s 2 4 d 5, 5 s 2 4 d 6, 5 s 2 4 d 7, 5 s 2 4 d 8, 5 s 2 4 d 10, 5 s 2 p 2 5 s 2 p 3 5 s 2 p 4 5 s 2 p 5 5 s 2 p 6

Tra gli orbitali 4 s, 4 p, 5 s, 4 d, 5 p, quale è occupato preferenzialmente da un elettrone? A 4 s B 4 p C 5 s D 4 d E 5 p La risposta esatta è A perché: L’elettrone occupa l’orbitale disponibile a minor energia Poiché l’energia degli orbitali aumenta all’aumentare di n, in questo caso sarà occupato per primo uno dei tre orbitali del quarto livello energetico. Dato poi che a parità di n l’energia aumenta all’aumentare del numero quantico secondario l l’orbitale occupato per primo sarà il 4 s (l=0) mentre 4 p (l=1) 4 d (l=2)

Sapendo che ZMg=12; ZNa=11; ZNe=10; ZF=9; ZO=8; quale di questi elementi possiede la seguente configurazione elettronica: 1 s 2 2 p 6? A Mg B Na C Ne D F E O La risposta esatta è C perché: Se facciamo il calcolo del numero degli elettroni totali vediamo che è 10. Il numero degli elettroni è uguale a quello dei protoni e pertanto l’atomo con Z= 10 è il Neon

La differenza fra gli isotopi 127 e 131 dello iodio consiste nel fatto che ? A il primo possiede due protoni e due neutroni in meno B il primo possiede quattro protoni in meno C il primo possiede quattro neutroni in meno D il primo possiede quattro elettroni in meno E il secondo possiede quattro protoni in più La risposta esatta è C perché: Due isotopi hanno lo stesso numero atomico, ma diverso numero di massa e pertando da un diverso numero di neutroni. Lo 127 I possiede quattro neutroni in meno dello 131 I

Litio e potassio: A possiedono lo stesso numero di elettroni nell’ultimo livello B sono entrambi non metalli C appartengono entrambi al secondo gruppo del sistema periodico D possiedono lo stesso numero di protoni nel nucleo E appartengono allo stesso periodo del sistema periodico La risposta esatta è A perché: Li e K sono due metalli appartenenti al gruppo I. Il Li ha Z=3 e pertanto appartiene al secondo periodo, il K ha Z= 19 e pertanto configurazione elettronica 1 s 2 2 s 22 p 6 3 s 23 p 6 4 s 1 e pertanto appartiene al 4 periodo.

L’affinità elettronica: A è maggiore nel potassio che nel litio B è maggiore nel fluoro che nell’ossigeno C è maggiore nel fosforo che nell’azoto D è minore nel carbonio che nel litio E è minore nell’ossigeno che nello zolfo La risposta esatta è B perché: Energia che si libera quando un atomo neutro acquista un e Aumenta lungo i periodi e diminuisce nei gruppi Li e K fanno parte rispettivamente del 2 e 4 periodo quindi l’AE è maggiore nel Li che nel K. Li (I) e C (XIV) entrambi del secondo periodo. L’AE è maggiore nel C che nel Li. N e P (XV) e O e S (XVI) sono due coppie di atomi di cui il primo (N e O) appartiene al 2 periodo e il secondo (P e S) al terzo periodo. Quindi le risposte C e E sono da scartare. F e O appartengono entrambi al 2 periodo (XVI e XVII).

Il volume di 22, 4 litri è quello occupato da: A 1 mole di azoto liquido B 1 Kg di acqua allo stato di vapore C 1 mole di qualunque gas in condizioni standard D 1 equivalente di una soluzione molare E 1 mole di qualunque sostanza alle condizioni standard

Il numero quantico di spin: A ha sempre valore (n-1), dove n rappresenta il numero quantico principale B può assumere tutti i valori interi da n a –n, zero compreso C fornisce indicazioni sulla distanza dell’elettrone dal nucleo D fornisce indicazioni sul verso della rotazione dell’elettrone intorno al proprio asse E fornisce indicazioni sul tipo di orbitale in cui l’elettrone è contenuto La risposta esatta è D perché: Può assumere solo due valor: +1/2 o -1/2 ed è correlato al senso di rotazione dell’elettrone intorno al proprio asse

Gli alogeni hanno configurazione elettronica esterna di tipo : A s 2 p 3 B s 2 p 5 C s 2 D s 2 p 6 E s 2 p 4 La risposta esatta è B perché: Gli alogeni sono elementi del XVII gruppo

2. Un composto ionico si dissocia se sciolto in un solvente: A molto volatile B polare C poco volatile D apolare E organico con bassa costante dielettrica

3. Indicare in quale delle seguenti sostanze il legame è dovuto principalmente a forze elettrostatiche: A sodio B cloruro di sodio C acido cloridrico D diamante E metano
2. L’elemento con numero atomico Z = 30 è un alogeno V F

4. I cristalli di iodio costituiscono un esempio classico di solido: A ionico B molecolare C covalente D metallico E amorfo

5. Quando due atomi si legano, per energia di legame si intende: A l’energia acquistata dagli atomi per la formazione del legame B l’energia perduta dagli atomi per la formazione del legame C l’energia donata da un atomo all’altro nella formazione del legame D la somma del contenuto energetico di ciascun elettrone coinvolto nel legame E l’energia di attivazione

7. Un legame covalente polare si può formare fra: A due elementi di diversa elettronegatività B due ioni di segno opposto C un atomo di potassio e uno di sodio D due atomi uguali E un atomo di cloro e uno di sodio

8. Quale è la definizione corretta di molecola? A L’atomo più piccolo e caratteristico di un elemento. B La più piccola quantità di un elemento di cui mantiene le caratteristiche fisiche. C La più piccola quantità di un composto di cui mantiene le caratteristiche chimiche e fisiche D La più piccola quantità di un elemento di cui mantiene le caratteristiche chimiche E La più piccola quantità di un elemento allo stato solido

9. Il legame tra l’ossigeno e l’idrogeno in una molecola di acqua è: A ionico B a idrogeno C dativo D covalente E di coordinazione
4. Il legame σ che contraggono due atomi di azoto nella molecola N 2 si forma per sovrapposizione di due orbitali 3 p V F
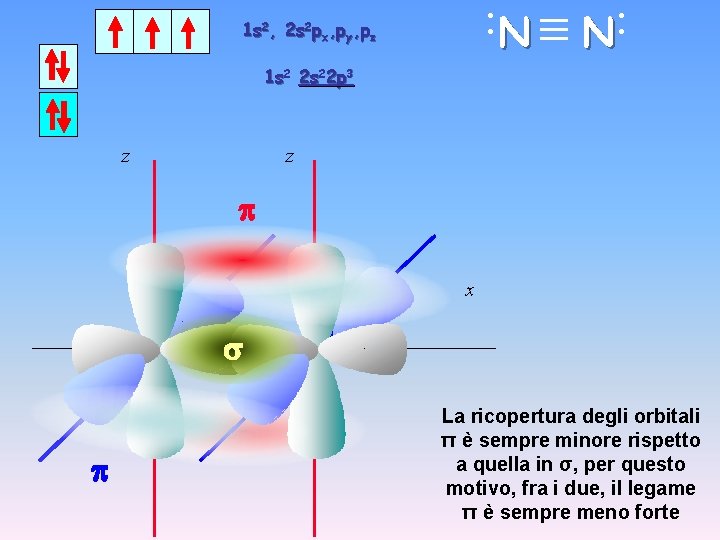
N • • N 1 s 2, 2 s 2 px, py, pz 1 s 2 2 s 22 p 3 z z p x s p La ricopertura degli orbitali π è sempre minore rispetto a quella in σ, per questo motivo, fra i due, il legame π è sempre meno forte

10. Quale fra le seguenti molecole non è polare: A NH 3 B H 2 O C HCl D CO 2 E CH 3 OH

11. Il legame chimico presente tra due atomi di carbonio appartenenti ad una catena idrocarburica satura è: A ionico B covalente C dativo D metallico E sempre polarizzato

12. Una delle seguenti caratteristiche è comune allo ione ammonio e al tetracloruro di carbonio: A la carica elettrica B la struttura spaziale C le spiccate proprietà basiche D le spiccate proprietà acide E l’energia di legame tra gli atomi costituenti le rispettive molecole

13. Nella molecola di H 2 O l’angolo H-O è pari a: A 90° B 180° C 109, 5° D 45° E 120°

14. Il legame a idrogeno: A è un legame forte B è presente nell’acqua allo stato solido e a quello liquido C è un legame covalente debole D è presente nel cicloesano E si stabilisce fra molecole polari

15. Per doppio legame si intende: A un legame covalente fra tre molecole B un legame fra ioni monovalenti C un legame tra ioni bivalenti D un legame derivante dalla compartecipazione di due coppie di elettroni E un legame tra due atomi
9. La massa molecolare relativa del diidrogenofosfato (V) di potassio è 174, 17 Pmr(30, 97), Kmr(39) V F

9. La massa molecolare relativa del diidrogenofosfato (V) di potassio è data da

La mole di una proteina pesa 60 Kg; nella mole in questione sono contenuti: A 60 aminoacidi B 6000 aminoacidi C 60. 000 molecole D 6, 023 x 1023 molecole di proteina E 6, 023 x 1023 molecole di aminoacidi
10. La tensione interfacciale fra acqua e benzene è più bassa di quella fra acqua e mercurio perché fra acqua e mercurio si possono contrarre legami a idrogeno V F

Il peso atomico del cloro è un numero decimale (35, 453) e non un numero intero (35) perchè ? A ogni atomo di cloro ha massa uguale a 35, 453 B tutti gli atomi di cloro hanno proprietà identiche C ci sono almeno due isotopi naturali del cloro D ogni atomo di cloro contiene 17 protoni E ogni atomo di cloro contiene 17 neutroni La risposta esatta è C perché: Ogni elemento è presente come miscela di isotopi Il PA è in pratica una media pesata dei pesi atomici degli isotopi e non può essere un numero intero

Un litro di acqua contiene circa: A 55 moli B 55 molecole C 55 grammi D 5, 5 moli E 55 x 1023 moli La risposta esatta è A perché: Il PM dell’acqua è 16(PAO)+ 2 x 1(PAH) = 18 1 lt di H 2 O pesa 1000 g quindi il n. di moli contenute sono: n H 2 O = 1000 g / 18 g mol-1 = 55 mol
11. Il numero di ossidazione del cloro nel pentossido di dicloro è +4 V F
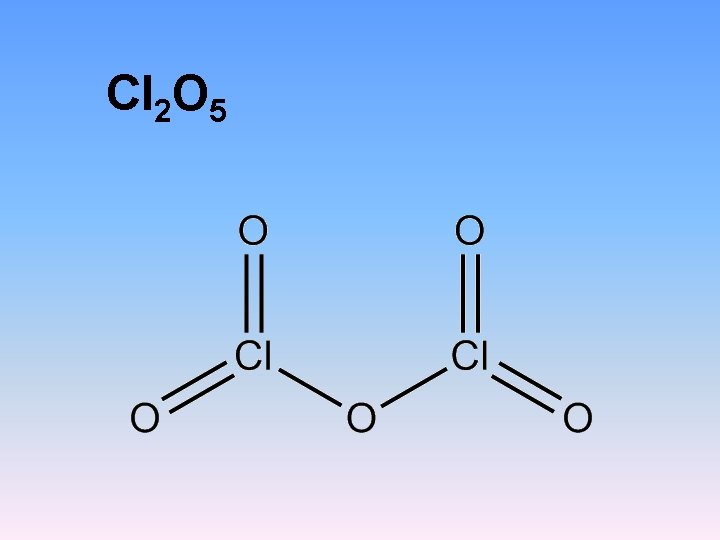
Cl 2 O 5

Quale delle seguenti affermazioni è corretta? A Una molecola di ossigeno pesa 32 g B Una molecola di ossigeno pesa 16 g C Una mole di ossigeno pesa 32 g D Una mole di ossigeno pesa 16 g E Una mole di ossigeno pesa 8 g La risposta esatta è C perché: L’ossigeno non è presente in natura come O, ma come molecola O 2 Il PM dell’O 2 è 32 g, quindi una mole di ossigeno pesa 32 g

Quanti grammi pesano 11, 2 litri di CH 4 in condizioni standard? A 11 B 10 C 16 D 8 E 4 La risposta esatta è D perché: In condizioni standard (P= 1 atm e T= 10 C) una mole di qualsiasi gas occupa 22, 4 litri 11, 2 litri sono quindi 0, 5 moli di CH 4
- Slides: 42