1 La configurazione elettronica dellelemento con numero atomico


















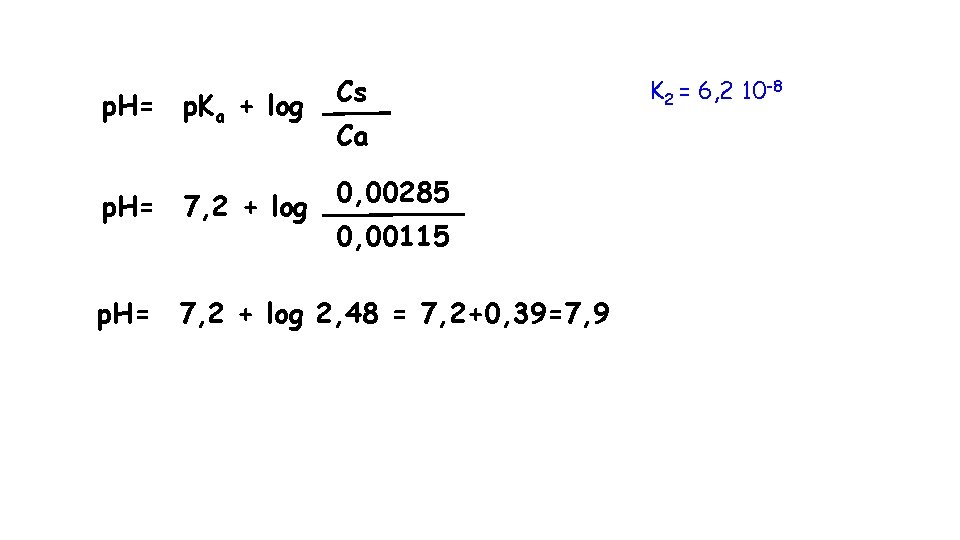
- Slides: 36

1 La configurazione elettronica dell'elemento con numero atomico Z = 21 è la seguente: 1 s 2, 2 p 6, 3 s 2, p 6, d 3 V F

2 La configurazione elettronica dello ione K+ è 1 s 2, 2 s 2 p 6, 3 s 2 p 6 V F

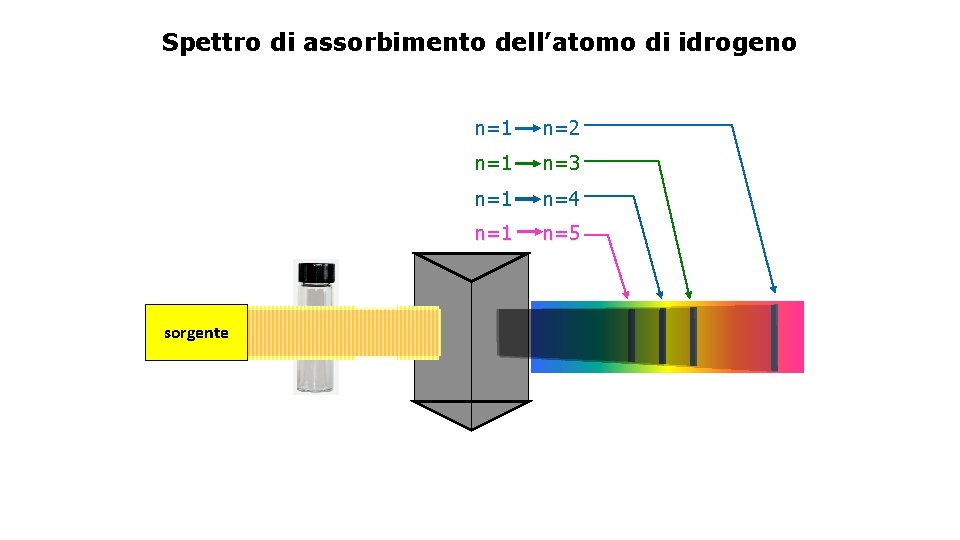
3 Nello spettro di assorbimento di un elemento sono assenti le stesse lunghezze d’onda che quell’elemento emette quando viene eccitato V F

Spettro di assorbimento dell’atomo di idrogeno sorgente n=1 n=2 n=1 n=3 n=1 n=4 n=1 n=5

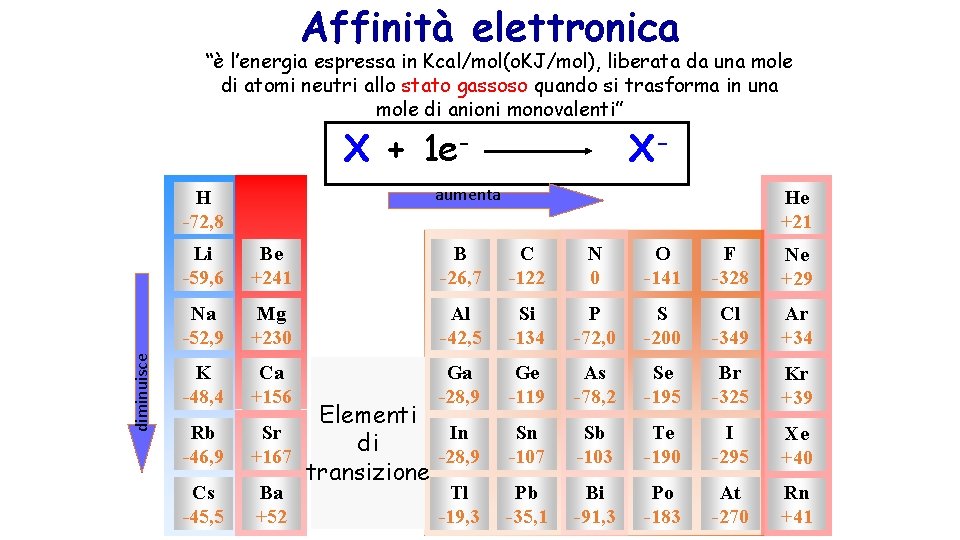
4 L’affinità per l’elettrone del Cloro è maggiore di quella dello Zolfo V F

Affinità elettronica “è l’energia espressa in Kcal/mol(o. KJ/mol), liberata da una mole di atomi neutri allo stato gassoso quando si trasforma in una mole di anioni monovalenti” X + 1 e- aumenta H -72, 8 diminuisce X- He +21 Li -59, 6 Be +241 B -26, 7 C -122 N 0 O -141 F -328 Ne +29 Na -52, 9 Mg +230 Al -42, 5 Si -134 P -72, 0 S -200 Cl -349 Ar +34 K -48, 4 Ca +156 Ga -28, 9 Ge -119 As -78, 2 Se -195 Br -325 Kr +39 Sn -107 Sb -103 Te -190 I -295 Xe +40 Pb -35, 1 Bi -91, 3 Po -183 At -270 Rn +41 Rb -46, 9 Cs -45, 5 Elementi Sr In di +167 -28, 9 transizione Ba +52 Tl -19, 3

5 A causa del carattere omopolare dei suoi orbitali molecolari, fra due molecole di bromo non possono contrarsi legami di van der Waals V F

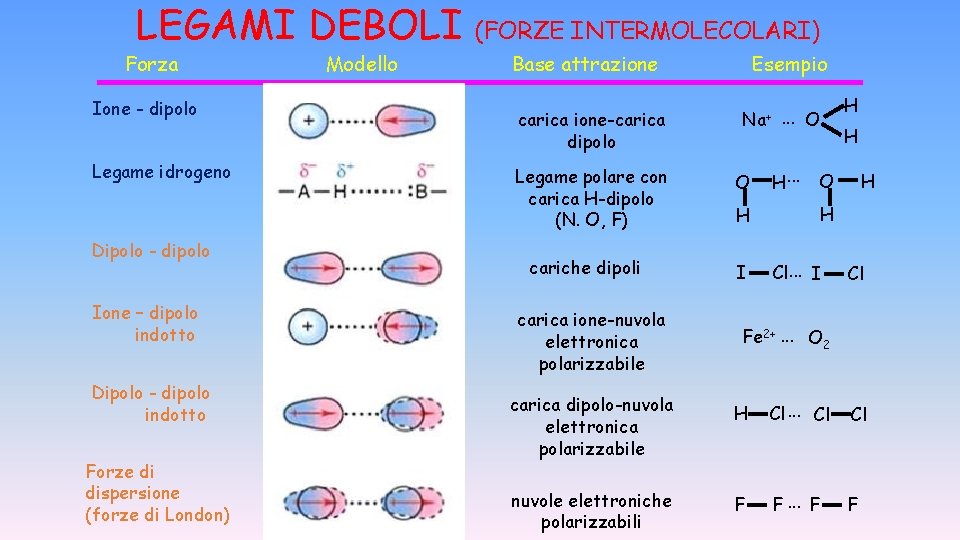
LEGAMI DEBOLI Forza Ione - dipolo Legame idrogeno Dipolo - dipolo Ione – dipolo indotto Dipolo - dipolo indotto Forze di dispersione (forze di London) Modello (FORZE INTERMOLECOLARI) Base attrazione carica ione-carica dipolo Legame polare con carica H-dipolo (N. O, F) cariche dipoli carica ione-nuvola elettronica polarizzabile Esempio Na+ O H I . . . O H. . . H H O H H Cl. . . I Cl Fe 2+. . . O 2 carica dipolo-nuvola elettronica polarizzabile H Cl. . . Cl Cl nuvole elettroniche polarizzabili F F. . . F F

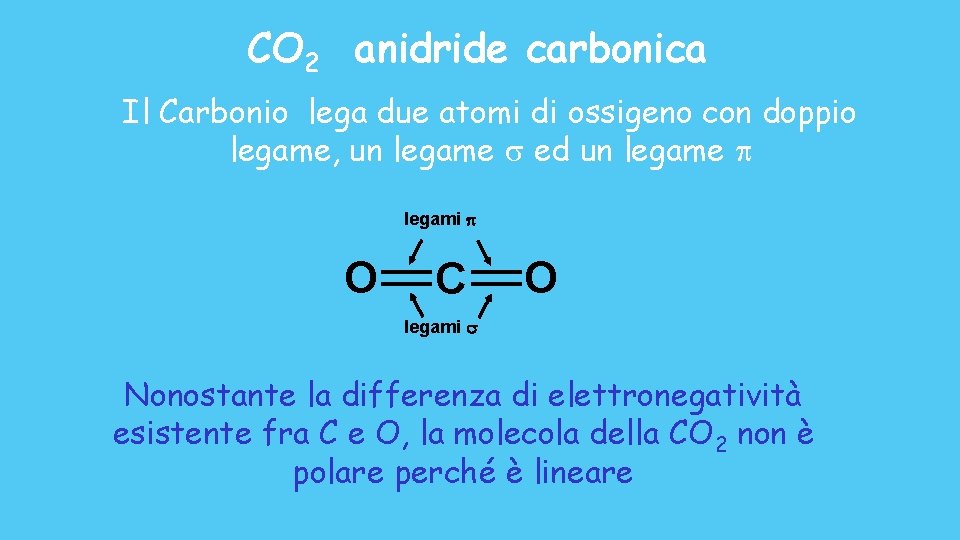
6 A causa della ibridazione sp 2 degli orbitali di valenza del carbonio, il biossido di carbonio è una molecola apolare V F

CO 2 anidride carbonica Il Carbonio lega due atomi di ossigeno con doppio legame, un legame s ed un legame legami p O C O legami s Nonostante la differenza di elettronegatività esistente fra C e O, la molecola della CO 2 non è polare perché è lineare

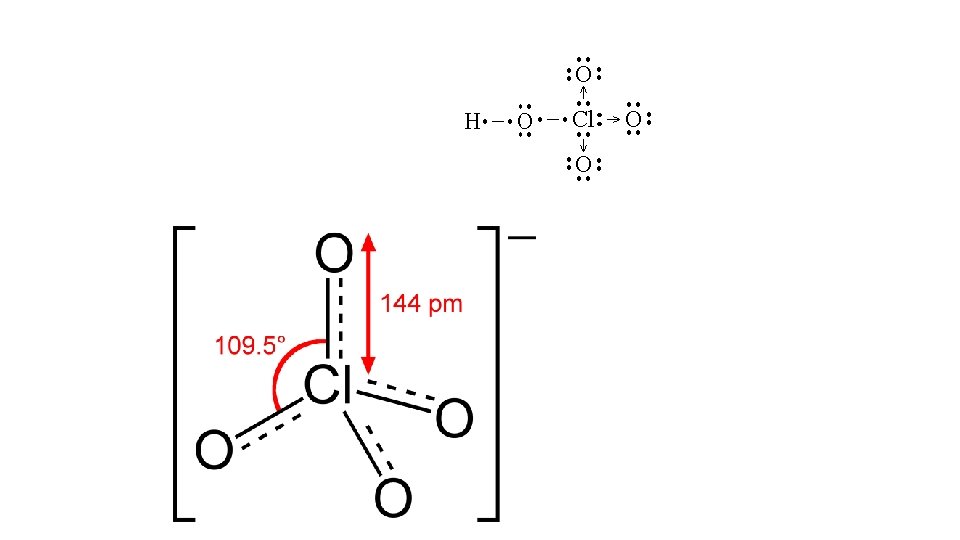
7 L’anione clorato (VII) presenta una carica negativa delocalizzata su un atomo di ossigeno V F


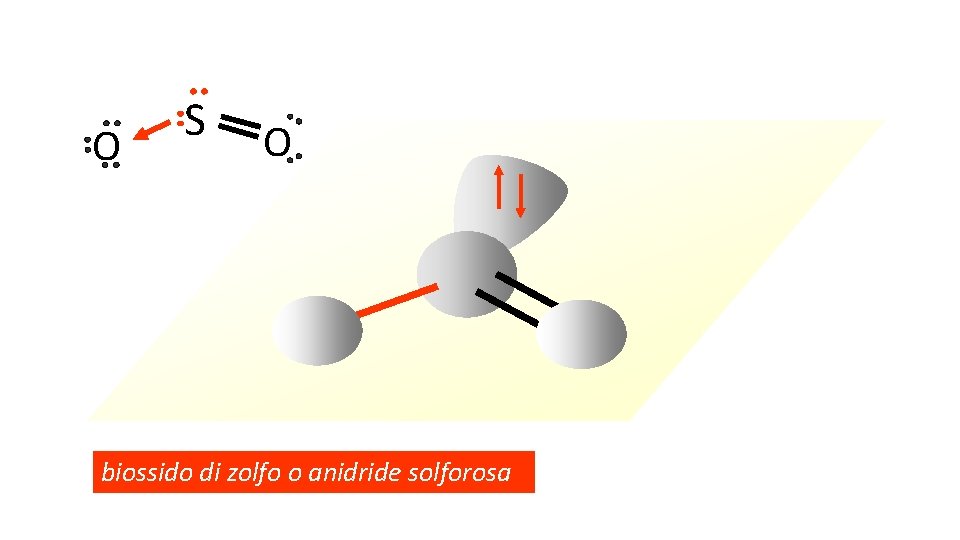
8 Per il principio della VSEPR, gli orbitali dello zolfo nel diossido di zolfo sono ibridati sp 2 V F

Teoria VSEPR Teoria che prevede la geometria delle molecole e si basa sulla repulsione tra i doppietti elettronici del guscio di valenza Valence Shell Electron Pair Repulsion Secondo tale teoria le coppie di elettroni più esterne, avendo tutte la stessa carica negativa, tendono a respingersi le une con le altre e a disporsi il più possibile lontano AXm. En A =atomo centrale X=atomi legati all’atomo centrale E= doppietti elettronici solitari m+n= 2 molecola lineare m+n=3 molecola trigonale planare m+n=4 molecola tetraedrica m+n=5 bipiramide a base trigonale m+n=6 ottaedrica

O S O biossido di zolfo o anidride solforosa

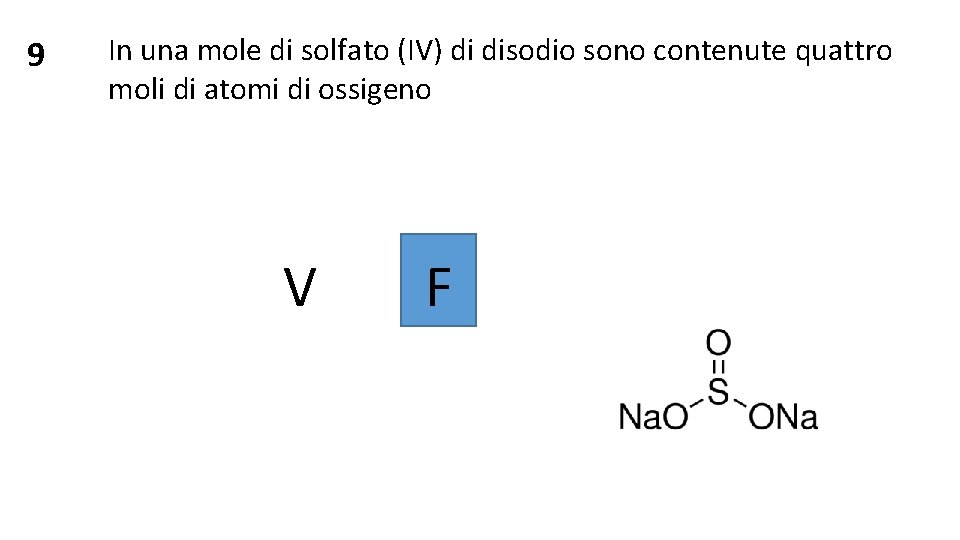
9 In una mole di solfato (IV) di disodio sono contenute quattro moli di atomi di ossigeno V F

10 Una bombola contiene 3 moli di ossigeno, 6 moli di elio e 15 moli di anidride carbonica, a 25°C. La pressione parziale dell'anidride carbonica è 5 atm. Che valore ha la pressione totale? P • V=n • R • T Pa = Ptot • Xa XCO 2 =15/24 =0. 625 Ptot = PCO 2 • XCO 2 Ptot = 5 • 0. 625=8

11 4 moli di Azoto (PM = 28) sono mantenute a P = 4 atm e T = 0°C. Qual è il volume occupato? P • V=n • R • T V = n • R • T/ P V = 4 • 0, 0821 • 273, 16/ 4= 22, 4

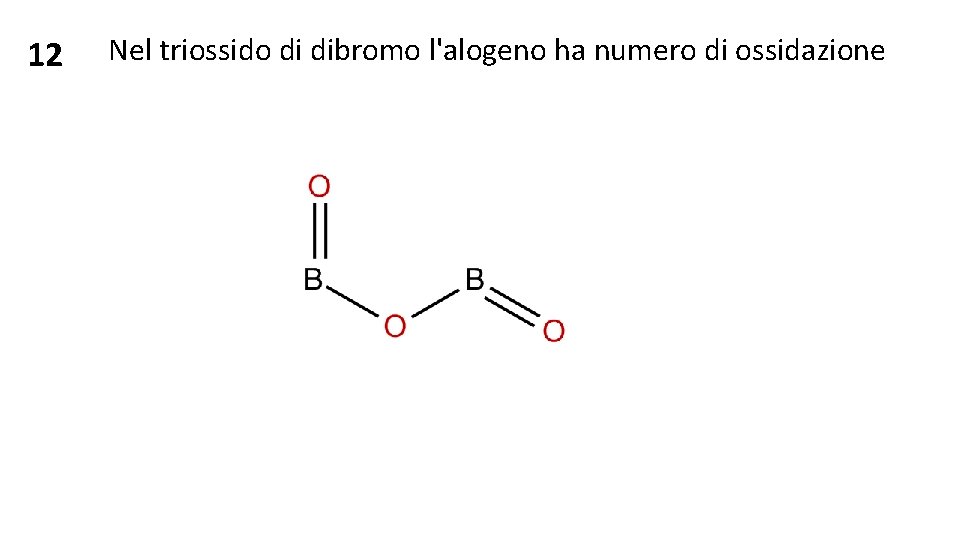
12 Nel triossido di dibromo l'alogeno ha numero di ossidazione

13 Identificare la corretta combinazione dei coefficienti stechiometrici dopo aver bilanciato la seguente reazione redox. IO 3 - + H 2 S I 2 + SO 3 -- + H 2 O + H+ + 10 e + 12 H+ 2 IO 3 - I + 6 H 2 O 2 2+ H 2 S SO + 3 H 2 O 3 + 6 e + 8 H x 3 x 5 6 IO 3 - + 36 H+ + 5 H 2 S + 15 H 2 O 3 I 2 + 18 H 2 O + 5 SO 32 - + 40 H+ 6 IO 3 - + 5 H 2 S 3 I 2 + 5 SO 32 - +3 H 2 O + 4 H+ 6 HIO 3 + 5 H 2 S 3 I 2 + 5 H 2 SO 3 +3 H 2 O RED OX

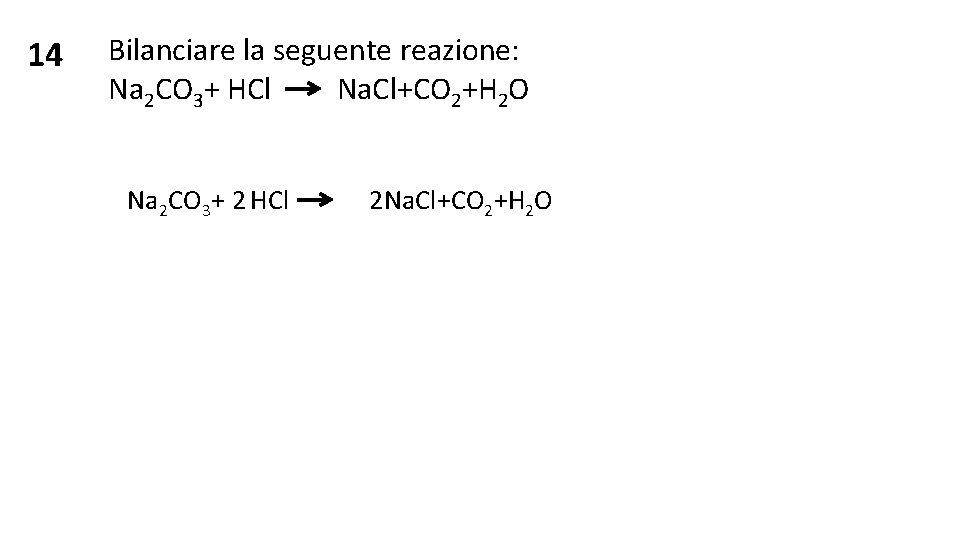
14 Bilanciare la seguente reazione: Na 2 CO 3+ HCl Na. Cl+CO 2+H 2 O Na 2 CO 3+ HCl Na. Cl+CO 2 2 2+H 2 O

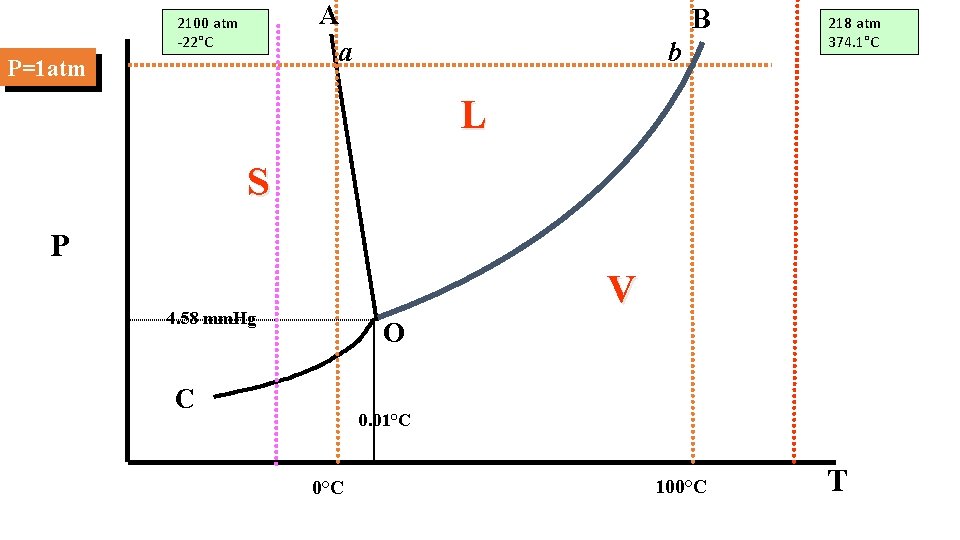
15 A pressioni superiori a quella del punto triplo la sublimazione del solido non è possibile V F

A a 2100 atm -22°C P=1 atm B b 218 atm 374. 1°C L S P V 4. 58 mm. Hg O C 0. 01°C 0°C 100°C T

16 18 g di glucosio (C 6 H 12 O 6) sono disciolti con acqua fino al volume di 500 ml. La concentrazione della soluzione è M=n moli/Vol n moli = g/PM PM C 6 H 12 O 6 = 180 n moli = 18/180 = 0. 1 M=0. 1/0. 5=0. 2

17 Diluendo 50 ml di una soluzione di fosfato (III) di triidrogeno 0. 1 M al volume finale di 200 ml si ottiene una soluzione la cui concentrazione è Mconc x Vconc = Mdil x Vdil 0. 1 x 50 = Mdil x 200 Mdil = 0. 25 N= M x X= 0. 25 x 3= 0. 75

18 10 ml di una soluzione di solfato (VI) di diidrogeno 1. 5 M vengono aggiunti a 500 ml di una soluzione di idrossido di calcio 100 m. M. Si ottiene un precipitato di solfato (VI) di calcio (II) pari a H 2 SO 4+Ca(OH)2 Ca. SO 4 + H 2 O H 2 SO 4= 1. 5 x 0. 01= 0. 015 Ca(OH)2 = 0. 5 x 0. 1= 0. 05 Ca. SO 4 = 0. 015 g= 0. 015 x 136= 2. 04 g PM Ca. SO 4 = 136

19 Calcolare la solubilità (moli/litro) di Mg(OH)2 in una soluzione avente p. H=12 (Kps=1, 2 x 10 -11) Mg(OH)2 Mg 2+ + 2 OH[OH- ]= 10 -2 M s (Mg 2+ )= Kps / [OH-]2 = 1. 2 10 -11/ (10 -2)2 = 1, 2 10 -7 M

20 La soluzione contenente 190. 4 mg di Mg. Cl 2 in 500 ml è isotonica rispetto alla soluzione contenente 720 mg di glucosio in 1 L, alla temperatura di 25°C =Cx. Rx. T PMMg. Cl 2= 95 Mg. Cl 2= (0. 194/95)/0. 5 x 0. 0821 x 298 x 3= 0. 3 PMglucosio= 180 glucosio= (0. 720/180)/1 x 0. 0821 x 298 x 3= 0. 1

21 Una massa di 10 grammi di un polipeptide di peso molecolare non noto viene disciolta nel volume di 400 ml. A 25°C, la pressione osmotica della soluzione è 6. 09 mm Hg. Calcolare il peso molecolare del polipeptide = C x R x T= n/V x R x T n= x V /R x T = 6. 09/760 =0. 008 atm n= 0. 008 x 0. 4 / 0. 0821 x 298 = 0. 00013 PM= g/n moli = 10/ 0. 00013 = 76923

22 A 20°C, la pressione osmotica di una soluzione composta mescolando 25 ml di fosfato (V) di trisodio 10 m. M, 30 ml di solfato (VI) di disodio 5 m. M, 10 ml di cloruro di sodio 50 m. M, 30 ml di glucosio 10 m. M è = C x R x T= ntot/V x R x T n H 3 PO 3= 0. 025 x 0. 01 x 4 = 0. 001 n Na 2 SO 4= 0. 03 x 0. 005 x 3 = 0. 00045 n Na. Cl= 0. 01 x 0. 05 x 2 = 0. 001 n glucosio= 0. 03 x 0. 01 = 0. 0003 n tot= 0. 00275 c Vtot= 95 ml =0. 00275/0. 095 x 0. 0821 x 293= 0. 68 atm

23 In 350 ml di soluzione acquosa sono contenuti 3 g di acido acetico (p. Ka = 4. 74). Il p. H della soluzione è Acidi deboli p. H = ½ p Ka – ½ log Cb p. H= 0. 5 x 4. 74 - 0. 5 x log (3/60) / 0. 35 p. H= 0. 5 x 4. 74 - 0. 5 x log 0. 142 p. H= 0. 5 x 4. 74 - 0. 5 x -0. 84= 2. 37 + 0. 42 = 2. 79

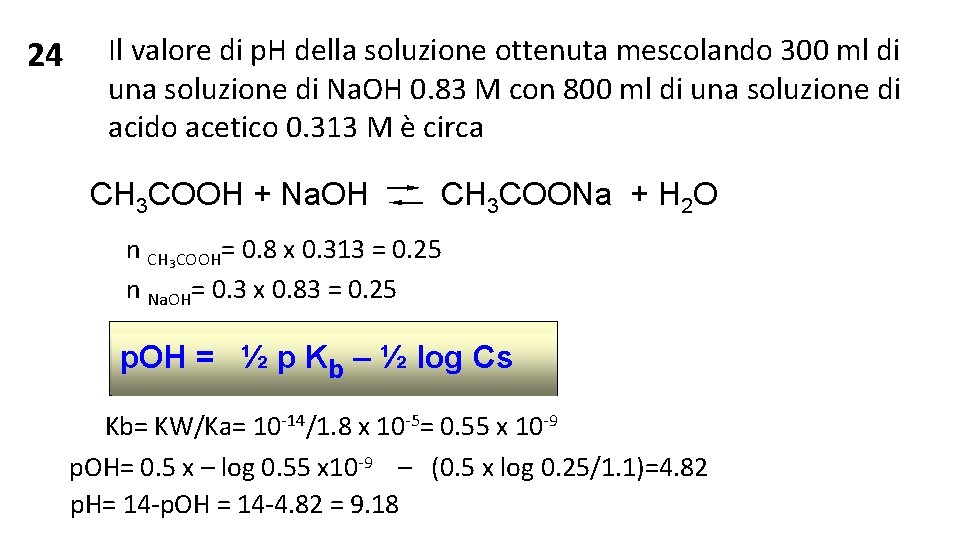
24 Il valore di p. H della soluzione ottenuta mescolando 300 ml di una soluzione di Na. OH 0. 83 M con 800 ml di una soluzione di acido acetico 0. 313 M è circa CH 3 COOH + Na. OH CH 3 COONa + H 2 O n CH 3 COOH= 0. 8 x 0. 313 = 0. 25 n Na. OH= 0. 3 x 0. 83 = 0. 25 p. OH = ½ p Kb – ½ log Cs Kb= KW/Ka= 10 -14/1. 8 x 10 -5= 0. 55 x 10 -9 p. OH= 0. 5 x – log 0. 55 x 10 -9 – (0. 5 x log 0. 25/1. 1)=4. 82 p. H= 14 -p. OH = 14 -4. 82 = 9. 18

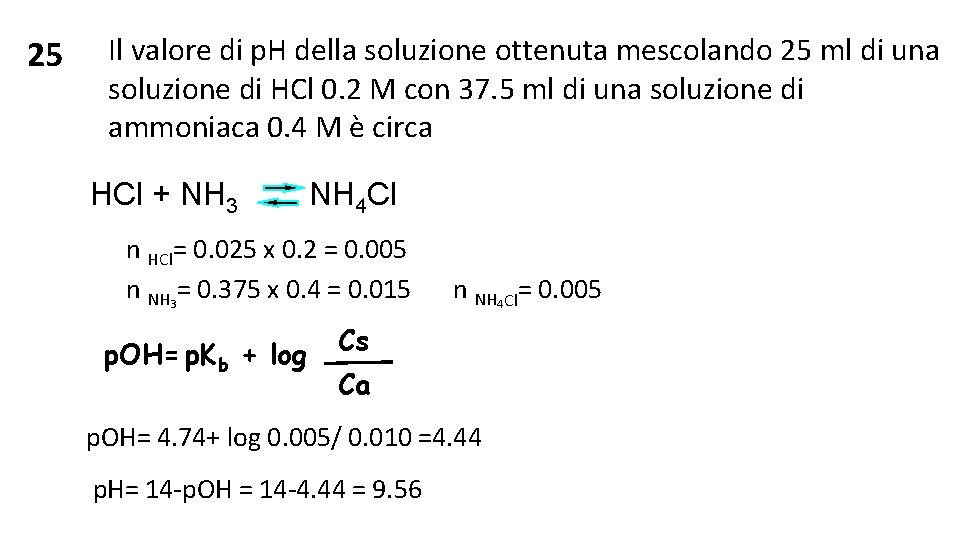
25 Il valore di p. H della soluzione ottenuta mescolando 25 ml di una soluzione di HCl 0. 2 M con 37. 5 ml di una soluzione di ammoniaca 0. 4 M è circa HCl + NH 3 NH 4 Cl n HCl= 0. 025 x 0. 2 = 0. 005 n NH 3= 0. 375 x 0. 4 = 0. 015 p. OH= p. Kb + log n NH 4 Cl= 0. 005 Cs Ca p. OH= 4. 74+ log 0. 005/ 0. 010 =4. 44 p. H= 14 -p. OH = 14 -4. 44 = 9. 56

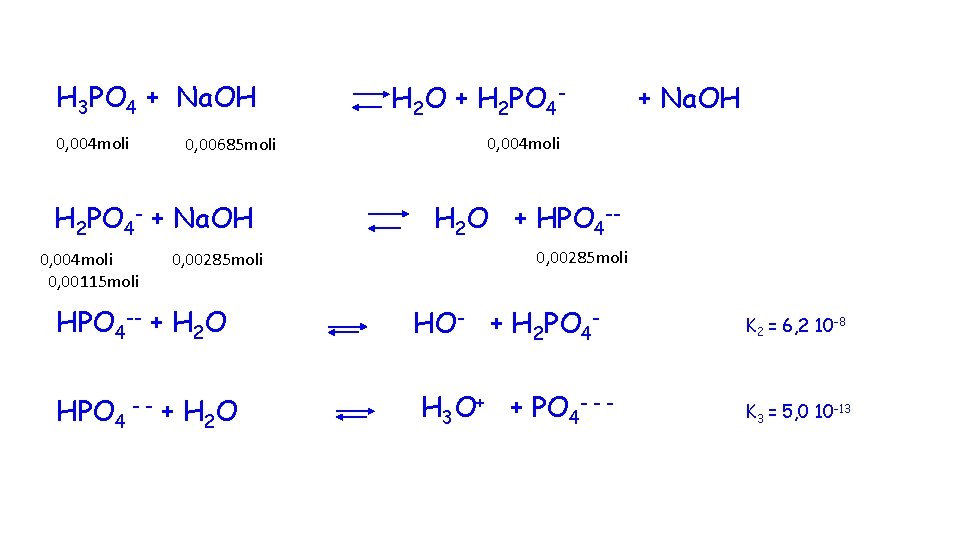
26 Il valore di p. H della soluzione ottenuta mescolando 40 ml di una soluzione di H 3 PO 4 0. 1 M con 50 ml di una soluzione di idrossido di sodio 137 m. M è circa

H 3 PO 4 + Na. OH 0, 004 moli 0, 00685 moli H 2 PO 4 - + Na. OH 0, 004 moli 0, 00115 moli 0, 00285 moli H 2 O + H 2 PO 4 - + Na. OH 0, 004 moli H 2 O + HPO 4 -0, 00285 moli HPO 4 -- + H 2 O HO- + H 2 PO 4 - HPO 4 - - + H 2 O H 3 O+ + PO 4 - - - K 2 = 6, 2 10 -8 K 3 = 5, 0 10 -13
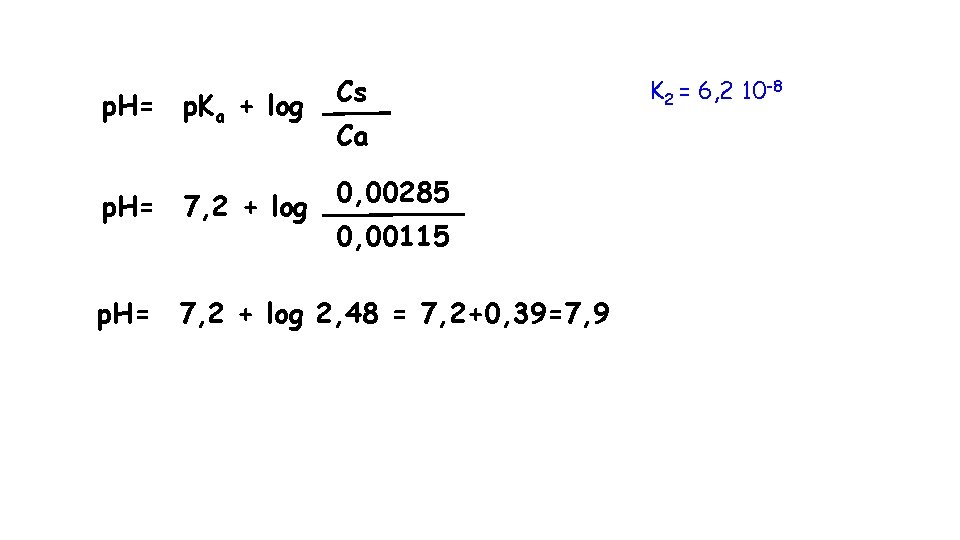
p. H= p. Ka + log Cs Ca 0, 00285 p. H= 7, 2 + log 0, 00115 p. H= 7, 2 + log 2, 48 = 7, 2+0, 39=7, 9 K 2 = 6, 2 10 -8