1 Equilibri acidobase prima parte Classificazione delle sostanze

1 Equilibri acido-base (prima parte)

Classificazione delle sostanze come acidi o basi In seguito sono state sviluppate teorie più razionali per l’interpretazione degli acidi e delle basi 2

Teoria di Arrhenius (1880 -1890) 3 Acidi: Acidi elettroliti di tipo HX che in H 2 O dissociano in ioni H+ e X-. Soluzioni acquose di un acido contengono un eccesso di ioni H +. Sono acidi di Arrhenius: HCl, HNO 3, H 2 SO 4, CH 3 COOH… Basi: Basi elettroliti di tipo MOH che in H 2 O dissociano in ioni OH- e M+. Soluzioni acquose di una base contengono un eccesso di ioni OH -. Sono basi di Arrhenius: Na. OH, Al(OH) 3, Mg(OH)2…

Teoria di Arrhenius (1880 -1890) 4

Limiti della teoria di Arrhenius • Ione H+ è è un protone nudo e non può esistere come tale in soluzione acquosa • Non riesce a spiegare il comportamento acido di alcune sostanze che non contengono ioni H+ nella loro formula (e. g. CO 2 discolta in H 2 O) o quello basico di sostanze che non contengono gruppi OH (come l’ammoniaca NH 3) • E’ limitata alle soluzioni acquose (ma molte sostanze si comportano da acidi o basi anche in altri solventi) 5
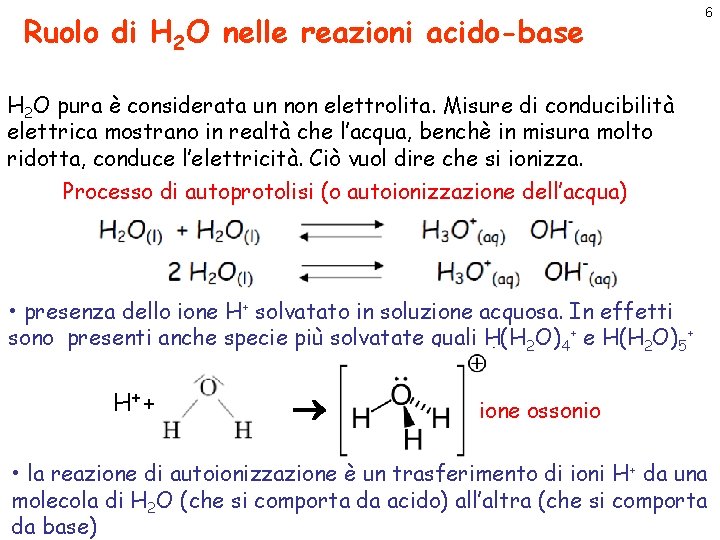
Ruolo di H 2 O nelle reazioni acido-base 6 H 2 O pura è considerata un non elettrolita. Misure di conducibilità elettrica mostrano in realtà che l’acqua, benchè in misura molto ridotta, conduce l’elettricità. Ciò vuol dire che si ionizza. Processo di autoprotolisi (o autoionizzazione dell’acqua) • presenza dello ione H+ solvatato in soluzione acquosa. In effetti sono presenti anche specie più solvatate quali H(H 2 O)4+ e H(H 2 O)5+ H+ + ione ossonio • la reazione di autoionizzazione è un trasferimento di ioni H + da una molecola di H 2 O (che si comporta da acido) all’altra (che si comporta da base)

Autoprotolisi dell’acqua Applichiamo la legge dell’azione di massa per ricavare la costante di equilibrio stechiometrica Kc costante di autoprotolisi o prodotto ionico dell’acqua Kw varia con la temperatura e siccome il processo è endotermico (perché G°>>0 e S° è piccolo) aumenterà all’aumentare di T 7
![8 [H]+ e [OH]- in acqua pura e p. H La scala di p. 8 [H]+ e [OH]- in acqua pura e p. H La scala di p.](http://slidetodoc.com/presentation_image_h/818a424a1963c78e5072003a243bb601/image-8.jpg)
8 [H]+ e [OH]- in acqua pura e p. H La scala di p. H è definito come il logaritmo decimale della concentrazione di ioni H 3 O+ cambiato di segno [H 3 O+] = 10 -p. H Se siamo a 25 °C in acqua pura p. H = -log[H 3 O+]=-log[10 -7] = 7. 00 Una soluzione acquosa che a 25 °C abbia un p. H = 7. 00 indica che [H 3 O+]=[OH-] e viene detta neutra

Logaritmi 9

Proprietà dei logaritmi 10

Definizione di acidità e basicità 11 Esempi calcolo p. H: La definizione di acidità e basicità può essere riformulata in termini di p. H dicendo che a 25 °C si ha:

p. OH Esempi: 12
![Scala di p. H e p. OH p. H = -log[H 3 O+] p. Scala di p. H e p. OH p. H = -log[H 3 O+] p.](http://slidetodoc.com/presentation_image_h/818a424a1963c78e5072003a243bb601/image-13.jpg)
Scala di p. H e p. OH p. H = -log[H 3 O+] p. OH = -log[OH-] 13
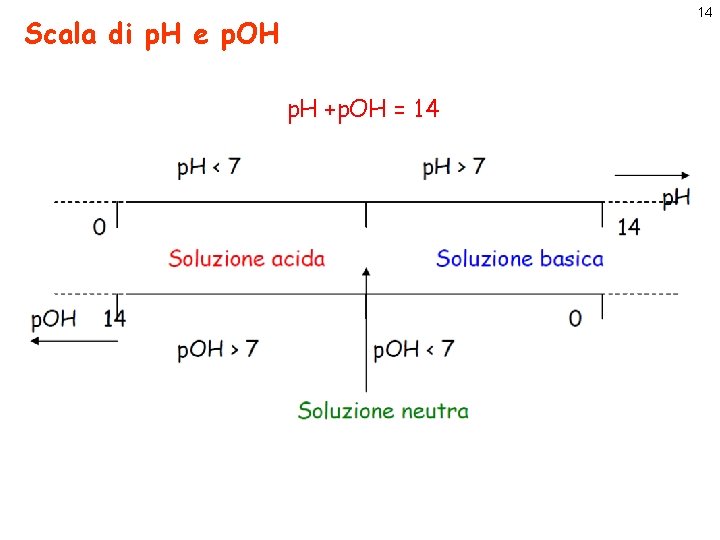
14 Scala di p. H e p. OH p. H +p. OH = 14
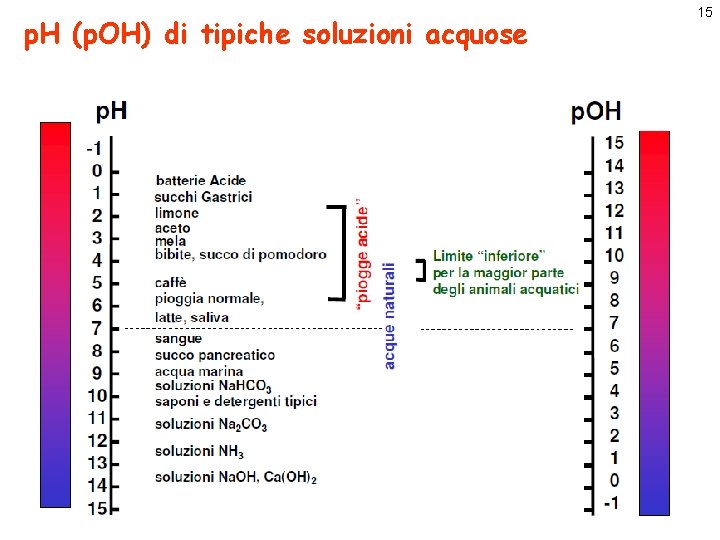
p. H (p. OH) di tipiche soluzioni acquose 15
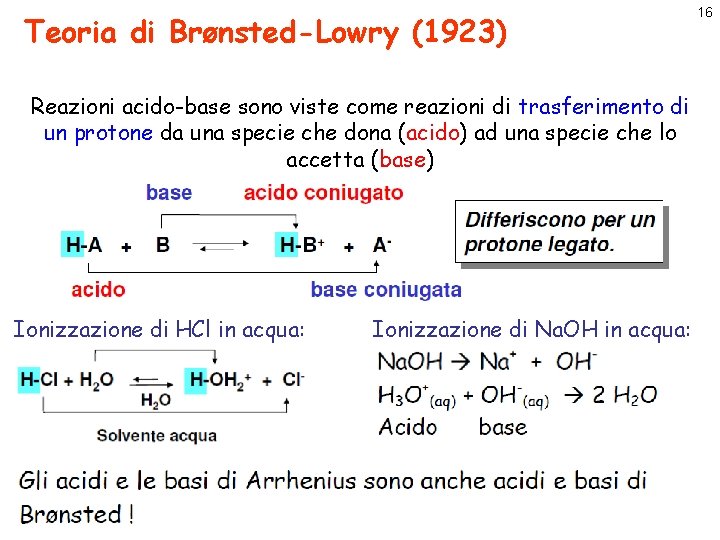
Teoria di Brønsted-Lowry (1923) Reazioni acido-base sono viste come reazioni di trasferimento di un protone da una specie che dona (acido) ad una specie che lo accetta (base) Ionizzazione di HCl in acqua: Ionizzazione di Na. OH in acqua: 16

Teoria di Brønsted-Lowry Ammoniaca: Ione idrogenocarbonato: 17
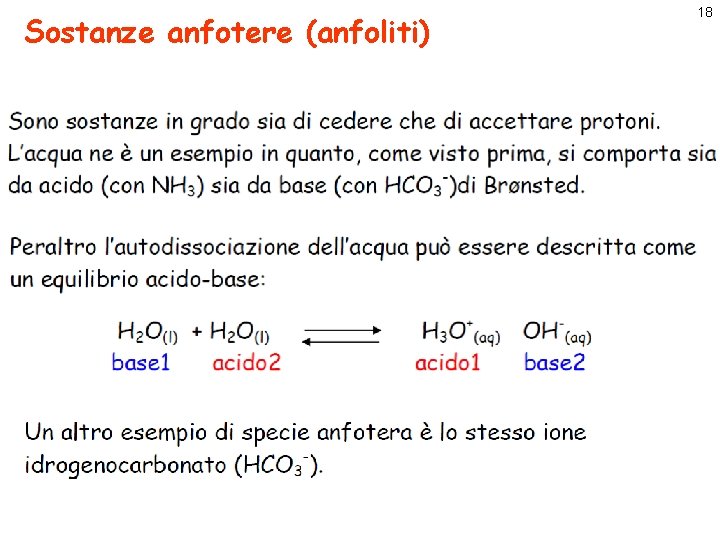
Sostanze anfotere (anfoliti) 18
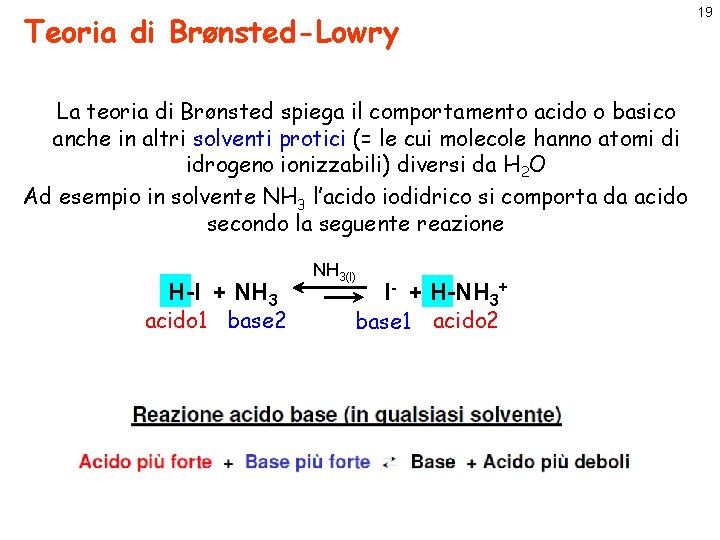
Teoria di Brønsted-Lowry La teoria di Brønsted spiega il comportamento acido o basico anche in altri solventi protici (= le cui molecole hanno atomi di idrogeno ionizzabili) diversi da H 2 O Ad esempio in solvente NH 3 l’acido iodidrico si comporta da acido secondo la seguente reazione H-I + NH 3 acido 1 base 2 NH 3(l) I- + H-NH 3+ base 1 acido 2 19
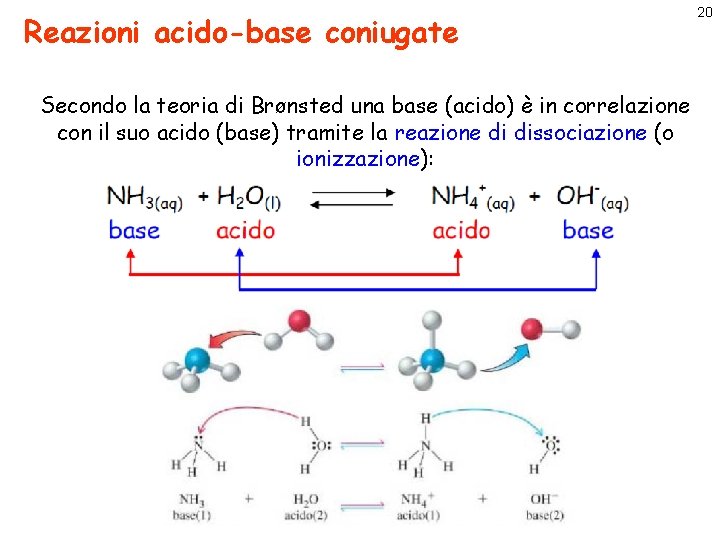
Reazioni acido-base coniugate Secondo la teoria di Brønsted una base (acido) è in correlazione con il suo acido (base) tramite la reazione di dissociazione (o ionizzazione): 20

Definizioni di Acido e Base 21

Acidi e basi di Lewis 22 Base di Lewis: specie in grado di donare una coppia elettronica solitaria Acido di Lewis: specie in grado di accettare una coppia elettronica solitaria NH 3 + BF 3 base NH 3 BF 3 acido Composti di elementi del III gruppo (B, Al) tendono ad essere forti acidi di Lewis perché l’interazione con la base permette di raggiungere l’ottetto (es. BF 3, Al. Cl 3) Atomi e ioni di elementi dei gruppi V, VI e VII hanno le coppie necessarie per comportarsi come basi di Lewis (es. NH 3, ma anche Cl-, F-, OH-, CN-, NO
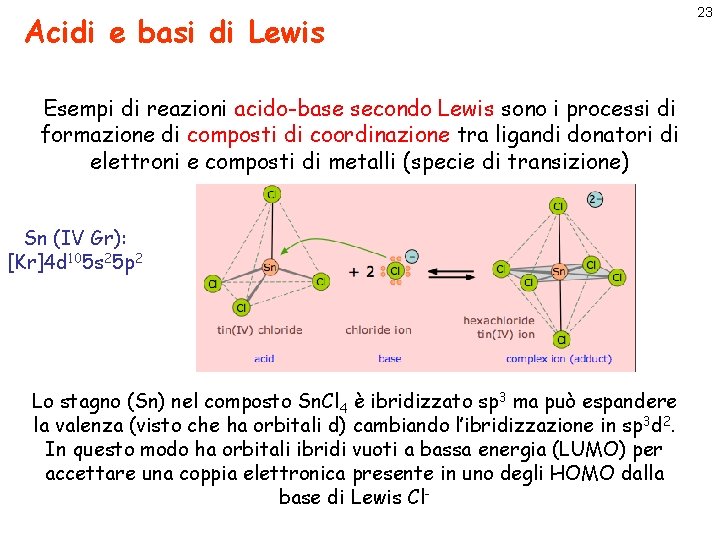
Acidi e basi di Lewis Esempi di reazioni acido-base secondo Lewis sono i processi di formazione di composti di coordinazione tra ligandi donatori di elettroni e composti di metalli (specie di transizione) Sn (IV Gr): [Kr]4 d 105 s 25 p 2 Lo stagno (Sn) nel composto Sn. Cl 4 è ibridizzato sp 3 ma può espandere la valenza (visto che ha orbitali d) cambiando l’ibridizzazione in sp 3 d 2. In questo modo ha orbitali ibridi vuoti a bassa energia (LUMO) per accettare una coppia elettronica presente in uno degli HOMO dalla base di Lewis Cl- 23

Costanti di dissociazione acida Per un generico acido HA in acqua possiamo scrivere la reazione di dissociazione: o più semplicemente: La costante di ionizzazione acida si può anche scrivere in forma logaritmica: [HA] p. Ka = p. H+log [A-] 24

Kw e Ka dell’acqua La Kw (costante di autoprotolisi dell’H 2 O in ambiente acquoso), è la costante relativa al seguente equilibrio: Kw = [H 3 O+][OH-] = 1. 00 x 10 -14 a 25 °C La Ka: costante di dissociazione acida dell’H 2 O (in un generico solvente protico) si scrive invece: H 2 O + S OH- + SH+ Ka = [SH+][OH-]/[H 2 O] in solvente acqua ( S=H 2 O): Ka = [H 3 O+][OH-]/[H 2 O] = 1. 00 x 10 -14/55. 5 ~ 10 -16 a 25 °C 25

Costanti di dissociazione basica Per una generica base B in acqua possiamo scrivere la reazione di dissociazione: La costante di ionizzazione basica si può anche scrivere in forma logaritmica: [B] p. Kb = p. OH+log [HB+] 26

Forza degli acidi e delle basi 27 Per forza di un acido (o di una base) si intende l’attitudine a cedere (o accettare) un protone all’H 2 O (o dall’H 2 O) in ambiente acquoso. La forza di un acido sarà tanto maggiore quanto più grande è il valore della sua Ka (o Kb) Esempi (acidi): L’acido acetico (CH 3 COOH) è più forte dell’acido cianidrico (HCN) perché ha una Ka più grande

Forza degli acidi e delle basi Esempi (basi): La metilammina è una base più forte dell’anilina perché ha una Kb più grande 28

Ka e p. Ka per alcuni acidi (deboli) 29 aumenta la forza dell’acido (libera più H+) Ka alta (105 – 100) acido forte Ka bassa (10 -2 – 10 -10) acido debole ovvero p. Ka bassa (anche negativa) ovvero p. Ka alta
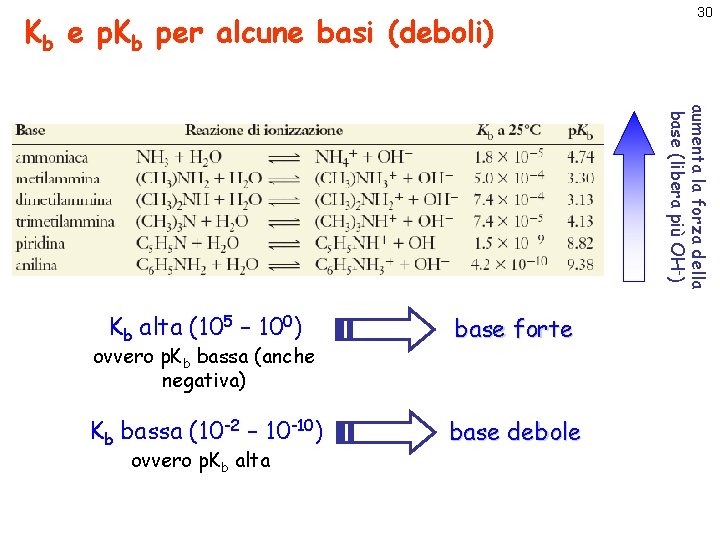
Kb e p. Kb per alcune basi (deboli) 30 aumenta la forza della base (libera più OH-) Kb alta (105 – 100) base forte Kb bassa (10 -2 – 10 -10) base debole ovvero p. Kb bassa (anche negativa) ovvero p. Kb alta

Relazione tra le costanti di dissociazione di un 31 acido e della sua base coniugata Considero la coppia base/acido coniugata NH 3/NH 4+: basica acida Sommando le reazioni (1) e (2) si ottiene l’ autoionizzazione di H 2 O:

Relazione tra le costanti di dissociazione di un 32 acido e della sua base coniugata Per qualsiasi coppia coniugata acido-base, a 25 °C: Ka Kb = Kw = 1. 00 10 -14 Esempi: p. Ka + p. Kb = p. Kw = 14 Coppia NH 3/NH 4+: Kb=1. 8 10 -5 quindi p. Kb=4. 74 e p. Ka=14. 00 -4. 74=9. 26 Coppia CH 3 COOH/CH 3 COO-: Ka=1. 8 10 -5 quindi p. Ka=4. 74 e p. Kb=14. 00 -4. 74=9. 26 Coppia HIO/IO-: Ka=2. 24 10 -11 quindi p. Ka=10. 65 e p. Kb=14 -10. 65=3. 35 Lo ione ammonio (NH 4+) è un acido debole (p. Ka=9. 26). E’ più debole di CH 3 COOH (p. Ka=4. 74) ma è più forte dell’acido ipoiodoso HIO (p. Ka=10. 65) In generale tanto più forte è un acido, tanto più debole è la sua base coniugata
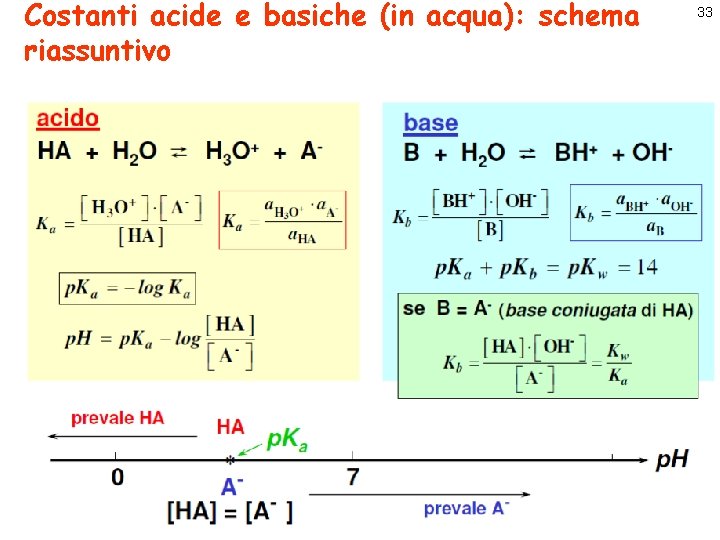
Costanti acide e basiche (in acqua): schema riassuntivo 33

Calcoli sul p. H di acidi e basi in acqua Acidi forti 34 Un acido forte in H 2 O è completamente dissociato. Equil. di dissociazione è completamente spostato a destra e la relativa K di dissociazione è >> 1 HCl. O 4 acido perclorico Acidi forti HNO 3 acido nitrico (in H 2 O) sono: H 2 SO 4 acido solforico HI HBr HCl acido iodidrico acido bromidrico acido cloridrico La [H 3 O+] per soluzioni di acidi forti sarà uguale a: Infatti l’equilibrio di autodissociazione di H 2 O è sempre presente: Se [H 3 O+]HA>> [H 3 O+]H 2 O 10 -7 il contributo derivante dall’autoprotolisi può essere trascurato [H 3 O+]tot = [H 3 O+]HA

Calcoli sul p. H di acidi e basi in acqua Acidi forti Per acidi forti non molto diluiti, vale a dire la cui C a=[HA]0 10 -6 il contributo dell’acqua può essere trascurato e si avrà 35

Calcoli sul p. H di acidi e basi in acqua Basi forti Per le basi forti valgono gli stessi ragionamenti fatti prima, Na. OH idrossido di Na Basi forti KOH idrossido di K (in H 2 O) sono: Ba(OH)2 idrossido di Ba Sr(OH)2 idrossido di Sr Ca(OH)2 idrossido di Ca Na 2 O ossido di Na Ca. O ossido di calcio La [OH-] per soluzioni di basi forti sarà uguale a: Se [OH-]B>> [OH-]H 2 O 10 -7 il contributo derivante dall’autoprotolisi può essere trascurato [OH-]tot = [OH-]B Per basi forti non molto diluite, vale a dire la cui C b=[B]0 10 -6 il contributo dell’acqua può essere trascurato e si avrà 36

Calcoli sul p. H di acidi e basi in acqua Basi forti 37

Calcoli sul p. H di acidi e basi in acqua Acidi deboli Gli acidi deboli sono solo parzialmente dissociati, e l’equilibrio di dissociazione è solo parzialmente spostato a destra (Ka< 1) Se la soluzione dell’acido è abbastanza concentrata il contributo derivante dall’autoionizzazione dell’acqua può essere trascurato: 38

Calcoli sul p. H di acidi e basi in acqua Acidi deboli 39

Calcoli sul p. H di acidi e basi in acqua Acidi deboli -1/2 log(Ca) L’approssimazione è valida quando 40

41 Calcoli sul p. H di acidi e basi in acqua Acidi deboli: esempio numerico Calcolare le concentrazioni di HA, H+ e A- e il p. H di una soluzione C 0 = 0. 1 M di un acido debole con Ka=1. 4 10 -5 Facciamo l’approssimazione: cont.

Calcoli sul p. H di acidi e basi in acqua Acidi deboli 42

Calcoli sul p. H di acidi e basi in acqua Grado di ionizzazione Il grado di ionizzazione di un acido (o base) è il rapporto tra la concentrazione di acido (base) che è ionizzato all’equilibrio e la concentrazione totale di acido presente inizialmente. Moltiplicato per 100 corrisponde alla percentuale di acido (base) ionizzata all’equilibrio. [A-] 1. 2 10 -3 [A-] -2 grado di ionizzazione= = 1. 2 10 = = C 0 0. 1 [HA]+[A-] % di ionizzazione = 1. 2 10 -2 100 = 1. 2% 43

Calcoli sul p. H di acidi e basi in acqua Basi deboli Per le basi deboli si applicano gli stessi ragionamenti visti sopra per gli acidi deboli Siccome p. H = 14 – p. OH si può scrivere: 44

45 Calcoli sul p. H di acidi e basi in acqua Base debole: esempio numerico Calcolare le concentrazioni di tutte le specie e il p. H di una soluzione C 0 = 0. 1 M di metilammina, base debole con Kb=4. 3 10 -4 cont.

Calcoli sul p. H di acidi e basi in acqua 46 Base debole cont.

Calcoli sul p. H di acidi e basi in acqua 47 Base debole cont.

Calcoli sul p. H di acidi e basi in acqua Base debole 48

Esercizio: base debole 49 Problema: Il p. H di una soluzione di NH 3 per usi domestici è di 11. 5. Calcolare la sua molarità (concentrazione analitica) sapendo che Kb(NH 3)=1. 8 x 10 -5 Soluzione: p. H+p. OH=14 quindi p. OH=14 -11. 5=2. 5 quindi [OH-]=10 -2. 5=3. 2 x 10 -3 M Scriviamo l’equilibrio acido-base coinvolto: 1 conc. iniz. variazione conc. equlibrio NH 3(aq) + H 2 O NH 4+(aq) x 0 OH-(aq) ~0 -3. 2 x 10 -3 +3. 2 x 10 -3 x-3. 2 x 10 -3 +3. 2 x 10 -3 Sostituiamo i valori delle conc. all’equilibrio nella K b: Kb= + [NH 4+][OH-] [NH 3] = (3. 2 x 10 -3) x-3. 2 x 10 -3 Risolviamo rispetto a x ed abbiamo x= 0. 57 M = 1. 8 x 10 -5 2 1

Grado di dissociazione e dipendenza dal p. H 50 Acido debole concentrazione analitica C 0: Il grado di dissociazione: x= [A-] [HA]+[A-] Posso esprimere Ka in funzione di x e [H 3 O+]: K a= da cui si ha: Ka(1 -x) = x[H 3 O+] x = In ambiente acido: [H 3 O+] >> Ka si ha che x Ka [H 3 O+] = 0 [A-] C 0 x. C 0[H 3 O+] C 0(1 -x) Ka [A-] = x C 0 [HA] = C 0 -[A-]=C 0(1 -x) = x[H 3 O+] (1 -x) [H 3 O+] + Ka quindi: [A-] 0 [HA] C 0 In ambiente acido l’acido debole è praticamente indissociato (equilibrio di dissociazione spostato verso sin. per via della presenza di una elevata [H 3 O+]
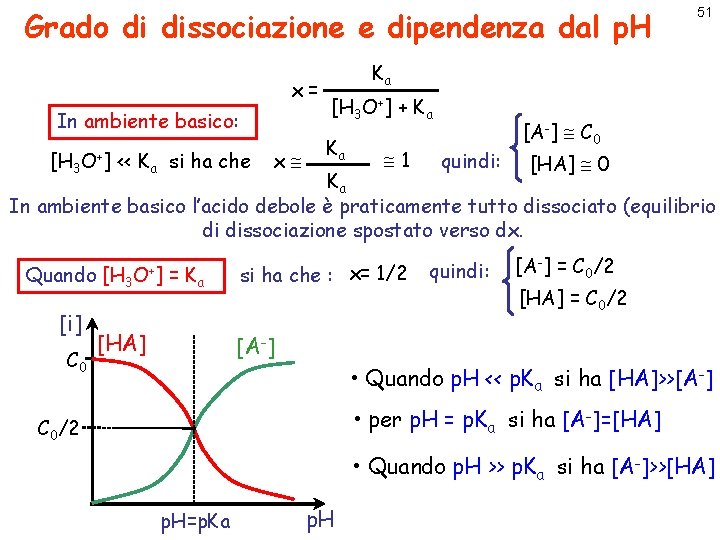
Grado di dissociazione e dipendenza dal p. H x= In ambiente basico: [H 3 O+] << Ka si ha che x 51 Ka [H 3 O+] + Ka Ka 1 quindi: [A-] C 0 [HA] 0 Ka In ambiente basico l’acido debole è praticamente tutto dissociato (equilibrio di dissociazione spostato verso dx. Quando [i] C 0 [H 3 O+] = Ka [HA] si ha che : x= 1/2 quindi: [A-] = C 0/2 [HA] = C 0/2 [A-] • Quando p. H << p. Ka si ha [HA]>>[A-] • per p. H = p. Ka si ha [A-]=[HA] C 0/2 • Quando p. H >> p. Ka si ha [A-]>>[HA] p. H=p. Ka p. H

Acidi poliprotici 52 Ka >> 1

Acidi poliprotici 53

Acidi poliprotici 54

Acidi poliprotici 55

Acidi poliprotici 56

Acidi poliprotici: acido fosforico p. Ka 1=2. 16 p. Ka 2=7. 21 a 3 p. Ka 3=12. 32 NOTA: il valore delle Ka successive diminuisce al crescere del numero di protoni ceduti dall’acido 57
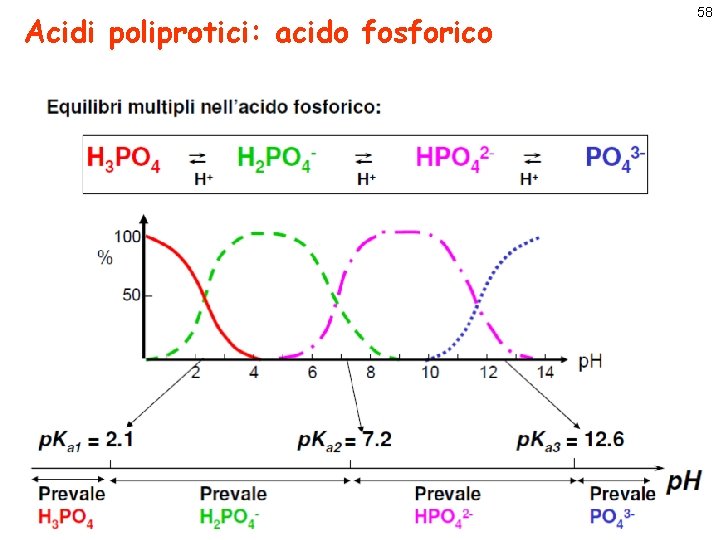
Acidi poliprotici: acido fosforico 58
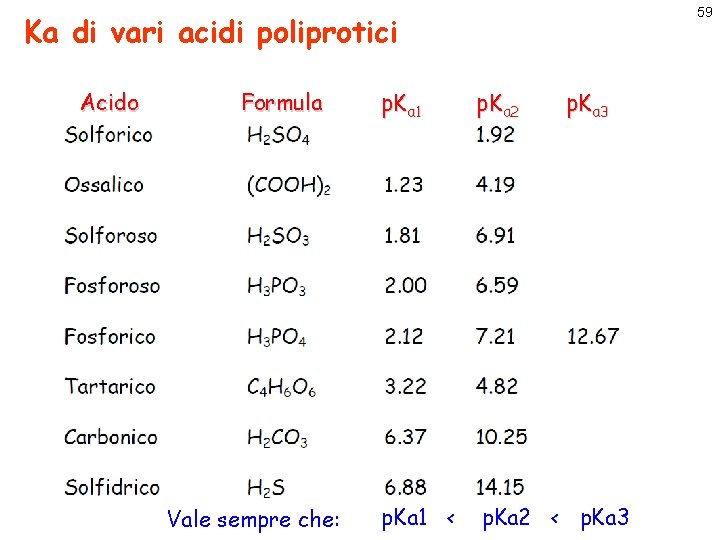
59 Ka di vari acidi poliprotici Acido Formula Vale sempre che: p. Ka 1 p. Ka 2 p. Ka 3 p. Ka 1 < p. Ka 2 < p. Ka 3

Soluzione rigorosa di problemi di equilibri multipli 60 Dobbiamo determinare i valori delle concentrazioni all’equilibrio di cinque specie : [H+], [OH-], [H 2 CO 3], [HCO 3 -], [CO 32 -] Ma abbiamo cinque equazioni: (aq) 2 H 2 O(l) (aq) H 3 O+(aq) + OH-(aq) Ka 1 Ka 2 Kw = [H 3 O+] [OH-] C 0= [H 2 CO 3] + [HCO 3 -] + [CO 32 -] bilancio di massa [H+] = [HCO 3 -] + [CO 32 -] +[OH-] bilancio di carica Quindi il problema ha una soluzione univoca, anche se matematicamente complessa (risoluzione di un sistema di 5 eq. in 5 incognite). Per questo quando possibile si ricorre ad approssimazioni che abbiano un senso chimico (es. trascurare le conc. di specie quando sono << rispetto ad altre)
- Slides: 60