1 Elektrine osobine atoma i molekula uslovljavaju pojavu

1

Električne osobine atoma i molekula uslovljavaju: Øpojavu dvojnog prelamanja svetlosti Øpojavu polarizacije rasejane svetlosti Ødijelektrične osobine Ømeđumolekulske interakcije Øpravila izbora u spektroskopiji Objašnjavaju se korišćenjem jednostavnih atomskih i molekulskih modela 2

Polarizacija molekula • Nepolarni molekuli-centri + i – naelektrisanja se podudaraju • Polarni molekuli centri + i – naelektrisanja na izvesnom rastojanju tako da formiraju dipolni momenat • Dejstvo električnog polja izaziva: – kod nepolarnih molekula razdvajanje + i – centara naelektrisanja i indukovanje dipola koji se orijentišu pod dejstvom polja. Jezgra su suviše teška tako da dolazi do distorzije elektronskog oblaka Distorted cloudoblaka Distorzija electron elektronskog 3
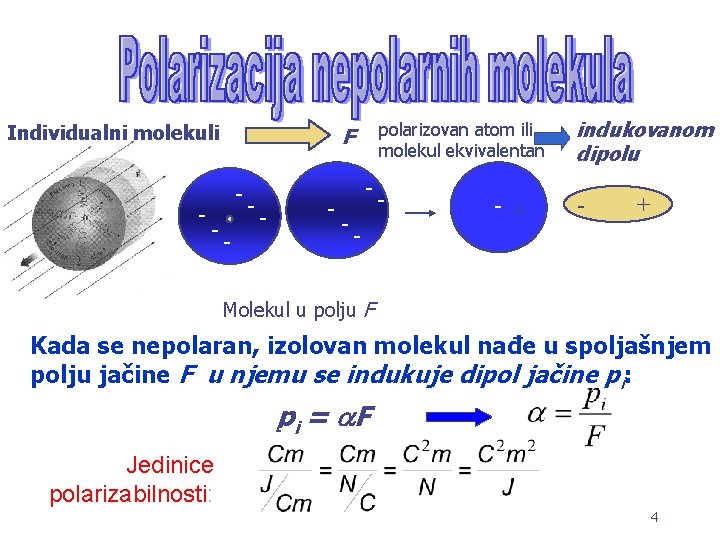
Individualni molekuli - - polarizovan atom ili molekul ekvivalentan F - -- - - + indukovanom dipolu - + Molekul u polju F Kada se nepolaran, izolovan molekul nađe u spoljašnjem polju jačine F u njemu se indukuje dipol jačine pi: Jedinice polarizabilnosti: - p - i = F - - -- 4

Polarizabilnost Da bi se pojednostavila jedinica C 2 m 2 J-1 za definiše se zapreminska polarizabilnost ’ kao: koja ima jedinicu zapremine m 3 a veličinu koja odgovara veličini molekula o=8, 854∙ 10 -12 F/m 5

Polarizabilnost = sposobnost tela da dobije dipolni momenat kada je izložen dejstvu električnog polja Polje duž z-ose može idukovati dipol sa komponentama u pravcu x i y osa Kod neizotropnih sredina polarizabilnost zavisi od pravca dejstva polja Srednja polazibilnost 6

Polarizabilnost-deformativnost: za veće jačine polja Koristeći Tejlorov red da bismo dobili izraz za energiju tela u polju koristeći da je: možemo pisati: p 0 z: permanentni dipolni momenat zz: polarizabilnost zz: hiperpolarizabilnost 7

Polarizabilnost Da bi se izračunala polarizabilnost molekula koristi se perturbaciona teorija kojom se dobija: p je fluktuacija dipolnog momenta, E srednja vrednost energija pobuđivanja. 8

Zavisnost polariozabilnosti od veličine Polarizabilnost raste sa veličinom molekula. Za atom sa jednim elektronom p = -er tako da je: Pretpostavljajući da je potencijal jonizacije I potencijalna energija elektrona na rastojanju Ra od jezgra, polarizabilnost je: Ovaj izraz pokazuje da polarizabilnost raste sa veličinom molekula i lakoćom da se molekul pobudi odn. jonizuje. Odavde se vidi i da je zapremiska polarizabilnost reda zapremine molekula 9

Još o polarizabilnosti Polarizabilnost zavisi od kvadrata dipolnog momenta prelaza ali na isti način zavisi i apsorpcija fotona. Veliki doprinost polarizabinosti potiče od nisko energetskih, intenzivnih prelaza. Mali je udeo visokoenergetskih prelaza. Ovo znači da su intenzivno obojeni molekuli veoma polarizabilni. Polarizabilnost takođe veoma raste sa brojem valentnih elektrona. 10

Elektronska polarizabilnost Najmanja He 0. 20 H 2 O 1. 45 O 2 1. 60 CO 1. 95 (4 o)10 -30 m 3 NH 3 2. 3 =1. 11 x 10 -40 C 2 m 2 J-1 CO 2 2. 6 Xe 4. 0 CHCl 3 8. 2 CCl 4 10. 5 jedinice: Najveća 11

Zapreminska polarizabilnost 0 = 8, 854 10 12 Fm 1 permitivnost vakuuma Jedinice ’: Električni dipolni momenti p i zapreminske polarizabilnosti ’ različitih supstancija Supstancija He H 2 N 2 HCl NH 3 H 2 O CH 4 CH 3 Cl CH 2 Cl 2 CHCl 3 CCl 4 p/(D) 0 0 0 1, 08 1, 47 1, 85 0 1, 01 1, 57 1, 01 0 ’/(10 24 cm 3) 0, 20 0, 82 1, 77 2, 63 2, 22 1, 48 2, 60 4, 53 6, 80 8, 50 10, 5 12

Relativna permitivnost Kada su naelektrisanja q 1 i q 2 na rastojanju r u vakuumu potencijalna energija njihove interakcije je: Kada su ista naelektrisanja uronjena u neku sredinu (kao npr. vazduh ili tečnost), njihova potencijalna energija se smanjuje: gde je permitivnost sredine 13

Relativna permitivnost Permitivnost se obično izražava kao relativna permitivnost r (ranije dijeleketrična konstanta) sredine: gde je 0 = 8, 854 10 12 Fm 1 permitivnost vakuuma Relativna permitivnost supstancije se meri poređenjem kapaciteta kondenzatora sa i bez date sredine: 14

Relativna permitivnost • Primer: Kolika je permitivnost kamfora ako je kapacitet kondenzatora u vakuumu 5, 01 p. F (1 F=1 C/V), a u kamforu je 57, 1 p. F: • Relativna permitivnost supstancije je bezdimenziona veličina, koja ima značajan uticaj na interakciju između jona u rastvoru. Tako npr. voda ima r=78 na 25 o. C pa se energija Kulonove interakcije smanjuje za blizu dva reda veličine u vodi u odnosu na vrednost u vakuumu. • Relativna permitivnost supstancije je velika ako su njeni molekuli polarni i visoko polarizabilni. 15
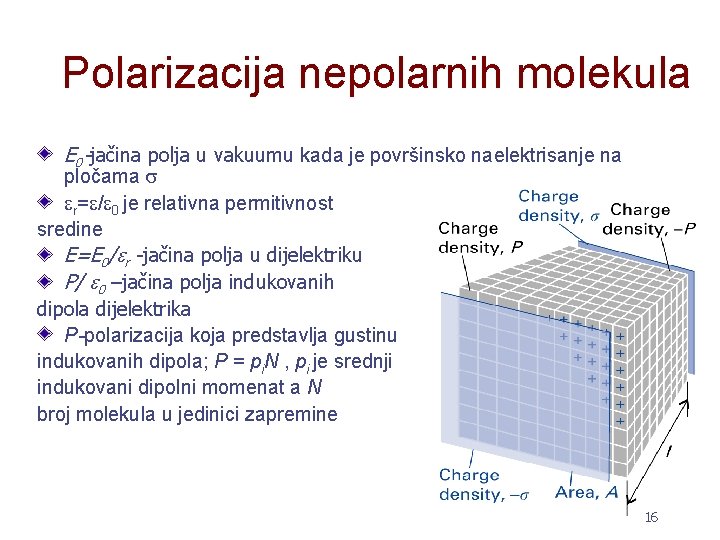
Polarizacija nepolarnih molekula E 0 -jačina polja u vakuumu kada je površinsko naelektrisanje na pločama r= / 0 je relativna permitivnost sredine E=E 0/ r -jačina polja u dijelektriku P/ 0 –jačina polja indukovanih dipola dijelektrika P-polarizacija koja predstavlja gustinu indukovanih dipola; P = pi. N , pi je srednji indukovani dipolni momenat a N broj molekula u jedinici zapremine 16
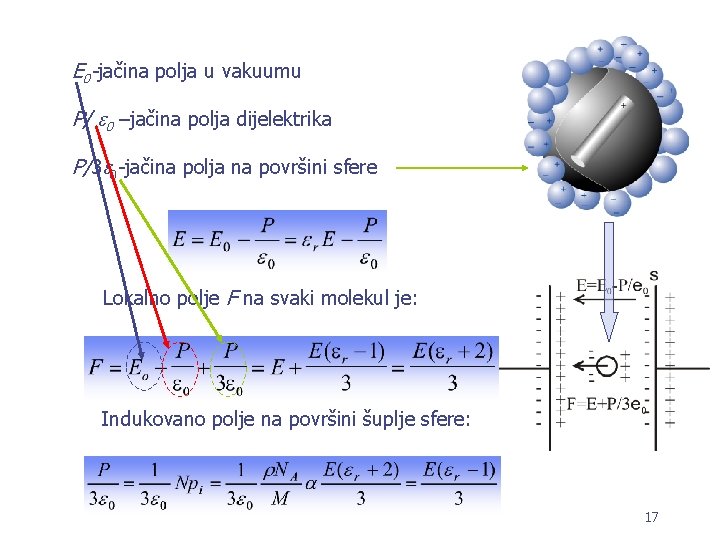
E 0 -jačina polja u vakuumu P/ 0 –jačina polja dijelektrika P/3 0 -jačina polja na površini sfere Lokalno polje F na svaki molekul je: Indukovano polje na površini šuplje sfere: 17

• Pm je molarna polarizacija nepolarne sredine • Ima dimenzije molarne zapremine • Naziva se indukovanom ili distorzionom polarizacijom PD r 1 = e, je električna susceptibilnost i uvek je pozitivna Polazeći od Maksvelove elektromagnetske teorije: n 2= r 18

Indukovana-distorziona polarizacija Iz indeksa prelamanja primenom vidljive svetlosti 19

Indukovani dipol idealno provodne sfere radijusa r u polju jačine F je: pi=r 3 F a ’=r 3 je polarizabilnost takvog molekula Stoga je molarna polarizacija odn. refrakcija kao makroskopska veličina povezana sa poluprečnikom molekula kao miksroskopskom veličinom: Merenja indeksa prelamanja omogućavaju određivanje molarne polaruzacije Pm, kao i polarizabilnosti i ’ kao i poluprečnika molekula kako kod nepolarnih tako i polarnih supstancija (jer i one imaju određenu polarizabilnost pored dipolnog momenta). Ali ako se polarizacija određuje iz merenja dijelektrične konstante onda se poluprečnik molekula može odrediti samo ya nepolarne 20 molekule za koje važi Maksvelova relacija.

Priroda svetlosti Svetlost je elektromagnetski talas: n Mnoge električne i optičke osobine materije, podaci o vezivanjima, sastavu i dr. dobijaju se na osnovu spektroskopije tj. interakcije elektromagnetskog zračenja sa materijom sa brzinom od c = 1/ ( 0 0) = 3 x 108 m/s Električna komponenta elektromagnetskog talasa interaguje elektrostatički sa elektronima atoma i molekula sredine kroz koju zračenje odn. svetlost prolaze 21

Polarizacija i refrakcija Gornja jednakost važi kada: §su molekuli nepolarni §kada se indeks prelamanja meri svetlošću velikog ªUsled interakcije električne komponente elektromagnetskog zračenja sa molekulima sredine, dolazi do polarizacije sredine i brzina svetlosti se menja usled čega se svetlost prelama. ªUkoliko je interakcija intenzivnija utoliko brzina prostiranja je manja a indeks prelamanja veći. ªInterakcija je intenzivnija što su fotoni veće frekvencije tj. veće energije 22

Polarizacija i refrakcija ªZavisnost indeksa prelamanja od frekvencije je disperzija refrakcije ªDa bi došlo do deformacije jezgara tj, uvijanja ili istezanja veza u molekulu potrebna su polja manjih frekvencija odnosno većih talasnih dužina kada identičnost između polarizacije i refrakcije važi. Pošto se elektronska polarizacija meri preko indeksa prelamanja određenog vidljivom svetlošću, to se refrakcije veza i elektronskih grupa izražavaju iz ekvivalenata refrakcije: 23

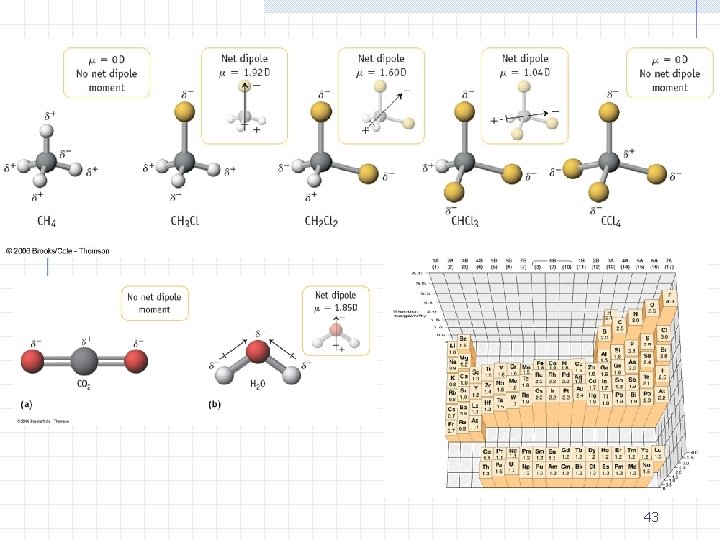
Polarizacija polarnih molekula Polaran Nepolaran Polaran ü Polarni molekuli su oni koji zbog svog sastava i geometrije imaju nesimetričnu raspodelu naelektrisanja ü Polarni molekuli poseduju permanentni dipolni momenat p ü Van polja zbog haotične raspodele ovih dipola nema doprinosa ovih dipola ukupnoj polarizaciji ü U spoljašnjem polju ovi dipoli orijenatcionom polarizacijom (PO ) doprinose ukupnoj polarizaciji u zavisnosti od veličine p, jačine polja i temperature 24

Dipolni momenti Polarnost molekula se izražava njegovim dipolnim momentom p: -q r +q gde su +q i –q naelektrisanja razdvojena rastojanjem . Tipično, q je naelektrisanje elektrona: 1, 602 x 10 -19 C a veličina je reda 1Å= 10 -10 m, dajući p = 1, 602 x 10 -29 Cm. “Konvencionalna” jedinica za dipolni momenat je debaj: 1 D = 3. 336 x 10 -30 Cm 25
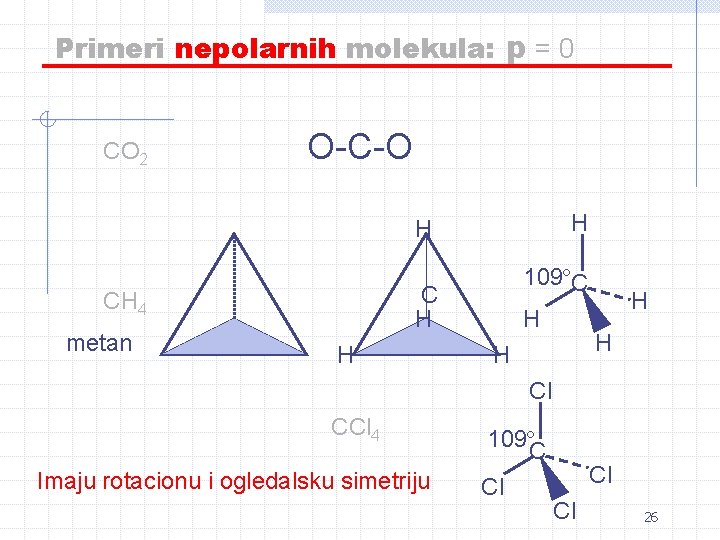
Primeri nepolarnih molekula: p = 0 CO 2 O-C-O H H CH 4 metan 109ºC H H H Cl CCl 4 Imaju rotacionu i ogledalsku simetriju 109º C Cl Cl Cl 26
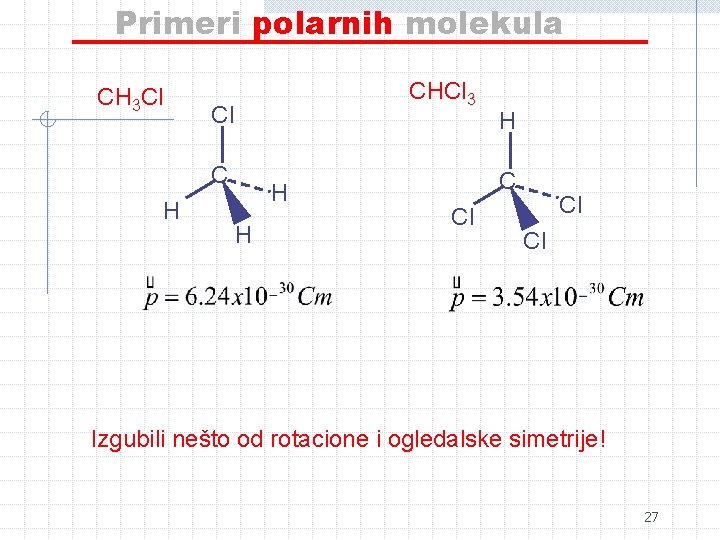
Primeri polarnih molekula CH 3 Cl CHCl 3 Cl C H H C Cl Cl Cl Izgubili nešto od rotacione i ogledalske simetrije! 27

Polarizacija polarnih molekula Spoljašnje polje može delimično orijentisati dipole: + F - Spoljašnje električno polje teži da orijentiše polarne molekule doprinoseći ukupnoj polarizaciji sredine orijentacionom polarizacijom. Energija dipola p u električnom polju jačine F je: U( )=-p. Fcos gde je ugao između pravca dipola i pravca polja. 28

Deo od ukupnog broja molekula čije ose dipola zaklapaju uglove između i +d a koji su obuhvaćeni prostornim uglom d je: d. N=Ad =A 2 sin d Kada se uključi polje jačine F, deo molekula d. N koji se orijentiše u pravcu polja u meri u kojoj dozvoljava srednja energija termalnog kretanja k. T, dobija se množenjem d. N sa Bolcmanovim faktorom: d. NF = A e-U/k. T d = A ep. Fcos /k. Td. w. Ukupan broj molekula čija orijentacija u spoljašnjem polju doprinosi polarizaciji sredine dobija se integracijom d. NF po čitavom prostornom uglu tj. za sve moguće orijentacije dipolnih momenata unutar sfere: 29

Da bi se odredio srednji moment kojim pojedini polarni molekuli doprinose ukupnoj polarizaciji sredine, potrebno je odrediti sumu svih momenata u pravcu polja i podeliti je ukupnim brojem molekula. Pošto polarizaciji doprinose samo komponente dipolnog momenta u pravcu polja, to će ukupni moment kojim molekuli unutar prostornog ugla d deluju u prisustvu polja jačine F biti: d. NF p cos = A ep. Fcos /k. T p cos d dok će ukupna suma momenata u čitavom prostornom uglu : tako da srednji momenat kojim polarni molekuli doprinose polarizaciji pri dejstvu polja jačine F i pri temperaturi T je: 30
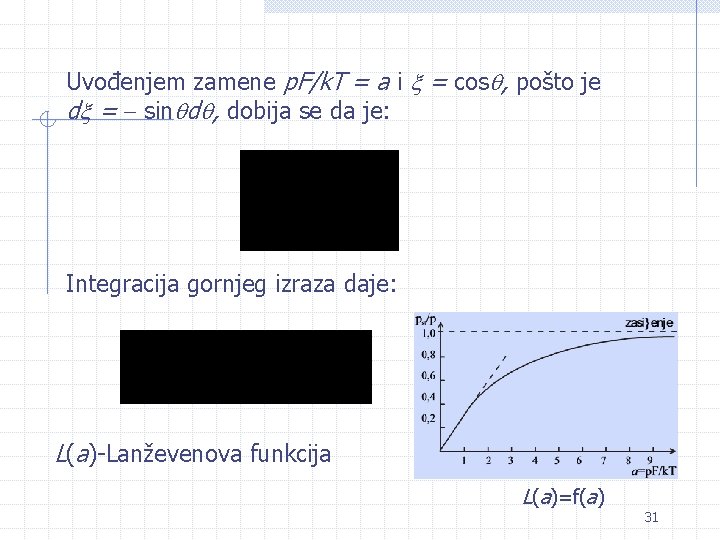
Uvođenjem zamene p. F/k. T = a i = cos , pošto je d = sin d , dobija se da je: Integracija gornjeg izraza daje: L(a)-Lanževenova funkcija L(a)=f(a) 31
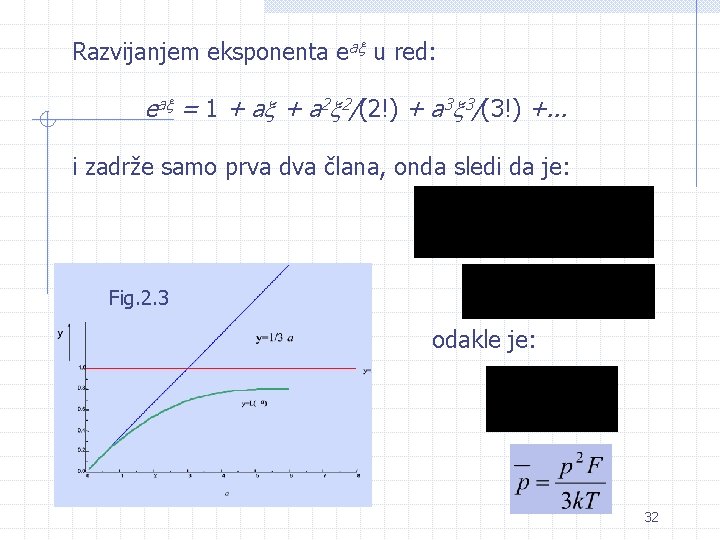
Razvijanjem eksponenta ea u red: ea = 1 + a 2 2/(2!) + a 3 3/(3!) +. . . i zadrže samo prva dva člana, onda sledi da je: Fig. 2. 3 odakle je: 32

Ukupni električni dipolni momenat usled indukcije i usled sopstvenih permanentnih dipola je: pi+ =F( +p 2/3 k. T) a ukupna polarizacija je: Pm = PD+PO = Debajeva jednačina a = N A / 3 0 odsečak prave Pm=f(1/T) p za 1/T 0 b = N A p 2 / 9 0 k nagib prave Pm=f(1/T) = 4, 27 10 32 (b)1/2 C m 33

Debajeva jednačina je bila prvi izraz koji je povezao molekulski parametar – dipolni momenat ispitivane supstancije sa fenomenološkim (makroskopskim) parametrom koji se može eksperimentalno meriti-sa električnom permitivnosti. Koristeći molarnu polarizaciju [P] , definisanu kao: možemo pisati Debye-evu jednačinu za čistu supstanciju kao: Stoga prema Debye-evoj jednačini, molarna polarizacija supstancije na datoj temperaturi je konstantna. Ona je nezavisna od pritiska i ista joj je vrednost u gasovitom i tečnom stanju. 34

Određivanje dipolnih momenata q. Grafički iz merenja polarizacije u funkciji od temperature: Pm se određuje merenjem permitivnosti q. Merenjem ukupne polarizacije iz permitivnosti i distorzione polarizacije iz indeksa prelamanja na jednoj temperaturi: 35
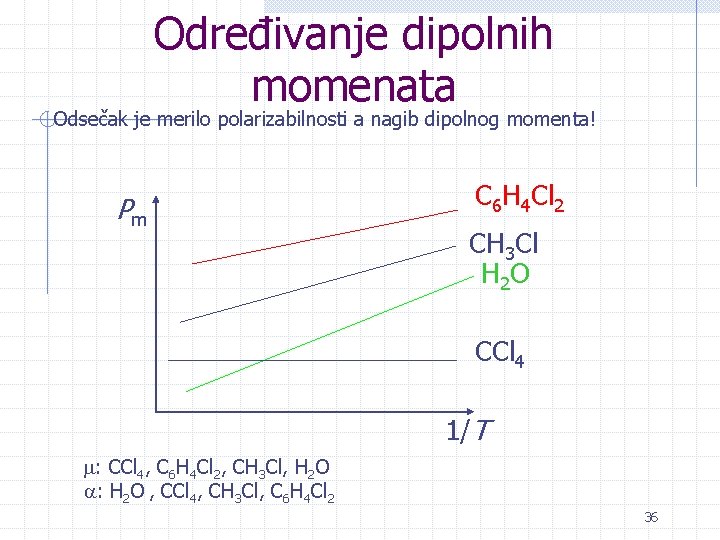
Određivanje dipolnih momenata Odsečak je merilo polarizabilnosti a nagib dipolnog momenta! Pm C 6 H 4 Cl 2 CH 3 Cl H 2 O CCl 4 1/T : CCl 4, C 6 H 4 Cl 2, CH 3 Cl, H 2 O : H 2 O , CCl 4, CH 3 Cl, C 6 H 4 Cl 2 36

Određivanje dipolnih momenata izračunava se q. Metodom razblaženja: P 1, 2 = x 1 P 1 + x 2 P 2 -P 1 polarizacija nepolarnog rastvarača molskog udela x 1 -P 2 polarizacija polarne rastvorene supstancije molskog udela x 2 q. Ukupna polarizacija rastvora je takođe: iz permitivnosti q. Mere se polarizacije rastvora različitih sastava i polarizacija nepolarnog rastvarača iz permitivnosti dok se polarizacija polarne supstancije izračunava. Da bi se izvegao uticaj rastvarača crta se zavisnost P 2 u funkciji x 2 i P 2 određuje pri beskonačnom razblaženju kada x 2 0 37

Jedna od savremenijim metoda merenja dipolnih momenata se zasniva na merenju mikrotalasnih i radiofrekventnih spektara koji obično predstavljaju rotacione (ređe rotaciono - vibracione) spektre. 38

Dipolni momenti veza i molekula Pošto dipolni momenti nastaju usled razlike u elektronegativnosti atoma vezanih hemijskom vezom, to je moguće svakoj vezi pripisati određeni dipolni momenat. Ukupni momenat molekula se može odrediti kao vektorska suma momenata pojedinih veza Veza H O H N H C C Cl C O C=O C N p/(D) 1, 5 1, 3 0, 4 1, 5 0, 8 2, 5 0, 5 39
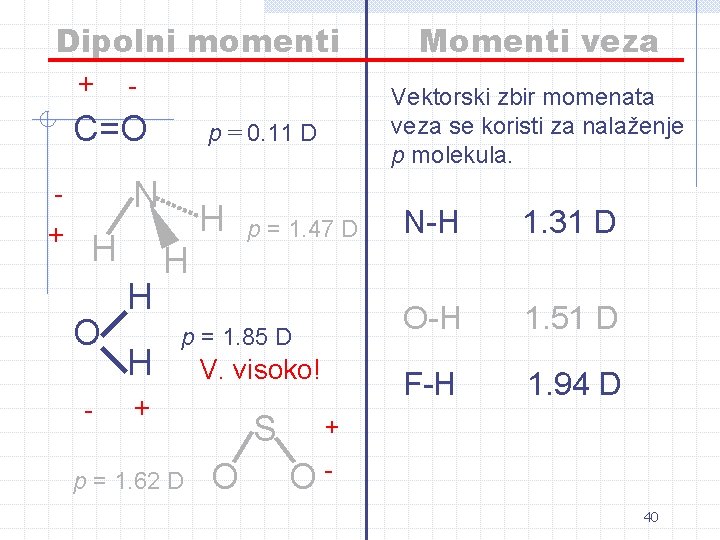
Dipolni momenti + - C=O p = 0. 11 D N + H O - H H p = 1. 47 D p = 1. 85 D + p = 1. 62 D V. visoko! Momenti veza Vektorski zbir momenata veza se koristi za nalaženje p molekula. N-H 1. 31 D O-H 1. 51 D F-H 1. 94 D S + O O 40
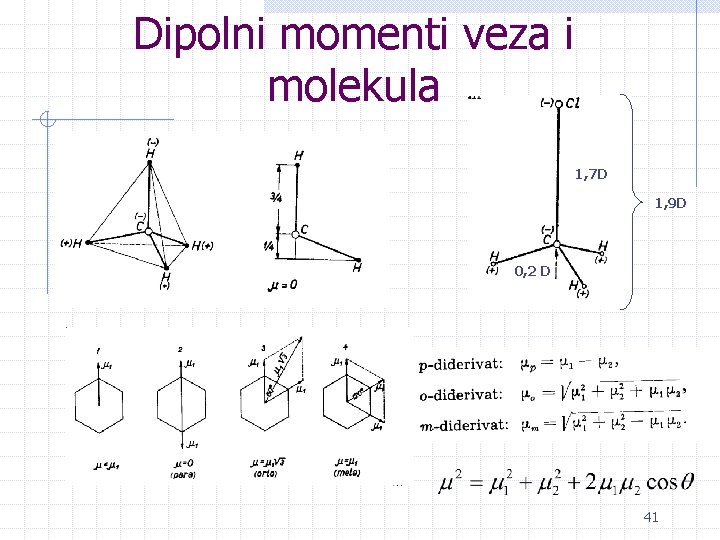
Dipolni momenti veza i molekula 1, 7 D 1, 9 D 0, 2 D 41

Zavisnost polarizacije od frekvencije 42
43
- Slides: 43