1 COURS DE THERMODYNAMIQUE Module Ph 21 13092021













































- Slides: 53

1 COURS DE THERMODYNAMIQUE (Module Ph 21) 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 1

1 Chapitre un Introduction à la thermodynamique 1. 1 Historique 1. 2 Introduction à la Thermodynamique 1. 3 Notion de température 1. 4 Notion de chaleur 1. 5 Vocabulaire thermodynamique 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 1 2

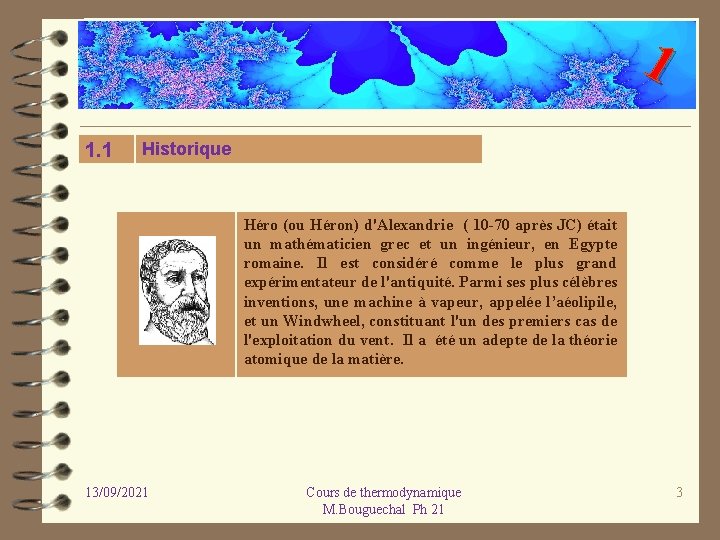
1 1. 1 Historique Héro (ou Héron) d'Alexandrie ( 10 70 après JC) était un mathématicien grec et un ingénieur, en Egypte romaine. Il est considéré comme le plus grand expérimentateur de l'antiquité. Parmi ses plus célèbres inventions, une machine à vapeur, appelée l’aéolipile, et un Windwheel, constituant l'un des premiers cas de l'exploitation du vent. Il a été un adepte de la théorie atomique de la matière. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 3

1 Aéolipile de d'Alexandrie 13/09/2021 Héro (ou Héron) Cours de thermodynamique M. Bouguechal Ph 21 4

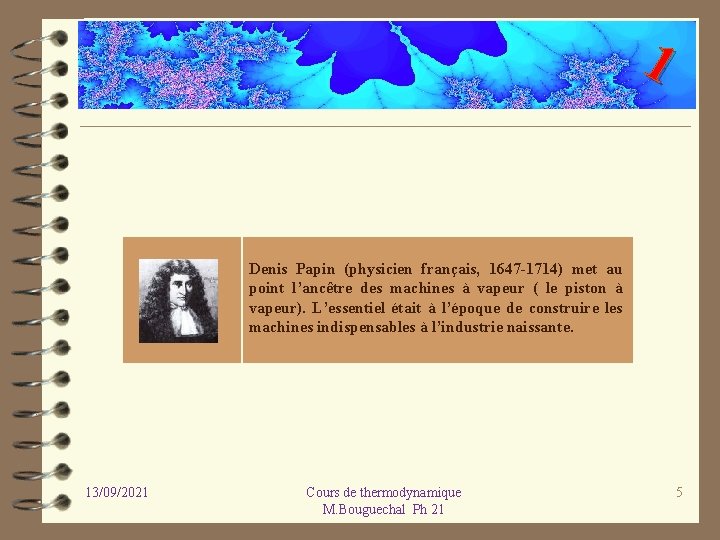
1 Denis Papin (physicien français, 1647 1714) met au point l’ancêtre des machines à vapeur ( le piston à vapeur). L’essentiel était à l’époque de construire les machines indispensables à l’industrie naissante. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 5

1 Piston à vapeur de Denis Papin 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 6

1 On dit que Denis Papin eut l'idée de construire une machine utilisant la vapeur d'eau en regardant bouillir de l’eau dans une marmite. La vapeur soulevant le couvercle, elle pouvait donc aussi repousser un piston et ainsi fournir du travail. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 7

1 La motivation initiale était donc de répondre à un besoin industriel essentiel à l'époque : trouver les conditions optimales pour « transformer » la « chaleur » en « travail » . Dans cette phrase, on trouve les trois mots fondamentaux de la thermodynamique. La thermodynamique est une science qui naît à la fin du XVIIème siècle. Le mot « thermodynamique » vient du grec « thermos » et « dunamikos » qui signifient respectivement chaleur et force. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 8

1 En 1824, Nicolas Léonard Sadi Carnot (physicien français, 1796 1832) développe les premières réflexions sur «la puissance motrice du feu et des machines propres à développer cette puissance» . Ces machines servent alors de support expérimental à une réflexion scientifique et à une ébauche de théorie. En 1831, Carnot propose que la chaleur se conserve: un moteur thermique ne peut fournir du travail que s’il emprunte de la chaleur à la source chaude et en restitue à la source froide. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 9

1 En 1860, James Prescott Joule (physicien et industriel anglais, 1818 1889) franchit une nouvelle étape importante. Il énonce le principe fondateur de la thermodynamique « L’énergie se conserve, c’est à dire que tout travail peut être intégralement transformé en chaleur » . Voilà énoncé le premier principe de la thermodynamique qui ne fait qu’exprimer un postulat maintenant accepté par tous : la conservation de l’énergie. L’énergie devient alors la grandeur importante de la thermodynamique et en particulier l’énergie propre au système : l’énergie interne U. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 10

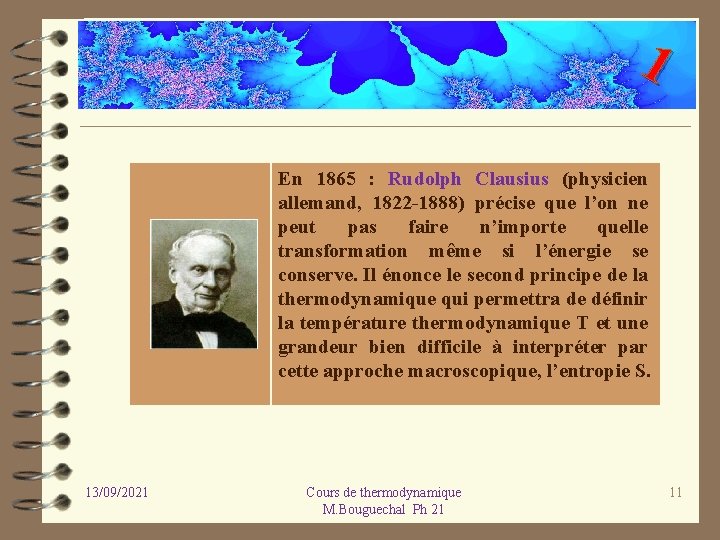
1 En 1865 : Rudolph Clausius (physicien allemand, 1822 1888) précise que l’on ne peut pas faire n’importe quelle transformation même si l’énergie se conserve. Il énonce le second principe de la thermodynamique qui permettra de définir la température thermodynamique T et une grandeur bien difficile à interpréter par cette approche macroscopique, l’entropie S. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 11

1 La thermodynamique du XIXème siècle est la science des transformations thermodynamiques : chaleur → travail. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 12

1 Le modèle de l’atome est loin d’être approuvée à cette époque et la thermodynamique repose donc essentiellement sur des postulats, appelés principes ou lois, sans aucune référence aux atomes ou aux molécules. Depuis le début du XXème siècle, nous savons que l’objet premier de la thermodynamique est l’étude de l'état d'équilibre d’un système. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 13

1 En 1875, les travaux de Ludwig Boltzmann (physicien autrichien, 1844 1906) démontrent que la thermodynamique qui traite avant tout de phénomènes macroscopiques peut être comprise au niveau microscopique, c'est à dire au niveau des molécules. Il introduit la célèbre relation définissant l’entropie d’un système : S = k ln(Ω). Ainsi, il est possible de donner un sens physique aux différentes grandeurs thermodynamiques comme la température, l’énergie interne, la chaleur, l’entropie grâce à la description microscopique d'un système. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 14

1 En 1880, Josiah Williard Gibbs (physicien américain, 1839 1903) généralise le raisonnement de Boltzmann et définit de nouvelles fonctions d’état : énergie libre F, enthalpie libre G… décrivant un état d’équilibre; les notions de chaleur et de travail deviennent alors secondaires. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 15

1 Une nouvelle approche de la thermodynamique se met lentement mais surement en place à la fin du XIXème et au début du XXème siècle. Cette branche de la thermodynamique appelée thermodynamique statistique s’appuie essentiellement sur la description d’un système comportant un grand nombre de molécules ou d’atome, et donc une étude statistique est nécessaire. Cette étude se verra consolidée par les travaux de Max Planck (1900) et Albert Einstein (1905) et d’autres physiciens qui fondent les bases de la théorie de l’atome que l’on appelle la mécanique quantique ou mécanique ondulatoire. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 16

1 La thermodynamique est une science essentielle, à la fois pour la physique : études machines, des matériaux comme les supraconducteurs, les polymères et autres, pour la chimie ( thermochimie ) : réactions et équilibres chimiques. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 17

1. 2 Introduction à la Thermodynamique 1 La thermodynamique est une science qui a pour objet principal l’étude et la description du comportement des systèmes en fonction de certaines grandeurs physiques comme la température T, la pression P, le volume V, mais aussi en fonction d’énergie échangée sous forme de chaleur Q et/ou de travail W. La thermodynamique étudie aussi l’évolution ou les transformations des systèmes en considérant les variations d’état du système lors des échanges d’énergie entre le milieu extérieur et le système. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 18

1. 2 Introduction à la Thermodynamique 1 La thermodynamique étudie aussi l’évolution ou les transformations des systèmes en considérant les variations d’état du système lors des échanges d’énergie entre le milieu extérieur et le système. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 19

1 1. 2 Introduction à la Thermodynamique On peut décrire la thermodynamique de deux manières différentes : ü l'aspect macroscopique : on s'intéresse aux propriétés de la matière ou du système à l'échelle globale ou macroscopique, alors les propriétés sont décrites par des variables d'état macroscopiques telles ( p, V, T, m. . . ) ü l'aspect microscopique : on s'intéresse aux propriétés de la matière à l'échelle microscopique ou atomique en utilisant comme variables grandeurs cinétiques des atomes ou molécules individuelles (pi , vi , Ei. . . ) 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 20

1 1. 2 Introduction à la Thermodynamique Selon que l'on considère l'un ou l'autre de ces aspects, on distingue alors entre la Thermodynamique Classique ou la Thermodynamique Statistique. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 21

1 La Thermodynamique Classique n'a besoin d'aucune hypothèse sur la structure atomique de la matière, elle explique le comportement de la matière ou des systèmes en fonction de leurs variations d'énergie et d'entropie : ü Elle décrit uniquement les états initiaux et finaux des systèmes en évolution et dresse le bilan énergétique du système. ü Le chemin suivi par la transformation du système peut jouer un rôle (notion de réversibilité des transformations). ü Elle ne cherche pas à élucider les mécanismes des transformations. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 22

1 La Thermodynamique Statistique par contre, cherche à expliquer l'origine et la signification des variables macroscopiques (P, T) et des notions de chaleur, de travail et d'entropie, en les reliant directement au mécanisme de l'agitation moléculaire. Ainsi, on explique les notions de température, de pression et de chaleur. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 23

1 La thermodynamique chimique ou thermochimie s’intéresse aux systèmes qui sont le siège d’une réaction chimique ou d’un équilibre chimique. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 24

1 1. 3 Notion de température La température définit le degré d'agitation des particules qui composent un système. Elle se mesure au moyen d'un thermomètre et est l'objet de la thermométrie. L'unité de mesure de la température dans le système international est le Kelvin de symbole K. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 25

1 Le théorème ou le principe de l’équipartition de l’énergie donne une équation qui permet de relier la température d’un système macroscopique aux énergies cinétiques moyennes des particules microscopiques qui le composent. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 26

1 Dans un système à l’équilibre thermodynamique à la température T, chaque degré de liberté contribue pour : à l’énergie totale, où k. B est la constante de Boltzmann Cette relation définit la température absolue T en Kelvin. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 27

1 On définit la température T pour un gaz monoatomique à l’équilibre, ayant donc trois degrés de liberté de translation, suivant les axes Ox, Oy et Oz en coordonnées cartésiennes par la relation : 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 28

1 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 29

1 est la vitesse quadratique moyenne des molécules. N. B : A l’équilibre, la vitesse moyenne des molécules est nulle. En effet, à l’équilibre, il y a autant de molécules suivant l’axe des x positif que de molécules dans le sens négatif. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 30

1 Théorie cinétique des gaz Cours de thermodynamique numero 1cinegaz. html http: //subaru 2. univ lemans. fr/enseignements/ physique/02/thermo/cineg az. html 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 31

1 1. 4 Notion de chaleur La chaleur est une forme ou un mode de transfert d’énergie entre deux systèmes. Lorsqu'on met deux corps en contact, ils échangent de la chaleur : l'un des deux corps a des particules qui ont plus d'énergie cinétique, en les mettant en contact, les chocs entre particules font que cette énergie cinétique microscopique (la chaleur) se transmet d'un corps à l'autre. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 32

1 1. 5 ü Vocabulaire thermodynamique Définition du système Pour décrire thermodynamiquement un système, il faut à la fois : • définir le système en délimitant ses frontières par rapport au milieu extérieur • déterminer l'état du système défini par ses variables. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 33

1 1. 5 Vocabulaire thermodynamique Le système est défini comme étant une région du monde physique dont on se propose d’étudier les propriétés thermodynamiques ( P, T, V, n …). Le système est délimité par une surface qui est sa frontière : celle ci peut être réelle et matérialisée par exemple par les parois d’un récipient ou d’un moteur …ou tout à fait virtuelle comme une étoile, une comète ou une flamme. Sy stè Milieu extérieur ( environnement ) 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 me (P , V , T , n . . ) 34

1 Système Echange Matière Echange de travail Echange de chaleur Energie isolé non non fermé non oui oui ouvert oui oui 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 35

1 Système fermé avec paroi mobile 13/09/2021 Système ouvert Cours de thermodynamique M. Bouguechal Ph 21 Système isolé 36

1 ü Etat du système L'état du système est défini ou décrit par ses variables macroscopiques (m, p, V, T, n. . . ) dites aussi variables d'état. A un système donné est associé tout un ensemble d'états possibles. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 37

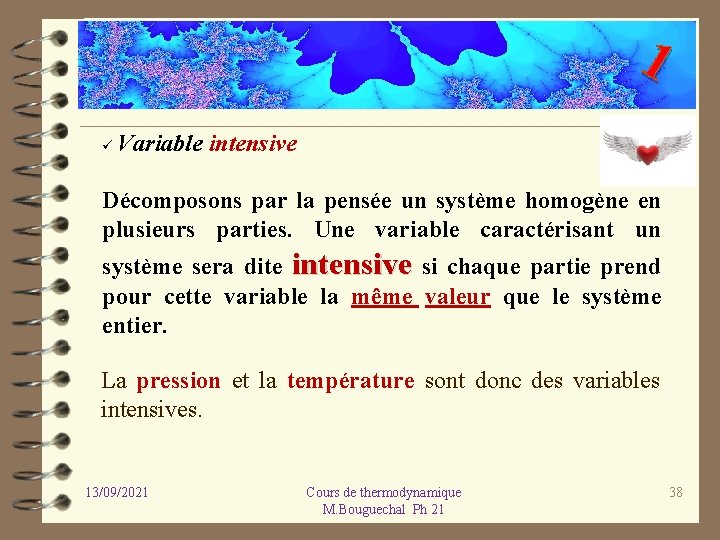
1 ü Variable intensive Décomposons par la pensée un système homogène en plusieurs parties. Une variable caractérisant un système sera dite intensive si chaque partie prend pour cette variable la même valeur que le système entier. La pression et la température sont donc des variables intensives. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 38

1 ü Variable extensive Décomposons par la pensée un système homogène en plusieurs parties. Une variable caractérisant un système sera dite extensive si la valeur de la variable prise par le système entier est la somme des valeurs de la même variable prise pour chaque partie. Le volume et la masse sont donc des variables extensives. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 39

1 On compte courantes : ü ü ü 13/09/2021 parmi les grandeurs intensives La pression La température Les forces La masse volumique La densité Cours de thermodynamique M. Bouguechal Ph 21 40

1 Le rapport de deux grandeurs extensives est intensif. Exemples : la masse volumique, la masse surfacique, la masse linéique, la charge surfacique…. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 41

1 En général une grandeur intensive est associée à une grandeur extensive. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 42

1 On appelle variables conjuguées, un couple de deux variables vérifiant les propriétés suivantes : ü L'une est intensive et l'autre extensive. ü Leur produit est homogène à une énergie. 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 43

1 La pression (variable intensive) est la variable conjuguée du volume (variable extensive). La température (variable intensive) est la variable conjuguée de l'entropie (variable extensive). Le temps (variable intensive) est la variable conjuguée de la puissance (variable extensive). La force (variable intensive) est la variable conjugué de la distance (variable extensive). 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 44

1 le travail élémentaire apparaît toujours comme le produit d’une variable intensive Yi , par la variation élémentaire d’une variable extensive Xi. Ces deux variables sont dites conjuguées. Le travail élémentaire total accompli sur un système s’exprime alors par : 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 45

1 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 46

1 Point méthode 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 47

1 Comment distinguer une variable intensive d’une variable extensive ? 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 48

1 Une variable extensive est proportionnelle à la « taille » du système. Une variable intensive prend une valeur définie en tout point du système et cette valeur est constante 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 49

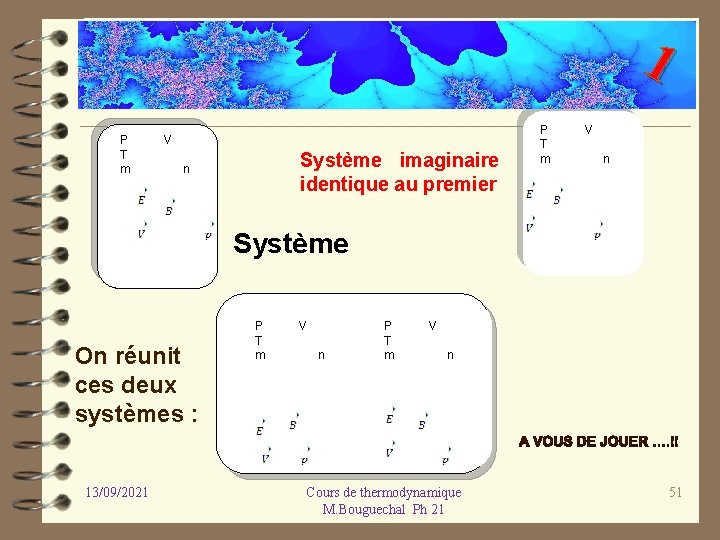
1 Notre système étant défini, on imagine un second système tout à fait identique au premier. ü On réunit ces deux systèmes de telle sorte que l’on obtienne un seul système : on les met côte à côte et on fait une ouverture entre les deux. ü Certaines variables voient leur valeur augmenter : ce sont extensives, les autres conservent la même valeur : ce sont des variables intensives. des variables 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 50

1 P T m V Système imaginaire identique au premier n P T m V n Système On réunit ces deux systèmes : 13/09/2021 P T m V n Cours de thermodynamique M. Bouguechal Ph 21 51

11 Fin de la leçon 1 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 52

1 13/09/2021 Cours de thermodynamique M. Bouguechal Ph 21 53