1 Complmentarit dchantillonneurs passifs et de bioindicateurs pour

1 Complémentarité d’échantillonneurs passifs et de bio-indicateurs pour évaluer la contamination en pesticides eaux de surface de bassins versants agricoles Le Dréau Matthieu, Chaumot Arnaud, Foulquier Arnaud, François Adeline, Geffard Olivier, Margoum Christelle, Pesce Stephane, Martin Caroline, Mazzella Nicolas, Gouy Véronique Groupe Français des Pesticides 27 mai 2015
Contexte et objectifs Diagnostic de la contamination en pesticides d’un cours d’eau // mesure de l’efficacité de plans d’action Analyses chimiques via une stratégie d’échantillonnage ponctuel Limites Mesure de la contamination à un instant t Manque de représentativité temporelle Effets biologiques induits par les pesticides ? Impact? 2
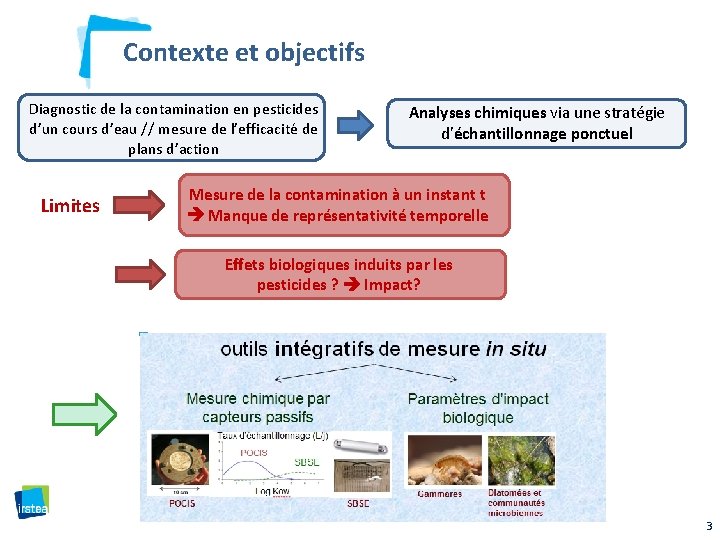
Contexte et objectifs Diagnostic de la contamination en pesticides d’un cours d’eau // mesure de l’efficacité de plans d’action Analyses chimiques via une stratégie d’échantillonnage ponctuel Limites Mesure de la contamination à un instant t Manque de représentativité temporelle Effets biologiques induits par les pesticides ? Impact? 3
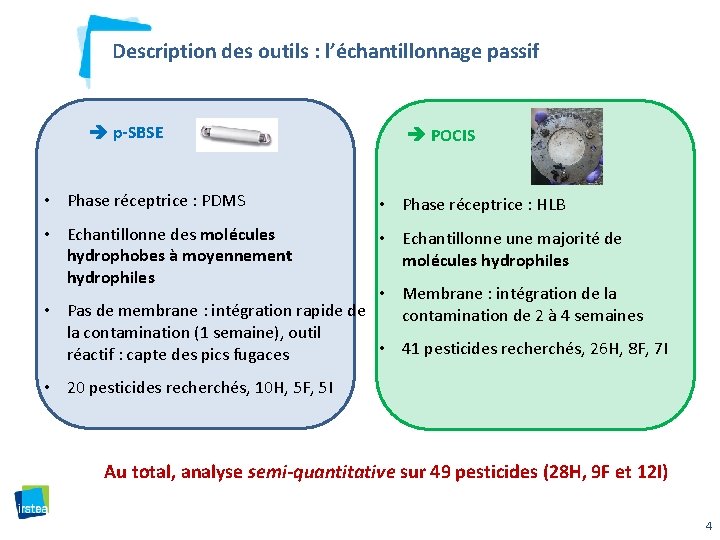
Description des outils : l’échantillonnage passif p-SBSE POCIS • Phase réceptrice : PDMS • Phase réceptrice : HLB • Echantillonne des molécules hydrophobes à moyennement hydrophiles • Echantillonne une majorité de molécules hydrophiles • Membrane : intégration de la • Pas de membrane : intégration rapide de contamination de 2 à 4 semaines la contamination (1 semaine), outil • 41 pesticides recherchés, 26 H, 8 F, 7 I réactif : capte des pics fugaces • 20 pesticides recherchés, 10 H, 5 F, 5 I Au total, analyse semi-quantitative sur 49 pesticides (28 H, 9 F et 12 I) 4
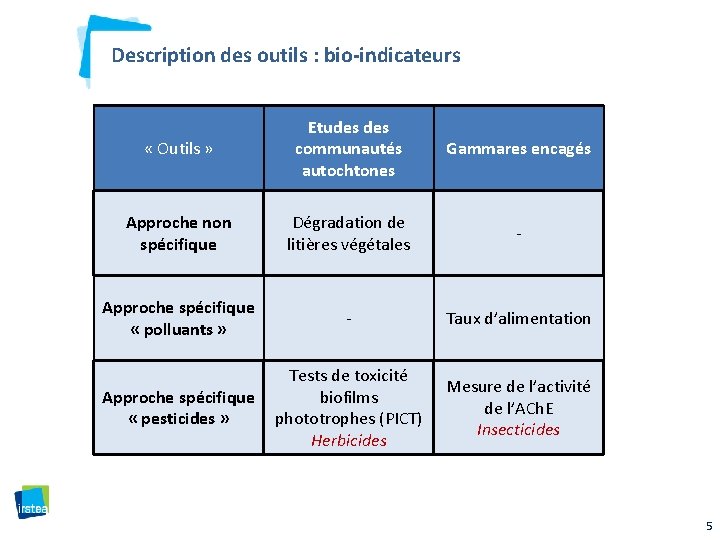
Description des outils : bio-indicateurs « Outils » Etudes communautés autochtones Gammares encagés Approche non spécifique Dégradation de litières végétales - Approche spécifique « polluants » - Taux d’alimentation Tests de toxicité Approche spécifique biofilms « pesticides » phototrophes (PICT) Herbicides Mesure de l’activité de l’ACh. E Insecticides 5
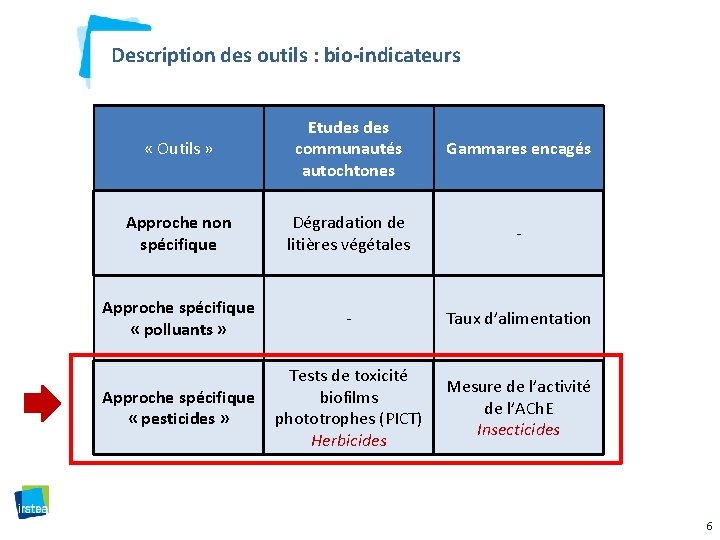
Description des outils : bio-indicateurs « Outils » Etudes communautés autochtones Gammares encagés Approche non spécifique Dégradation de litières végétales - Approche spécifique « polluants » - Taux d’alimentation Tests de toxicité Approche spécifique biofilms « pesticides » phototrophes (PICT) Herbicides Mesure de l’activité de l’ACh. E Insecticides 6

Description des outils : Test de toxicité sur les biofilms phototrophes Immersion de lames de verre (4 semaines) pour colonisation des biofilms naturels Algues (diatomées) Cyanobactéries Herbicides Bactéries/Champignons PICT (Pollution Induced Community tolerance) = des biofilms chroniquement exposés dans le milieu à un toxique s’adaptent et deviennent plus tolérants Réalisation de tests de toxicité aigüs avec un herbicide « modèle » : Etude de la réponse d’un paramètre sensible (photosynthèse, croissance, …) en fonction d’un gradient de concentration Lien entre niveau de sensibilité et exposition préalable au toxique (ou à des toxiques présentant le même mode d’action) 7

Description des outils : Encagement de gammares (monitoring actif) Monitoring actif : transplantation d’organismes non autochtones Calibration des organismes : une seule espèce (Gammarus fossarum), individus mâles, d’une seule population Mesure de l’activité de l’acéthylcholine-estérase ACh. E - Enzyme régulateur du neurotransmetteur ACh - Réponse spécifique aux insecticides inhibiteurs (organo. P et carbamates) - Valeurs obtenues comparées aux valeurs attendues hors contamination (référentiel) Inhibition (ou non) de l’activité ACh. E 8
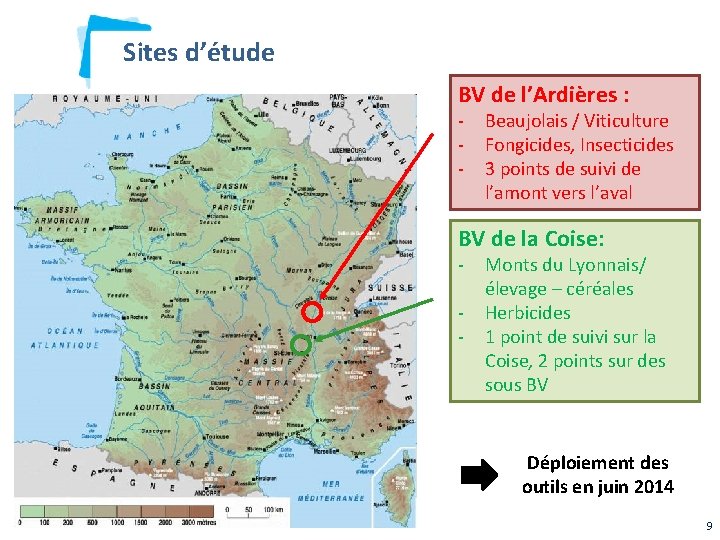
Sites d’étude BV de l’Ardières : - Beaujolais / Viticulture Fongicides, Insecticides 3 points de suivi de l’amont vers l’aval BV de la Coise: - Monts du Lyonnais/ élevage – céréales Herbicides 1 point de suivi sur la Coise, 2 points sur des sous BV Déploiement des outils en juin 2014 9

Quelques résultats…
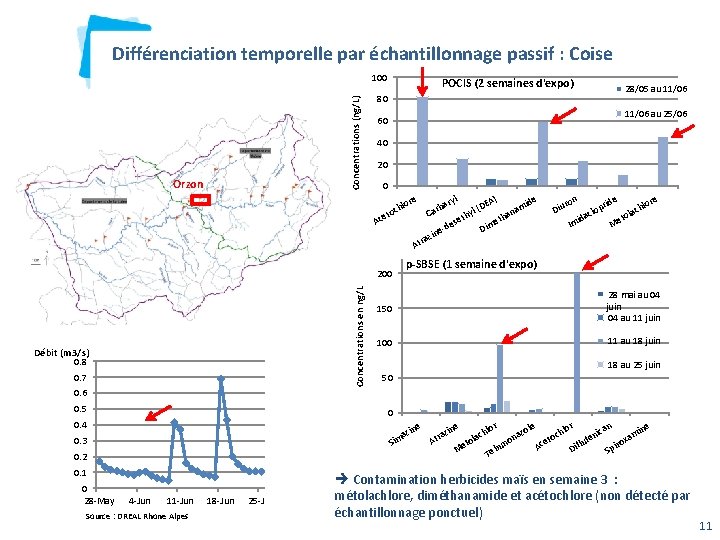
Différenciation temporelle par échantillonnage passif : Coise Concentrations (ng/L) 100 Orzon POCIS (2 semaines d'expo) 11/06 au 25/06 60 40 20 0 re A) de ryl DE mi hlo ( rba a c l a n o C a et thy eth Ac ese m i d D ne azi r t A Concentrations en ng/L 200 Débit (m 3/s) 0. 8 0. 7 0. 6 0. 5 ron Diu id Im rid op acl e e lor ch ola t Me p-SBSE (1 semaine d'expo) 150 28 mai au 04 juin 04 au 11 juin 100 11 au 18 juin 18 au 25 juin 50 0 0. 4 e Sim 0. 3 0. 2 0. 1 0 28 -May 28/05 au 11/06 80 4 -Jun 11 -Jun Source : DREAL Rhone Alpes 18 -Jun 25 -Jun n azi e zin a Atr Me hlo ac tol r Te n bu e zol a on r an ine nic am e f x lu iro Dif Sp hlo A oc cet Contamination herbicides maïs en semaine 3 : métolachlore, diméthanamide et acétochlore (non détecté par échantillonnage ponctuel) 11
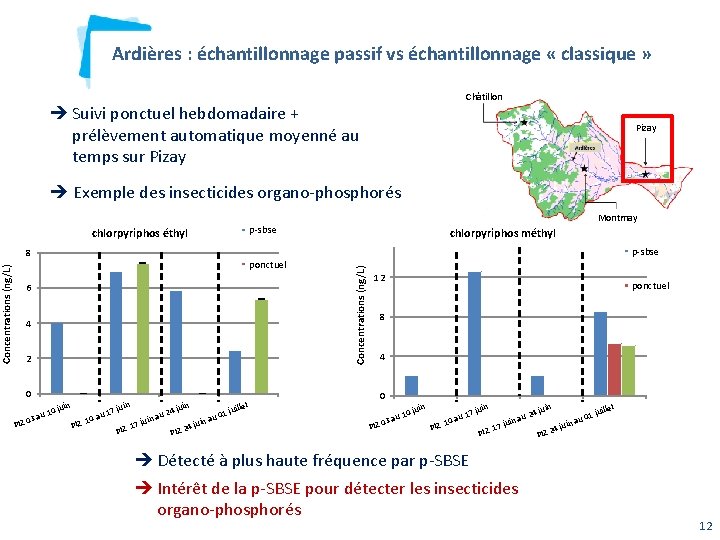
Châtillon Suivi ponctuel hebdomadaire + prélèvement automatique moyenné au temps sur Pizay Exemple des insecticides organo-phosphorés chlorpyriphos éthyl 8 ponctuel 6 4 2 Montmay p-sbse chlorpyriphos méthyl Concentrations (ng/L) Ardières : échantillonnage passif vs échantillonnage « classique » 12 p-sbse ponctuel 8 4 0 let uin uin juil 17 j 10 j 24 j 1 u u u 0 a a a au 03 10 juin PIZ 17 24 j Z PIZ I P 0 PI juin 10 au Z 03 PIZ 17 au 10 PIZ j 17 Détecté à plus haute fréquence par p-SBSE Intérêt de la p-SBSE pour détecter les insecticides organo-phosphorés let uin 24 j au uin juil u 01 in a 4 ju 2 PIZ 12
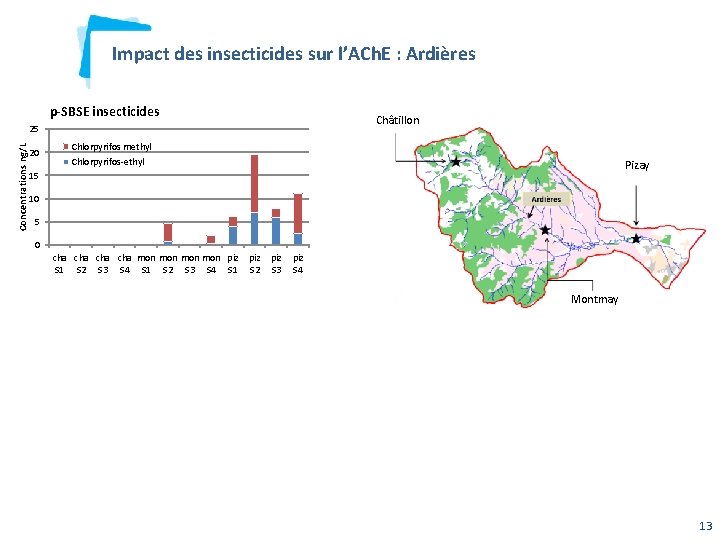
Impact des insecticides sur l’ACh. E : Ardières p-SBSE insecticides Concentrations ng/L 25 20 Chlorpyrifos methyl Châtillon Chlorpyrifos-ethyl Pizay 15 10 5 0 cha cha mon mon piz piz S 1 S 2 S 3 S 4 Montmay 13
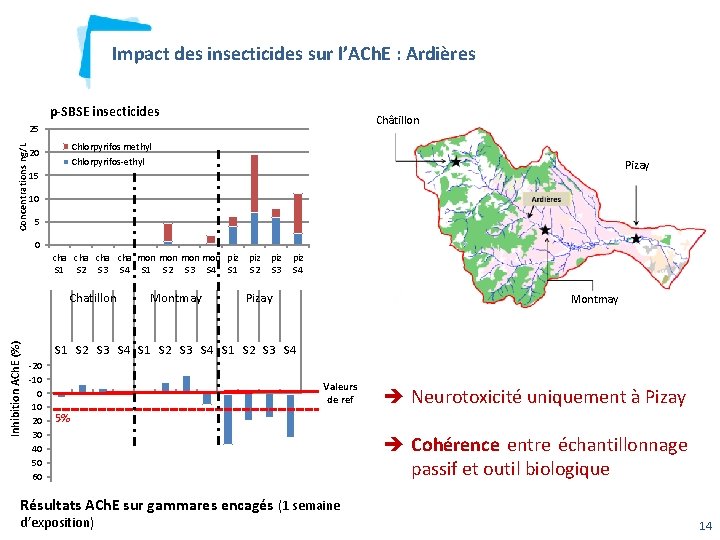
Impact des insecticides sur l’ACh. E : Ardières p-SBSE insecticides Châtillon Concentrations ng/L 25 Chlorpyrifos methyl 20 Chlorpyrifos-ethyl Pizay 15 10 5 0 cha cha mon mon piz piz S 1 S 2 S 3 S 4 Chatillon Montmay Pizay Montmay Inhibition ACh. E (%) S 1 S 2 S 3 S 4 -20 -10 0 10 20 30 40 50 60 70 Valeurs de ref Neurotoxicité uniquement à Pizay 5% Cohérence entre échantillonnage passif et outil biologique Résultats ACh. E sur gammares encagés (1 semaine d’exposition) 14
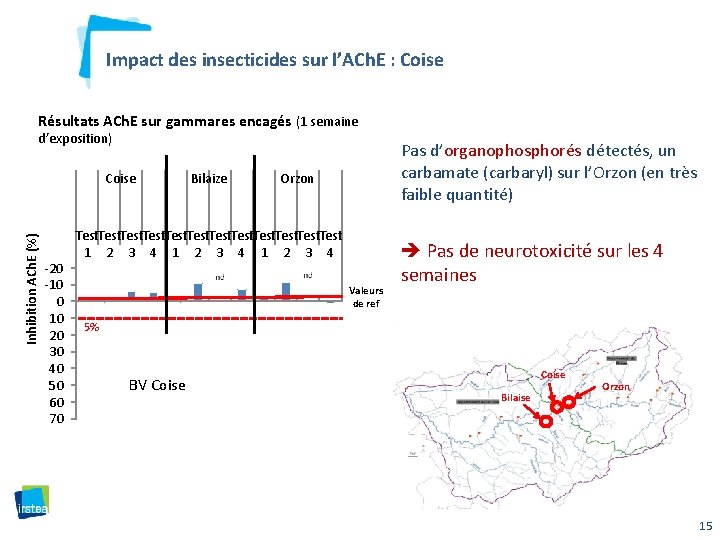
Impact des insecticides sur l’ACh. E : Coise Résultats ACh. E sur gammares encagés (1 semaine d’exposition) Inhibition ACh. E (%) Coise -20 -10 0 10 20 30 40 50 60 70 Bilaize Pas d’organophosphorés détectés, un carbamate (carbaryl) sur l’Orzon (en très faible quantité) Orzon Test Test Test 1 2 3 4 Valeurs de ref Pas de neurotoxicité sur les 4 semaines 5% BV Coise Bilaise Orzon 15

Impact des herbicides sur les biofilms phototrophes : Ardières Données POCIS (ng/L) : Augmentation du diuron d’amont en aval Etudes antérieures : acquisition de tolérance des communautés vis-à-vis du diuron Augmentation de la tolérance des biofilms à cet herbicide ? 16
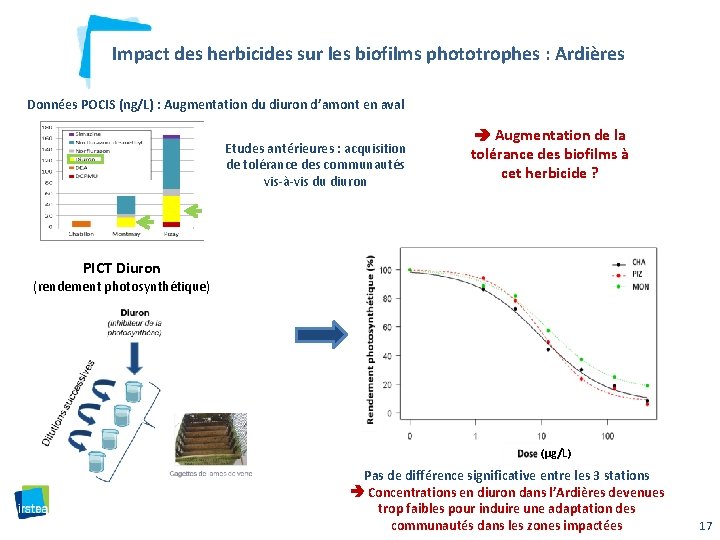
Impact des herbicides sur les biofilms phototrophes : Ardières Données POCIS (ng/L) : Augmentation du diuron d’amont en aval Etudes antérieures : acquisition de tolérance des communautés vis-à-vis du diuron Augmentation de la tolérance des biofilms à cet herbicide ? PICT Diuron (rendement photosynthétique) (µg/L) Pas de différence significative entre les 3 stations Concentrations en diuron dans l’Ardières devenues trop faibles pour induire une adaptation des 17 communautés dans les zones impactées
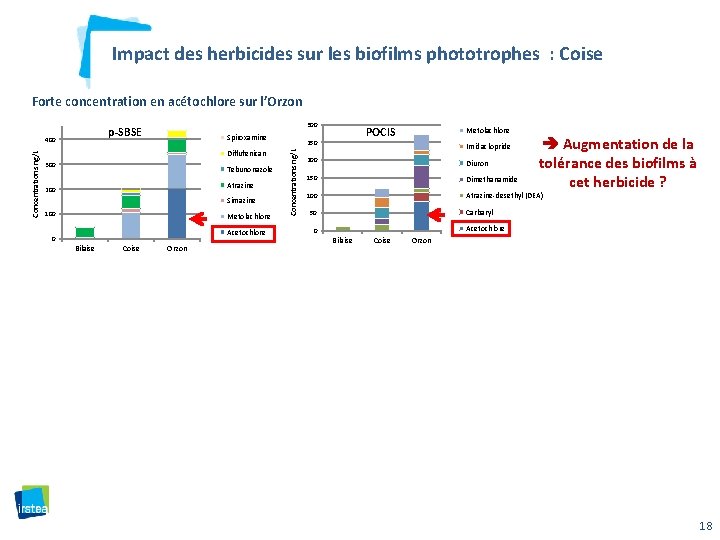
Impact des herbicides sur les biofilms phototrophes : Coise Forte concentration en acétochlore sur l’Orzon Spiroxamine Diflufenican 300 Tebunonazole Atrazine 200 Simazine 100 Metolachlore Acetochlore 0 Bilaise Coise Orzon POCIS 250 Concentrations ng/L 400 Concentrations ng/L 300 p-SBSE Metolachlore Imidaclopride Augmentation de la tolérance des biofilms à cet herbicide ? 200 Diuron 150 Dimethanamide 100 Atrazine-desethyl (DEA) Carbaryl 50 Acetochlore 0 Bilaise Coise Orzon 18
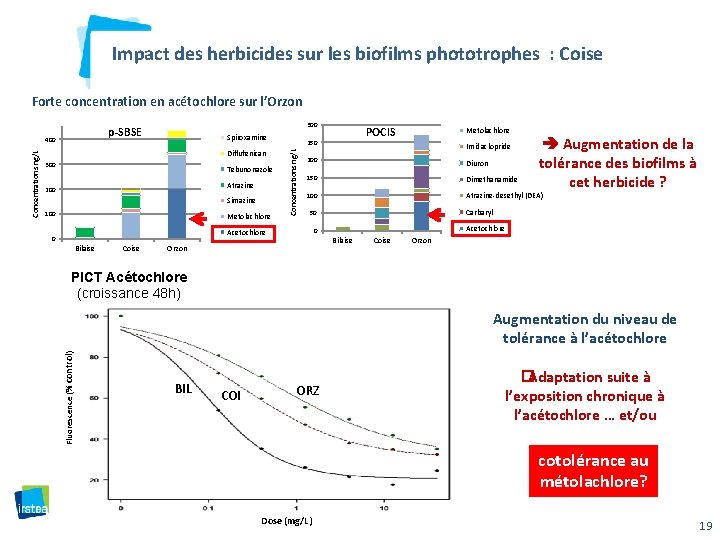
Impact des herbicides sur les biofilms phototrophes : Coise Forte concentration en acétochlore sur l’Orzon Spiroxamine Diflufenican 300 Tebunonazole Atrazine 200 Simazine 100 Metolachlore Bilaise Coise Metolachlore Imidaclopride Augmentation de la tolérance des biofilms à cet herbicide ? 200 Diuron 150 Dimethanamide 100 Atrazine-desethyl (DEA) Carbaryl 50 Acetochlore 0 POCIS 250 Concentrations ng/L 400 Bilaise Orzon Coise Orzon PICT Acétochlore (croissance 48 h) Fluorescence (% control) Concentrations ng/L 300 p-SBSE BIL COI ORZ Augmentation du niveau de tolérance à l’acétochlore � Adaptation suite à l’exposition chronique à l’acétochlore … et/ou cotolérance au métolachlore? Dose (mg/L) 19

Conclusion / Perspectives • Discrimination de typologie de pression (contextes polyculture/ viticulture) • Discrimination de gradients spatiaux (amont-aval, hiérarchisation de SBV) • Réactivité / intégration temporelle de l’effet des crues • Apport vis-à-vis des suivis ponctuels pour l’appui au diagnostic et à l’évaluation d’actions correctives : - Caractère intégratif (concentration plus représentative, piégeage de SA « fugaces » ) - Information sur l’impact biologique (outil gammares opérationnel, encore des développements requis pour les communautés microbiennes) • Perspectives 2015 : - Consolidation des résultats sur les mêmes BV + un nouveau site de grandes cultures céréalières, - Rédaction d’un guide opérationnel • A plus long terme : - Elargir la gamme des substances recherchées (dont métabolites) (apport de l’analyse non ciblée ? ) - Compléter les outils biologiques (gamme d’impacts, effets long terme) 20

Remerciements • Equipe EMHA : Motte B. , Volat B. , Rosy C. • Equipe Ecotox : Noury P. , Quéau H. • Equipe CARMA : Moreira A. , Gery K. • Equipe POLLDIFF: Liger L. , Le Hénaff G. • Equipe LAMA : Martin A. , Assoumani A. , Guillemain C. , laboratoires majeurs et métaux • Syndicats de rivières : SMRB, SIMA Coise 21
- Slides: 21