1 ACIDOS Y BASES DEFINICIN cido es toda

1 ACIDOS Y BASES

DEFINICIÓN Ácido: es toda sustancia que en disolución acuosa se disocia con formación de iones hidrógeno, H+ 2 Base: sería toda sustancia que en disolución acuosa se disocia con formación de iones hidróxido, OH-

CARACTERISTICAS Ácidos Bases Tienen sabor agrio (limón, vinagre, etc). Tiene sabor cáustico o amargo (a lejía) En disolución acuosa enrojecen la tintura o papel de tornasol En disolución acuosa azulean el papel o tintura de tornasol Decoloran la fenolftaleína enrojecida por las bases Enrojecen la disolución alcohólica de la fenolftaleína Producen efervescencia con el carbonato de calcio (mármol) Producen una sensación untuosa al tacto Reaccionan con algunos metales desprendiendo hidrógeno Precipitan sustancias disueltas por ácidos Neutralizan la acción de las bases Neutralizan la acción de los ácidos En disolución acuosa dejan pasar la corriente eléctrica, experimentando ellos, al mismo tiempo una descomposición química En disolución acuosa dejan pasar la corriente eléctrica, experimentando ellas, al mismo tiempo, una descomposición química Concentrados destruyen los tejidos biológicos vivos (son corrosivos para la piel) Suaves al tacto pero corrosivos con la piel (destruyen los tejidos vivos) Enrojecen ciertos colorantes vegetales (cambian a rojo) Dan color azul a ciertos colorantes vegetales Pierden sus propiedades al reaccionar con bases Pierden sus propiedades al reaccionar con ácidos 3
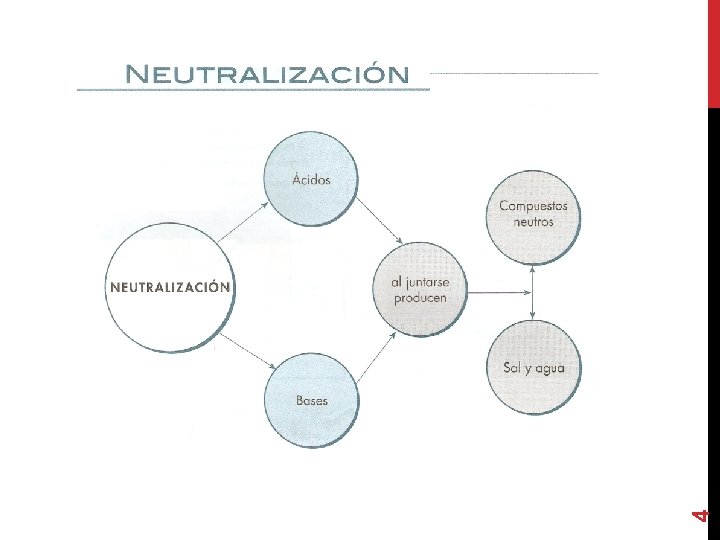
4

5

H P POTENCIAL DE IONES HIDRÓGENO El p. H sirve para indicar de forma precisa la acidez o basicidad de una sustancia. Normalmente oscila entre los valores de 0 (más ácido) y 14 (más básico). Indicadores: 6 Los indicadores son colorantes orgánicos, que cambian de color según estén en presencia de una sustancia ácida, o básica.

Dos tipos de ácidos inorgánicos: Hidrácidos = Hidrógeno + No Metal Ejemplo HCl Oxiacidos = Hidrógeno No Metal y Oxigeno 7 Ejemplo HCO 3

Nomenclatura Stock Se nombra al no metal con el sufijo ato, seguido del valor de la valencia del no metal y por último se agrega de hidrógeno. 8

Nomenclatura clásica ó tradicional Para formar los ácidos correspondientes del carbono, se parte de su óxido o anhídrido ( es decir de su radical) en presencia de agua, reaccionan y se produce: 9

Reglas para nombrar los ácidos de acuerdo a su radical: 1. - Cambiar la terminación del radical: uro hídrico Hidrácidos Ato ico Ito oso Oxácidos 10 2. - No se llaman radical “ de hidrogeno” sino que primero se nombra la palabra “acido” y después el radical con la terminación apropiada

Ejemplos HNO 3 radical nitrato cambia a ico Nitrato de Hidrogeno Acido Nítrico HCl Radical = cloruro, uro cambia a hídrico 11 Acido Clorhídrico
- Slides: 11