1 7 Ders EVRMSEL DNCE ZERNE BR RNEK

1 7. Ders: EVRİMSEL DÜŞÜNCE ÜZERİNE BİR ÖRNEK ; HIV DOÇ. DR. YEŞIM DOĞAN ANKARA ÜNIVERSITESI DTCF ANTROPOLOJI BÖLÜMÜ

2 NEDEN EVRİM ÇALIŞIYORUZ ?

3 EVRİM ÇALIŞANLAR 1. Çevrede meydana gelen değişimler sonucu popülasyonda meydana gelen değişimleri anlamaya çalışır. 2. Yeni türler nasıl oluşur? Anlamaya çalışır. SONUÇ OLARAK ; adaptasyon ve çeşitlilik

4 (Human Immuno Deficiency Syndrome (AIDS) İnsanlık tarihinin en yıkıcı epidemilerinden biri HIV 1. Azidotimidin (AZT) ilk kullanımda ümit vaadetmiş ancak sonra etkili olmamıştır. Neden? 2. HIV insanları neden öldürür? 3. Bazı insanlar enfeksiyona rağmen hastalığa direnç gösterir. Neden ? HIV nereden gelmektedir? ��
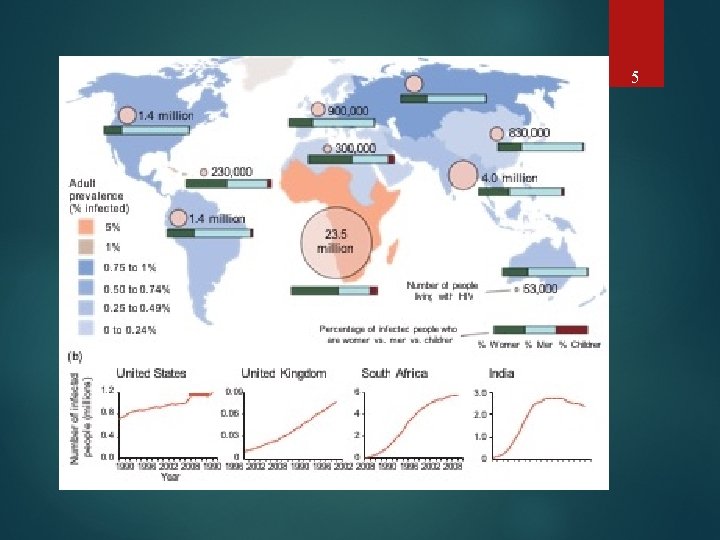
5
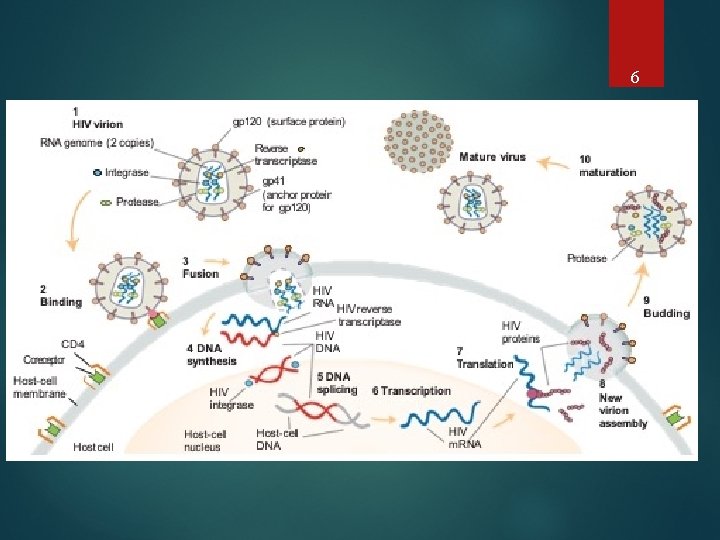
6
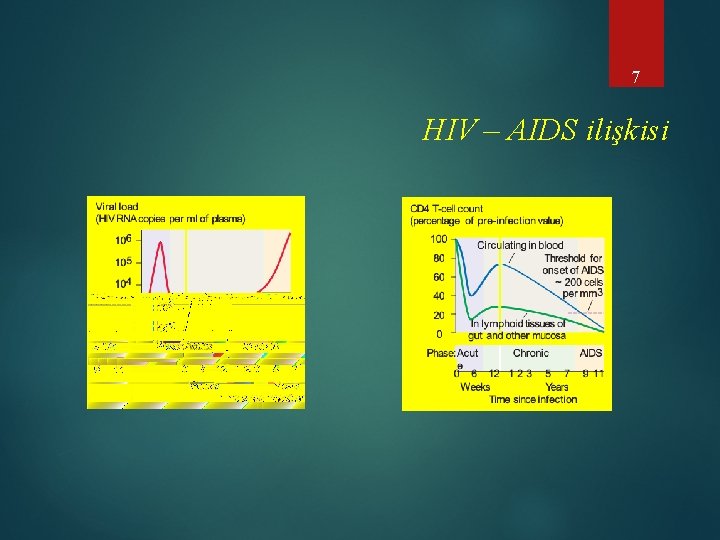
7 HIV – AIDS ilişkisi
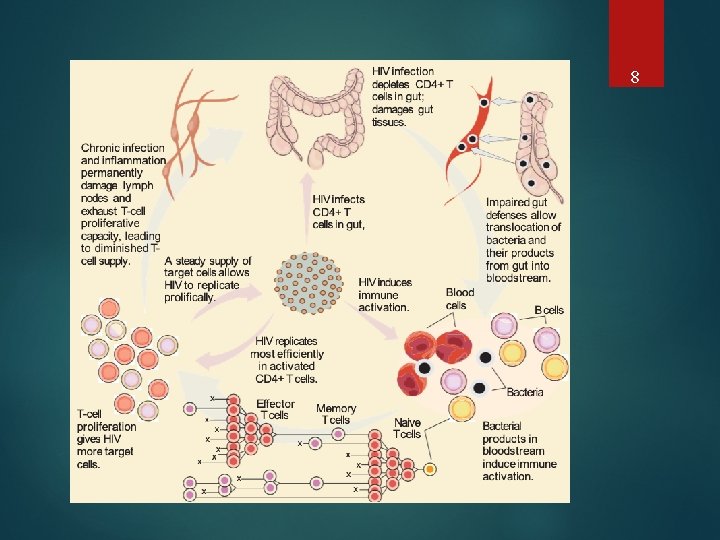
8

9 Tedavide yaşanan zorluklar ? Tedavi için kullanılacak ilaç konakçıya minimum zarar ile virüsü durdurmalı ? ?
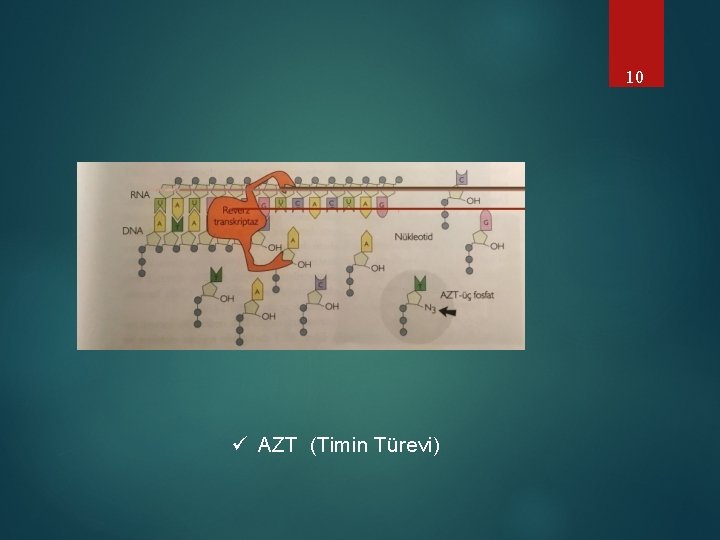
10 ü AZT (Timin Türevi)

11 AZT tedavisi umut verici gibi Maksimum 6 ay olumlu etki (Hücre kültürü çalışmaları) AZT tedavisi gören hastalardan virüs izolasyonu Sekans analizi (reverse transkriptaz enzimi) Reverse transkriptaz aktif merkezinde mutasyon
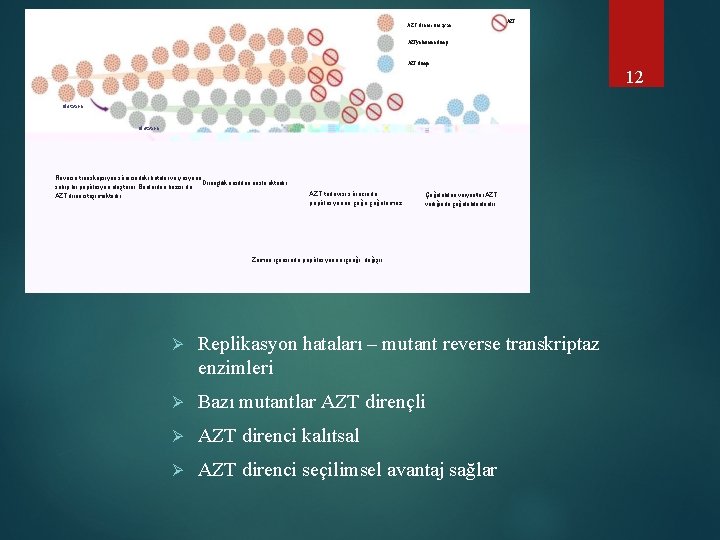
. AZT direnci olmayan AZT’ye kısmen dirençli AZT dirençli 12 Mutation Reverse transkripsiyon sürecindeki hatalar varyasyona Dirençlilik nesilden nesle aktarılır sahip bir popülasyon oluşturur. Bunlardan bazısı da AZT direnci taşımaktadır. AZT tedavisi sürecinde popülasyonun çoğu çoğalamaz Çoğalabilen varyantlar AZT varlığında çoğalabilenlerdir Zaman içerisinde popülasyonun içeriği değişir Ø Replikasyon hataları – mutant reverse transkriptaz enzimleri Ø Bazı mutantlar AZT dirençli Ø AZT direnci kalıtsal Ø AZT direnci seçilimsel avantaj sağlar

13 Direnç mekanizmasının anlaşılması umut verdi? ? NEDEN?

14 Ama HAART tedavileri de virüsü kazımaz. Sadece üremeyi durdurur. . Neyseki üremeyen evrimleşemez Ama HAART yan etkileri nedeni ile uzun süre uygulanamaz

15 İleriyi görmeyen evrim PARADOKS!!

16 EPİTOP: HIV tarafından enfekte olan hücrelerin yüzeylerinde HIV’e ait protein kalıntıları olur. Epitoplar da HIV genleri tarafından sentezlenir Onlar da mutant olabilir. Bu da tanınmamaları için avantaj kazandırır.

17 HIV Farklı epitopları olan varyantlar oluşturmak üzere sürekli evrimleşir Bir insanda enfeksiyonun ilk döneminde izole edilen virüsler ile daha sonra izole edilenler arasında zararlılık yönünde bir artış gözlenir Hücreye koreseptörleri kullanarak girerler (CCR 5), evrimleşen HIV CXCR 4’ü de koreseptör olarak kullanmaya başlar ( özelleşmiş T hücrelerini enfekte edebilirler)

18 Akılcı süreç değil, matematiksel bir süreç İleriyi Göremeyen Evrim !! Sonuç KONAĞIN ÖLÜMÜ !! Peki konakçı? Üstelik X 4 virionlar başka konağa da aktarılamıyor

19 Nadir HIV suşları Sydney Kan Bankası Vakası ( 1 verici – 8 alıcı) 25 yıl boyunca takip edilmişler 2 kişi HIV dışı nedenlerle öldü 2 kişi 17 yıl sonra AIDS oldu. Retro viral tedaviden fayda gördüler 2 kişi de viral yük tespit bile edilemedi 1 kişi viral yük tespit edilmesine rağmen AIDS olmadı

20 Genetik Analiz nef geninde mutasyon DAHA AZ ZARARLI Konakçı yaşar, virüs popülasyonu da yaşar Daha başarılı gibi ama neden nadir ?

21 SIV (Simian Immün Deficiency Virus) HIV’in yakın akrabası Yeşil maymunlar enfekte – ama hasta değil Rhesus maymunu enfekte – AIDS Gerçek konak bir bağışıklık mekanizması geliştirmiş HIV için iyi bir haber olabilir mi?

22 HIV için bağışıklık mekanizması geliştirebilmemiz için ne gerekli ? Parmaklar havaya ! Bu soru önemli ��

23 Bazı bireyler defalarca karşılaşmalarına rağmen virüsü kapmıyor ? ? CCR 5 geni HIV’in hücre içine giriş için kullandığı reseptör Bu bireylerde CCR 5 geni mutant 32 bazlık delesyon (�� 32)

24 Yeşil maymunlarda da CCR 5 bir amino asit farklı Kırmızı maymunlarda 24 bazlık delesyon İsli maymunlarda proteini işlevsiz kılan çeşitli delesyonlar Peki �� 32’nin yeryüzündeki popülasyonlarda freka nedir?

�� HAYDAA! 25
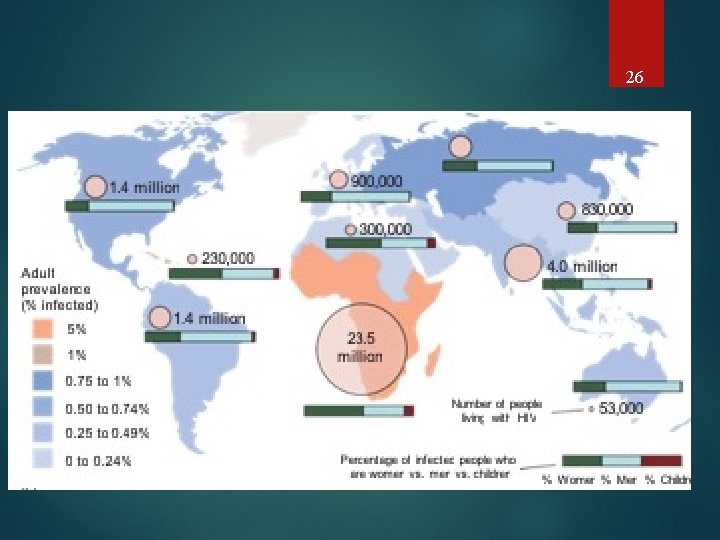
26

27 Peki bu AIDS dağılımı ile �� 32 dağılımının uyumsuzluğunu nasıl açıklayacağız ��

28 2 olasılık üzerinde duruluyor ; 1. 2. Doğal Seçilim ile teşvik Genetik sürüklenme ile raslantısal artış

29 PEKİ HIV’in KÖKENİ NEDİR? SIV virüsü ile benzer? Ama hangi SIV, HIV kökeni olabilir Filogenetik analiz Kladogram ya da filogenetik ağaç
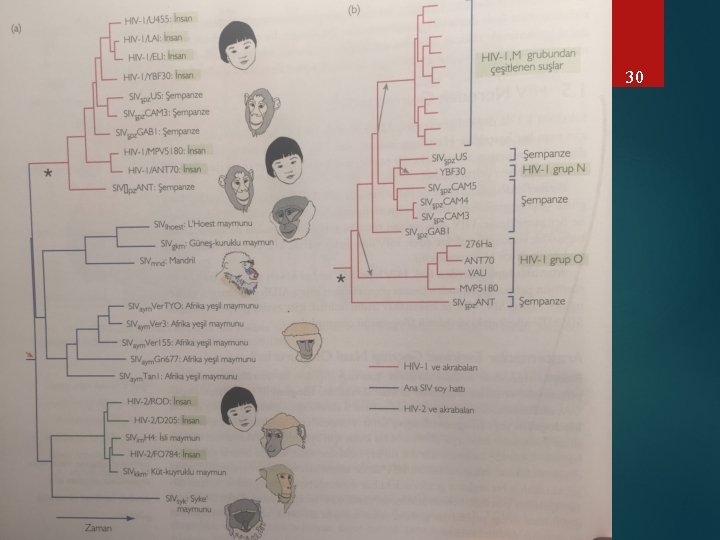
30

31 HIV aşısı neden yok ? Aşı çalışmaları gp 120 epitoplarına yönelik Onlarca alt grup 1959’da Kongo’lu bir erkekten alınan kanda virüs 4— 50 yılda virüs çeşitlenmesinin boyutlarını gösteriyor

Bir Soru? �� HIV için kullanılan çoklu ilaç tedavisinin ardında yatan düşünce, direncin gerçekleşebilmesi için gerekli mutasyon sayısının arttırılması ve böylece virüs popülasyonunun devamlılığını sağlayacak genetik çeşitlilik miktarının ilaç varlığında azaltılmasıdır. Aynı etkiyi antiviral ilaçları aynı anda kullanmak yerine sırayla kullanmakla da başarabilir miyiz? Neden evet ya da neden değil ? 32
- Slides: 32