1 2 TERIA HYBRIDIZCIE Seminr z CH 11

-1 - -2 - TEÓRIA HYBRIDIZÁCIE Seminár z CH 11 (13. , 14. vyuč. hod. ) z Teória hybridizácie 180° (PREHĽAD CHÉMIE P. Silný, B. Brestenská str. 69 -72) Pomocou teórie valenčných väzieb sa nedali vysvetliť niektoré experimentálne namerané údaje o štruktúre veľkého počtu molekúl ( väzbové uhly v molekule, energia väzieb), napr. Be. Cl 2 , BF 3 , CH 4 , NH 3 , H 2 O a mnohých ďalších. Pre vysvetlenie experimentálne nameraných údajov pre vyššie uvedené molekuly bola vytvorená teória hybridizácie. Základom hybridizácie je predstava, že atóm nevytvára väzbu pomocou energeticky rozdielnych atómových orbitálov vo valenčnej vrstve (napr. s a p atómových orbitálov), ale vo valenčnej vrstve atómu sa lineárnou kombináciou energeticky rozdielnych atómových orbitálov vytvárajú energeticky rovnocenné hybridné orbitály, ktoré sa potom zúčastňujú s inými atómami na tvorbe kovalentných väzieb v molekulách. Pri tvorbe hybridných orbitálov platia tieto pravidlá: a) Počet vytvorených hybridných orbitálov sa rovná počtu pôvodných atómových orbitálov, z ktorých vznikli. Napríklad ak dochádza k lineárnej kombinácii jedného s a troch p atómových orbitálov, vznikajú štyri hybridné orbitály. b) Hybridné orbitály môžu vzniknúť lineárnou kombináciou len energeticky blízkych atómových orbitálov. Napríklad hybridné orbitály môžu vzniknúť z 2 s a 2 p atómových orbitálov, ale nemôžu sa kombinovať atómové orbitály 1 s a 2 p – pretože sú energeticky značne rozdielne. c) Hybridné orbitály majú iné tvary ako pôvodné atómové orbitály, sú nesymetricky rozložene vzhľadom na jadro atómu. Kovalentné väzby tvorené hybridnými orbitálmi sú pevnejšie, lebo dochádza k väčšiemu prekryvu hybridných orbitálov v porovnaní s prekrytím pôvodných atómových orbitálov. HYBRIDIZÁCIA sp Lineárnou kombináciou jedného atómového orbitálu s a jedného atómového orbitálu p vzniknú dva energeticky rovnocenné hybridné orbitály – sp. V priestore sú umiestnené pozdĺž priamky – lineárne, zvierajú uhol 180°. z z z hybridizácia y s orbitál x y y p orbitál y a) x y dva sp hybridné orbitály Vznik dvoch sp hybridných orbitálov p Be – sp Cl sp – p b) HYBRIDIZÁCIA sp 2 Lineárnou kombináciou jedného atómového orbitálu s a dvoch atómových orbitálov p vzniknú tri energeticky rovnocenné hybridné orbitály – sp 2. V priestore majú trigonálne (trojuholníkové) usporiadanie a navzájom zvierajú uhol 120°. z 120° 2 Vznik väzieb v molekule BF 3 možno vysvetliť takto: tvoria tri sp 2 hybridné orbitály Vznik troch sp hybridných orbitálov x 120° Geometrické usporiadanie väzieb v molekule BF 3 HYBRIDIZÁCIA sp 3 Lineárnou kombináciou jedného atómového orbitálu s a troch atómových orbitálov p vzniknú štyri energeticky rovnocenné hybridné orbitály – sp 3. V priestore smerujú do vrcholov tetraédra a zvierajú uhly 109° 28'. Príkladom hybridizácie sp 3 je vznik štyroch rovnocenných väzieb v molekule metánu CH 4. Hybridizácia sp umožňuje vysvetliť vznik väzieb v molekule Be. Cl 2. Atóm berília má v základnom stave vo valenčnej sfére len dva spárené elektróny (2 s 2 ). Vznik dvoch rovnocenných väzieb, ktoré vznikajú v priebehu reakcie Be + Cl 2 Be. Cl 2 možno vysvetliť takto: Be 1 s 2 2 s 2 – základný stav Be* 1 s 2 2 s 1 2 p 1 – vzbudený stav Cl Vznik dvoch hybridných orbitálov sp (a), vznik väzieb v molekule Be. Cl 2 (b) z x x Be. Cl 2 lineárna x molekula 180° tvoria štyri sp 3 hybridné orbitály
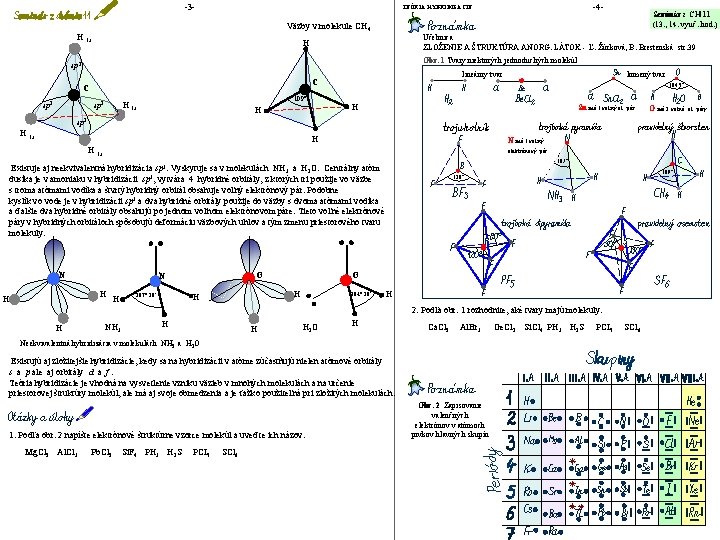
-3 - -4 - TEÓRIA HYBRIDIZÁCIE Seminár z CH 11 (13. , 14. vyuč. hod. ) Väzby v molekule CH 4 H 1 s Učebnica ZLOŽENIE A ŠTRUKTÚRA ANORG. LÁTOK - Ľ. Žúrková, B. Brestenská str. 39 H Obr. 1 Tvary niektorých jednoduchých molekúl sp 3 lineárny tvar C C 109° H 1 s sp 3 lomený tvar 104, 5° H H Sn má 1 voľný el. pár O má 2 voľné sp 3 H 1 s H N má 1 voľný H 1 s elektrónový pár 107° Existuje aj neekvivalentná hybridizácia sp 3. Vyskytuje sa v molekulách NH 3 a H 2 O. Centrálny atóm dusíka je v amoniaku v hybridizácii sp 3, vytvára 4 hybridné orbitály, z ktorých tri použije vo väzbe s troma atómami vodíka a štvrtý hybridný orbitál obsahuje voľný elektrónový pár. Podobne kyslík vo vode je v hybridizácii sp 3 a dva hybridné orbitály použije do väzby s dvoma atómami vodíka a ďalšie dva hybridné orbitály obsahujú po jednom voľnom elektrónovom páre. Tieto voľné elektrónové páry v hybridných orbitáloch spôsobujú deformáciu väzbových uhlov a tým zmenu priestorového tvaru molekuly. N H H H 107° 20' O O N H H 109° 120° 104° 30' H 2. Podľa obr. 1 rozhodnite, aké tvary majú molekuly: H NH 3 H H H 2 O H Ca. Cl 2 Al. Br 3 Neekvivalentná hybridizácia v molekulách NH 3 a H 2 O Existujú aj zložitejšie hybridizácie, kedy sa na hybridizácii v atóme zúčastňujú nielen atómové orbitály s a p ale aj orbitály d a f. Teória hybridizácie je vhodná na vysvetlenie vzniku väzieb v mnohých molekulách a na určenie priestorovej štruktúry molekúl, ale má aj svoje obmedzenia a je ťažko použiteľná pri zložitých molekulách. 1. Podľa obr. 2 napíšte elektrónové štruktúrne vzorce molekúl a uveďte ich názov: Mg. Cl 2 Al. Cl 3 Pb. Cl 2 Si. F 4 PH 3 H 2 S PCI 5 SCl 6 Obr. 2 Zapisovanie valenčných elektrónov v atómoch prvkov hlavných skupín Ge. Cl 2 Si. Cl 4 PH 3 H 2 S PCI 5 SCl 6 el. páry
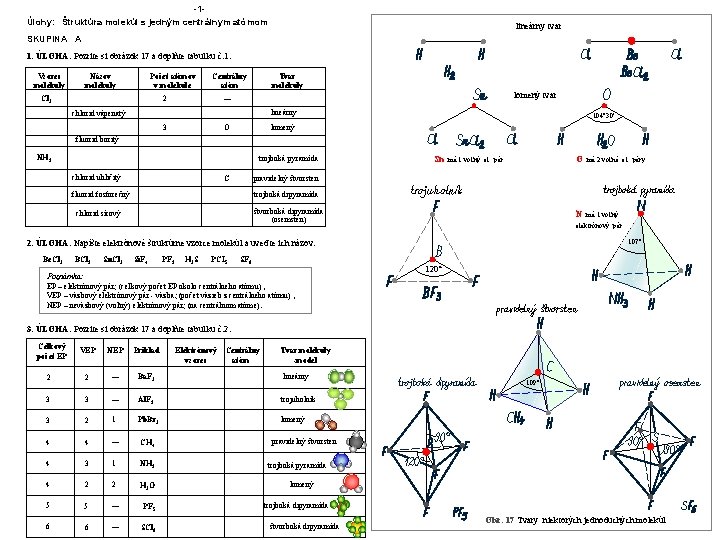
-1Úlohy: Štruktúra molekúl s jedným centrálnym atómom lineárny tvar SKUPINA A 1. ÚLOHA: Pozrite si obrázok 17 a doplňte tabuľku č. 1. Vzorec molekuly Názov molekuly Počet atómov v molekule Centrálny atóm 2 Cl 2 Tvar molekuly lomený tvar — lineárny chlorid vápenatý 3 O 104° 30' lomený fluorid boritý NH 3 trojboká pyramída chlorid uhličitý C Sn má 1 voľný el. pár štvorboká dipyramída (osemsten) má 1 voľný elektrónový pár 2. ÚLOHA: Napíšte elektrónové štruktúrne vzorce molekúl a uveďte ich názov: Sn. Cl 2 N trojboká dipyramída chlorid sírový BCl 3 má 2 voľné el. páry pravidelný štvorsten fluorid fosforečný Be. Cl 2 O Si. F 4 PF 3 H 2 S PCI 5 SF 6 Poznámka: EP – elektrónový pár; (celkový počet EP okolo centrálneho atómu) , VEP – väzbový elektrónový pár - väzba; (počet väzieb z centrálneho atómu) , NEP – neväzbový (voľný) elektrónový pár; (na centrálnom atóme). 107° 120° 3. ÚLOHA: Pozrite si obrázok 17 a doplňte tabuľku č. 2. Celkový počet EP VEP NEP Príklad Elektrónový vzorec Centrálny atóm Tvar molekuly -model 2 2 — Ba. F 2 lineárny 3 3 — Al. F 3 trojuholník 3 2 1 Pb. Br 2 lomený 4 4 — CH 4 4 3 1 NH 3 4 2 2 H 2 O 5 5 — PF 5 6 6 — SCl 6 109° pravidelný štvorsten trojboká pyramída lomený trojboká dipyramída štvorboká dipyramída Obr. 17 Tvary niektorých jednoduchých molekúl
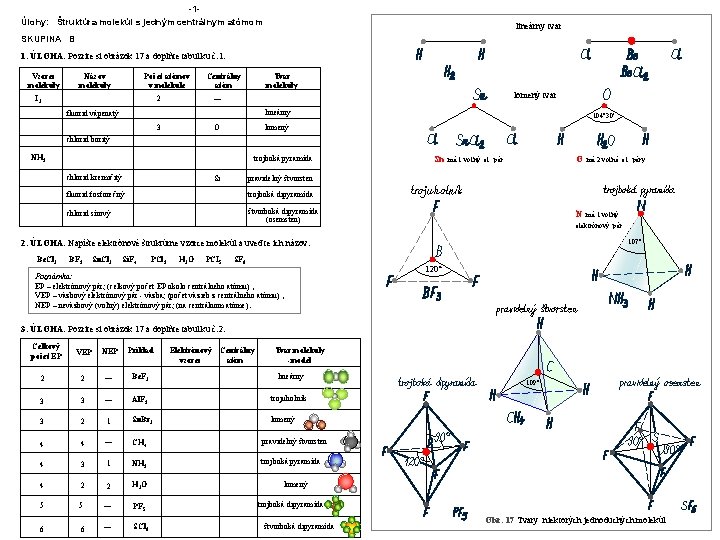
-1Úlohy: Štruktúra molekúl s jedným centrálnym atómom lineárny tvar SKUPINA B 1. ÚLOHA: Pozrite si obrázok 17 a doplňte tabuľku č. 1. Vzorec molekuly Názov molekuly Počet atómov v molekule Centrálny atóm 2 I 2 Tvar molekuly lomený tvar — lineárny fluorid vápenatý 3 O 104° 30' lomený chlorid boritý NH 3 trojboká pyramída chlorid kremičitý Si Sn má 1 voľný el. pár fluorid fosforečný trojboká dipyramída chlorid sírový štvorboká dipyramída (osemsten) BF 3 Sn. Cl 2 Si. F 4 PCl 3 H 2 O PCI 5 má 2 voľné el. páry N má 1 voľný pravidelný štvorsten elektrónový pár 2. ÚLOHA: Napíšte elektrónové štruktúrne vzorce molekúl a uveďte ich názov: Be. Cl 2 O SF 6 107° 120° Poznámka: EP – elektrónový pár; (celkový počet EP okolo centrálneho atómu) , VEP – väzbový elektrónový pár - väzba; (počet väzieb z centrálneho atómu) , NEP – neväzbový (voľný) elektrónový pár; (na centrálnom atóme). 3. ÚLOHA: Pozrite si obrázok 17 a doplňte tabuľku č. 2. Celkový počet EP VEP NEP Príklad Elektrónový vzorec Centrálny atóm Tvar molekuly -model 2 2 — Be. F 2 lineárny 3 3 — Al. F 3 trojuholník 3 2 1 Sn. Br 2 lomený 4 4 — CH 4 pravidelný štvorsten 4 3 1 NH 3 trojboká pyramída 4 2 2 H 2 O 5 5 — PF 5 6 6 — SCl 6 109° lomený trojboká dipyramída štvorboká dipyramída Obr. 17 Tvary niektorých jednoduchých molekúl
- Slides: 4