0 La Lettre du Cancrologue Dclaration publique de

0 La Lettre du Cancérologue

Déclaration publique de liens d’intérêts 1 • Jean-Yves Pierga déclare avoir des liens d’intérêts avec MSD, Roche, Novartis, Pfizer et Amgen. • Céline Rouger déclare n’avoir aucun lien d’intérêt. La Lettre du Cancérologue SABCS 2018

2 La Lettre du Cancérologue

• Introduction……. . . . 4 • Immunothérapie en association……. 7 • Facteurs prédictifs de réponse……. 24 • Biomarqueurs……. . . . 40 • Concept d’immunomodulation……. . 43 La Lettre du Cancérologue

Chapitre I Introduction Céline Rouger (Villejuif) La Lettre du Cancérologue
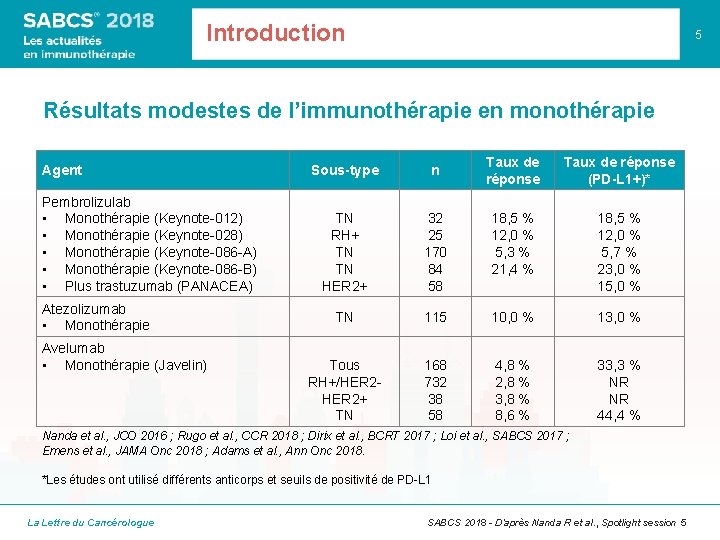
Introduction 5 Résultats modestes de l’immunothérapie en monothérapie Agent Pembrolizulab • Monothérapie (Keynote-012) • Monothérapie (Keynote-028) • Monothérapie (Keynote-086 -A) • Monothérapie (Keynote-086 -B) • Plus trastuzumab (PANACEA) Atezolizumab • Monothérapie Avelumab • Monothérapie (Javelin) Taux de réponse (PD-L 1+)* 32 25 170 84 58 18, 5 % 12, 0 % 5, 3 % 21, 4 % 18, 5 % 12, 0 % 5, 7 % 23, 0 % 15, 0 % TN 115 10, 0 % 13, 0 % Tous RH+/HER 2+ TN 168 732 38 58 4, 8 % 2, 8 % 3, 8 % 8, 6 % 33, 3 % NR NR 44, 4 % Sous-type n TN RH+ TN TN HER 2+ Nanda et al. , JCO 2016 ; Rugo et al. , CCR 2018 ; Dirix et al. , BCRT 2017 ; Loi et al. , SABCS 2017 ; Emens et al. , JAMA Onc 2018 ; Adams et al. , Ann Onc 2018. *Les études ont utilisé différents anticorps et seuils de positivité de PD-L 1 La Lettre du Cancérologue SABCS 2018 - D’après Nanda R et al. , Spotlight session 5
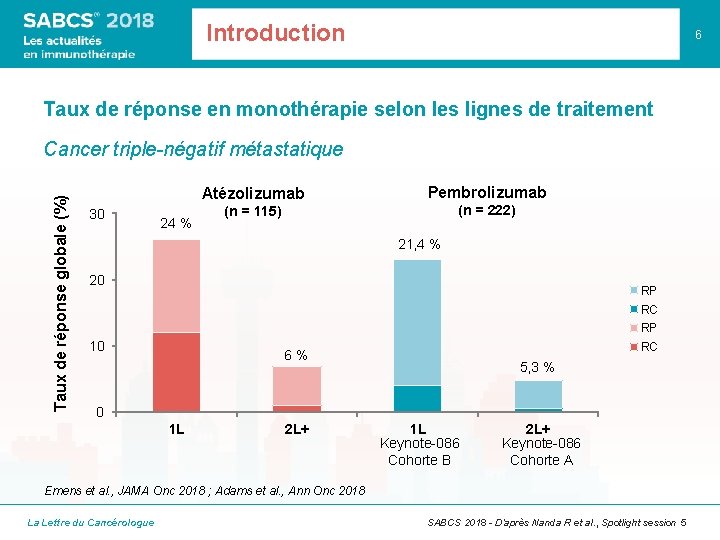
Introduction 6 Taux de réponse en monothérapie selon les lignes de traitement Taux de réponse globale (%) Cancer triple-négatif métastatique 30 24 % Atézolizumab Pembrolizumab (n = 115) (n = 222) 21, 4 % 20 RP RC RP 10 RC 6% 5, 3 % 0 1 L 2 L+ 1 L Keynote-086 Cohorte B 2 L+ Keynote-086 Cohorte A Emens et al. , JAMA Onc 2018 ; Adams et al. , Ann Onc 2018 La Lettre du Cancérologue SABCS 2018 - D’après Nanda R et al. , Spotlight session 5

Chapitre II Immunothérapie en association Céline Rouger (Villejuif) La Lettre du Cancérologue
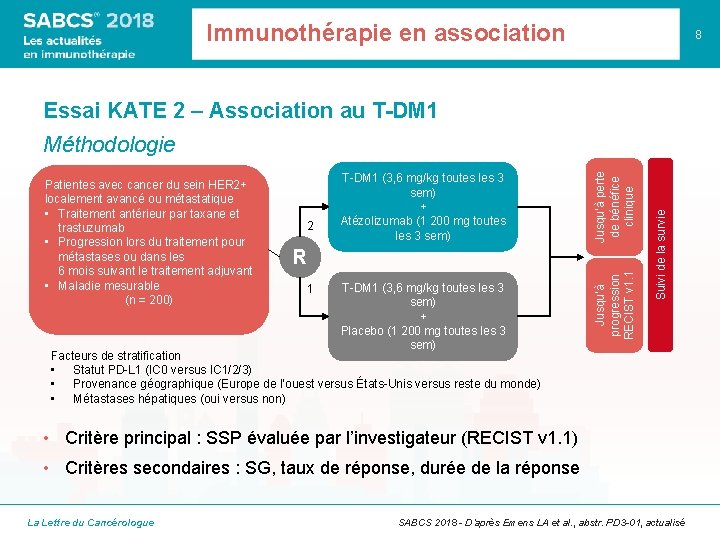
Immunothérapie en association 8 Essai KATE 2 – Association au T-DM 1 R 1 T-DM 1 (3, 6 mg/kg toutes les 3 sem) + Placebo (1 200 mg toutes les 3 sem) Suivi de la survie 2 T-DM 1 (3, 6 mg/kg toutes les 3 sem) + Atézolizumab (1 200 mg toutes les 3 sem) Jusqu’à progression RECIST v 1. 1 Patientes avec cancer du sein HER 2+ localement avancé ou métastatique • Traitement antérieur par taxane et trastuzumab • Progression lors du traitement pour métastases ou dans les 6 mois suivant le traitement adjuvant • Maladie mesurable (n = 200) Jusqu’à perte de bénéfice clinique Méthodologie Facteurs de stratification • Statut PD-L 1 (IC 0 versus IC 1/2/3) • Provenance géographique (Europe de l’ouest versus États-Unis versus reste du monde) • Métastases hépatiques (oui versus non) • Critère principal : SSP évaluée par l’investigateur (RECIST v 1. 1) • Critères secondaires : SG, taux de réponse, durée de la réponse La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. PD 3 -01, actualisé
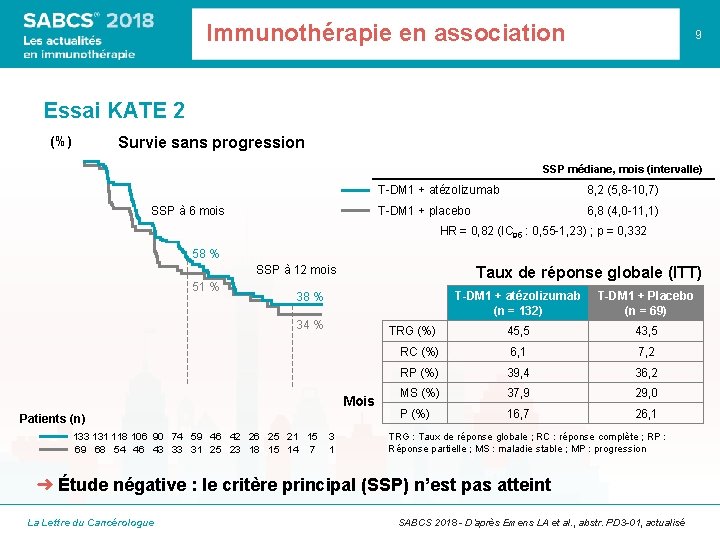
Immunothérapie en association 9 Essai KATE 2 (%) Survie sans progression SSP médiane, mois (intervalle) SSP à 6 mois T-DM 1 + atézolizumab 8, 2 (5, 8 -10, 7) T-DM 1 + placebo 6, 8 (4, 0 -11, 1) HR = 0, 82 (IC 95 : 0, 55 -1, 23) ; p = 0, 332 58 % SSP à 12 mois 51 % Taux de réponse globale (ITT) T-DM 1 + atézolizumab (n = 132) T-DM 1 + Placebo (n = 69) TRG (%) 45, 5 43, 5 RC (%) 6, 1 7, 2 RP (%) 39, 4 36, 2 MS (%) 37, 9 29, 0 P (%) 16, 7 26, 1 38 % 34 % Mois Patients (n) 133 131 118 106 90 74 59 46 42 26 25 21 15 69 68 54 46 43 33 31 25 23 18 15 14 7 3 1 TRG : Taux de réponse globale ; RC : réponse complète ; RP : Réponse partielle ; MS : maladie stable ; MP : progression ➜ Étude négative : le critère principal (SSP) n’est pas atteint La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. PD 3 -01, actualisé
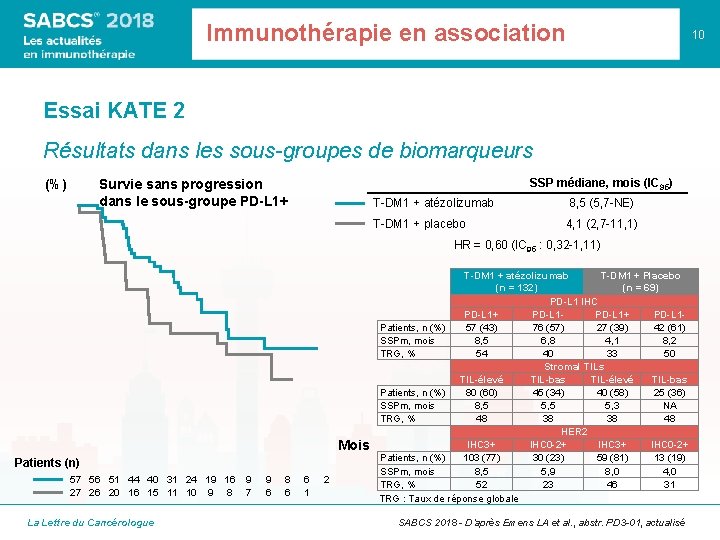
Immunothérapie en association 10 Essai KATE 2 Résultats dans les sous-groupes de biomarqueurs (%) SSP médiane, mois (IC 95) Survie sans progression dans le sous-groupe PD-L 1+ T-DM 1 + atézolizumab 8, 5 (5, 7 -NE) T-DM 1 + placebo 4, 1 (2, 7 -11, 1) HR = 0, 60 (IC 95 : 0, 32 -1, 11) Mois Patients (n) 57 56 51 44 40 31 24 19 16 27 26 20 16 15 11 10 9 8 La Lettre du Cancérologue 9 7 9 6 8 6 6 1 2 T-DM 1 + atézolizumab T-DM 1 + Placebo (n = 132) (n = 69) PD-L 1 IHC PD-L 1+ PD-L 1 Patients, n (%) 57 (43) 76 (57) 27 (39) 42 (61) SSPm, mois 8, 5 6, 8 4, 1 8, 2 TRG, % 54 40 33 50 Stromal TILs TIL-élevé TIL-bas Patients, n (%) 80 (60) 45 (34) 40 (58) 25 (36) SSPm, mois 8, 5 5, 3 NA TRG, % 48 38 38 48 HER 2 IHC 3+ IHC 0 -2+ Patients, n (%) 103 (77) 30 (23) 59 (81) 13 (19) SSPm, mois 8, 5 5, 9 8, 0 4, 0 TRG, % 52 23 46 31 TRG : Taux de réponse globale SABCS 2018 - D’après Emens LA et al. , abstr. PD 3 -01, actualisé

Immunothérapie en association Essai KATE 2 Conclusions • L'ajout de l'atézolizumab au T-DM 1 n'a pas démontré de bénéfice sur la SSP dans la population en ITT chez les patientes HER 2 3+ (SSP de 8, 5 versus 8, 0 mois). Une analyse ultérieure de la SG est prévue au protocole. • L’analyse exploratoire des biomarqueurs montre des résultats intéressants sur la SSP dans la population PD-L 1+ (PD-L 1 IC ≥ 1 %) ou avec un nombre élevé de TIL (Tumor Infiltrating Lymphocytes). • Le taux de toxicité de grade 3 à 5 était similaire entre les 2 bras. • Cependant un taux d’effets secondaires amenant à arrêter le traitement était plus important dans le bras atézolizumab conduisant également à des réduction de doses de T-DM 1. La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. PD 3 -01, actualisé 11

Immunothérapie en association Essai TOPACIO – Association avec inhibiteur de PARP Méthodologie Dose recommandée de phase II Niraparib 200 mg + pembrolizumab 200 mg Phase 2 Critères d’évaluation Critère principal Taux de réponse globale selon RECIST 1. 1 Critères secondaires Survie sans progression (SSP) Durée de la réponse (DDR) Critères exploratoires Identification de biomarqueurs La Lettre du Cancérologue SABCS 2018 - D’après Vinayak S et al. , abstr. PD 5 -02, actualisé 12
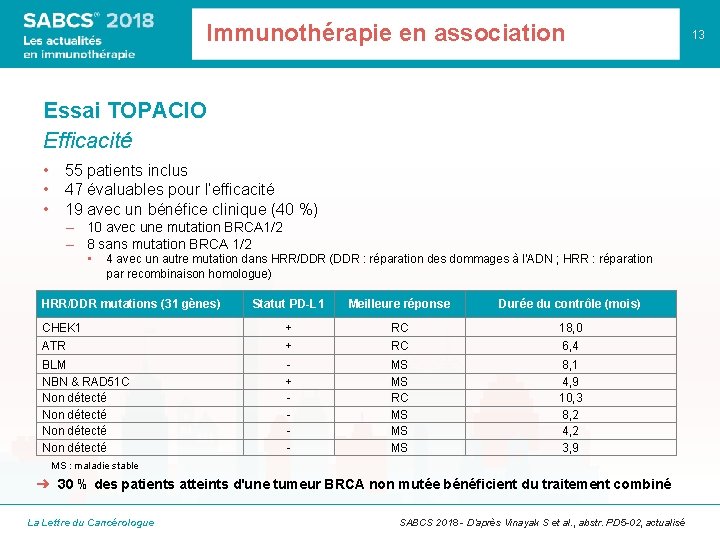
Immunothérapie en association Essai TOPACIO Efficacité • 55 patients inclus • 47 évaluables pour l’efficacité • 19 avec un bénéfice clinique (40 %) – 10 avec une mutation BRCA 1/2 – 8 sans mutation BRCA 1/2 • 4 avec un autre mutation dans HRR/DDR (DDR : réparation des dommages à l’ADN ; HRR : réparation par recombinaison homologue) HRR/DDR mutations (31 gènes) Statut PD-L 1 Meilleure réponse Durée du contrôle (mois) CHEK 1 + RC 18, 0 ATR + RC 6, 4 BLM NBN & RAD 51 C Non détecté + - MS MS RC MS MS MS 8, 1 4, 9 10, 3 8, 2 4, 2 3, 9 MS : maladie stable ➜ 30 % des patients atteints d'une tumeur BRCA non mutée bénéficient du traitement combiné La Lettre du Cancérologue SABCS 2018 - D’après Vinayak S et al. , abstr. PD 5 -02, actualisé 13
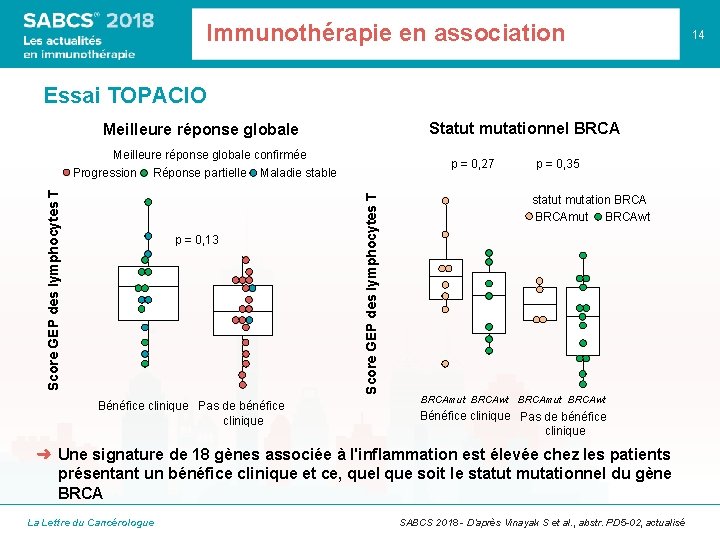
Immunothérapie en association Essai TOPACIO Statut mutationnel BRCA Meilleure réponse globale p = 0, 13 Bénéfice clinique Pas de bénéfice clinique p = 0, 27 Score GEP des lymphocytes T Meilleure réponse globale confirmée Progression Réponse partielle Maladie stable p = 0, 35 statut mutation BRCAmut BRCAwt Bénéfice clinique Pas de bénéfice clinique ➜ Une signature de 18 gènes associée à l'inflammation est élevée chez les patients présentant un bénéfice clinique et ce, quel que soit le statut mutationnel du gène BRCA La Lettre du Cancérologue SABCS 2018 - D’après Vinayak S et al. , abstr. PD 5 -02, actualisé 14
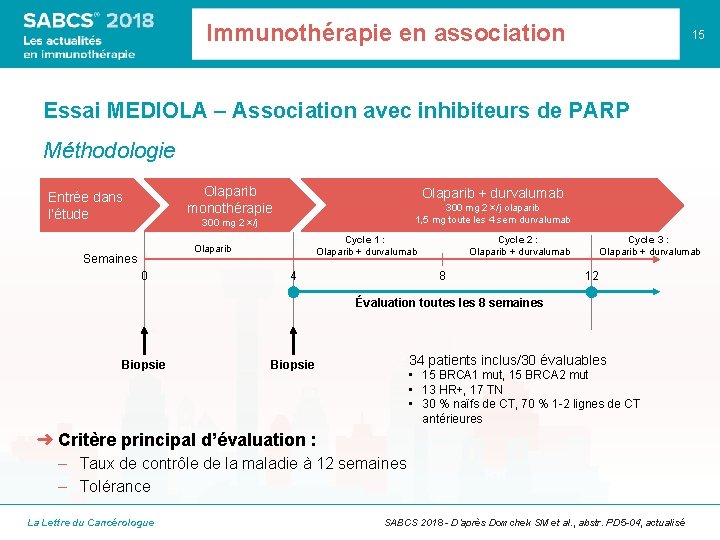
Immunothérapie en association 15 Essai MEDIOLA – Association avec inhibiteurs de PARP Méthodologie Olaparib monothérapie Entrée dans l’étude Olaparib + durvalumab 300 mg 2 ×/j olaparib 1, 5 mg toute les 4 sem durvalumab 300 mg 2 ×/j Cycle 1 : Olaparib + durvalumab Olaparib Semaines 0 4 Cycle 2 : Olaparib + durvalumab 8 Cycle 3 : Olaparib + durvalumab 12 Évaluation toutes les 8 semaines Biopsie 34 patients inclus/30 évaluables Biopsie • 15 BRCA 1 mut, 15 BRCA 2 mut • 13 HR+, 17 TN • 30 % naïfs de CT, 70 % 1 -2 lignes de CT antérieures ➜ Critère principal d’évaluation : – Taux de contrôle de la maladie à 12 semaines – Tolérance La Lettre du Cancérologue SABCS 2018 - D’après Domchek SM et al. , abstr. PD 5 -04, actualisé
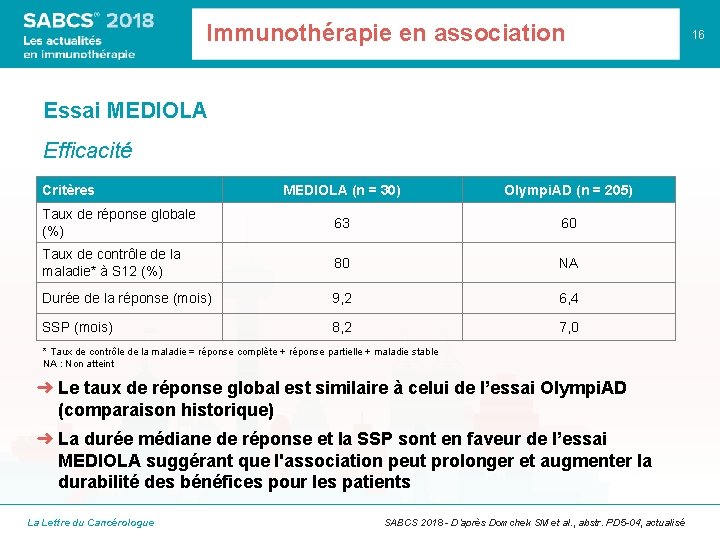
Immunothérapie en association Essai MEDIOLA Efficacité Critères MEDIOLA (n = 30) Olympi. AD (n = 205) Taux de réponse globale (%) 63 60 Taux de contrôle de la maladie* à S 12 (%) 80 NA Durée de la réponse (mois) 9, 2 6, 4 SSP (mois) 8, 2 7, 0 * Taux de contrôle de la maladie = réponse complète + réponse partielle + maladie stable NA : Non atteint ➜ Le taux de réponse global est similaire à celui de l’essai Olympi. AD (comparaison historique) ➜ La durée médiane de réponse et la SSP sont en faveur de l’essai MEDIOLA suggérant que l'association peut prolonger et augmenter la durabilité des bénéfices pour les patients La Lettre du Cancérologue SABCS 2018 - D’après Domchek SM et al. , abstr. PD 5 -04, actualisé 16
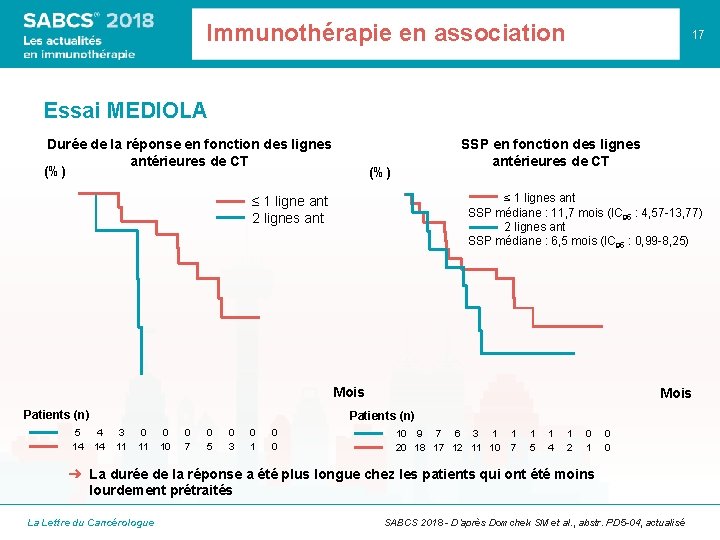
Immunothérapie en association 17 Essai MEDIOLA Durée de la réponse en fonction des lignes antérieures de CT (%) SSP en fonction des lignes antérieures de CT (%) ≤ 1 lignes ant SSP médiane : 11, 7 mois (IC 95 : 4, 57 -13, 77) 2 lignes ant SSP médiane : 6, 5 mois (IC 95 : 0, 99 -8, 25) ≤ 1 ligne ant 2 lignes ant Mois Patients (n) 5 14 Mois Patients (n) 4 14 3 11 0 10 0 7 0 5 0 3 0 1 0 0 10 9 7 6 3 1 20 18 17 12 11 10 1 7 1 5 1 4 1 2 0 1 0 0 ➜ La durée de la réponse a été plus longue chez les patients qui ont été moins lourdement prétraités La Lettre du Cancérologue SABCS 2018 - D’après Domchek SM et al. , abstr. PD 5 -04, actualisé
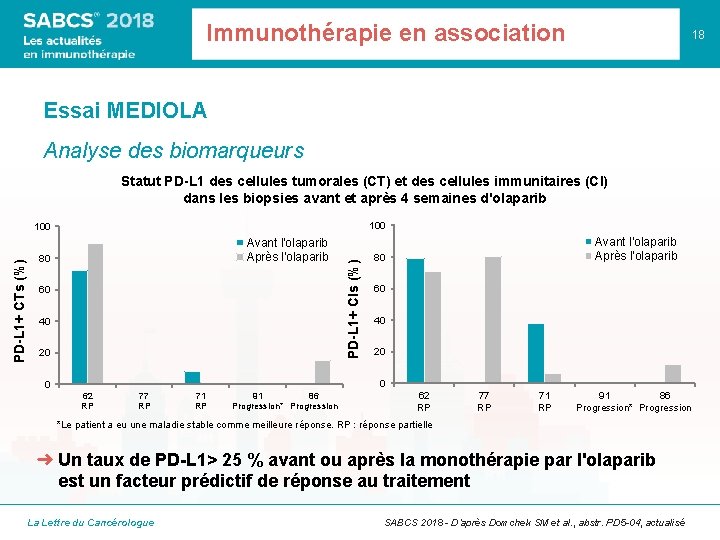
Immunothérapie en association 18 Essai MEDIOLA Analyse des biomarqueurs Statut PD-L 1 des cellules tumorales (CT) et des cellules immunitaires (CI) dans les biopsies avant et après 4 semaines d'olaparib 100 Avant l'olaparib Après l'olaparib 80 60 40 20 PD-L 1+ CIs (%) PD-L 1+ CTs (%) 100 Avant l'olaparib Après l'olaparib 80 60 40 20 0 0 62 RP 77 RP 71 RP 91 86 Progression* Progression *Le patient a eu une maladie stable comme meilleure réponse. RP : réponse partielle ➜ Un taux de PD-L 1> 25 % avant ou après la monothérapie par l'olaparib est un facteur prédictif de réponse au traitement La Lettre du Cancérologue SABCS 2018 - D’après Domchek SM et al. , abstr. PD 5 -04, actualisé

Immunothérapie en association 19 Essai KEYNOTE-173 – Association avec la chimiothérapie Méthodologie Biopsie Cycle 1 2 3 4 5 6 Nab-paclitaxel 125 mg/m² i. v. jours 1, 8 et 15 toutes les 3 sem Cohorte A IRM 7 8 9 Doxorubicine 60 mg/m² jour 1 toutes les 3 sem Cyclophosphamide 600 mg/m² j 1 toutes les 3 sem Pembrolizumab 200 mg i. v. jour 1 toutes les 3 sem Cohorte B Nab-paclitaxel 100 mg/m² i. v. jours 1, 8 et 15 toutes les 3 sem Carboplatine dose de départ ASC 6 jour 1 toutes les 3 sem Doxorubicine 60 mg/m² jour 1 toutes les 3 sem Cyclophosphamide 600 mg/m² j 1 toutes les 3 sem Cohorte C Nab-paclitaxel 125 mg/m² i. v. jours 1, 8 et 15 toutes les 3 sem Carboplatine dose de départ ASC 5 jour 1 toutes les 3 sem Doxorubicine 60 mg/m² jour 1 toutes les 3 sem Cyclophosphamide 600 mg/m² j 1 toutes les 3 sem Pembrolizumab 200 mg i. v. jour 1 toutes les 3 sem Cohorte D Nab-paclitaxel 125 mg/m² i. v. jours 1, 8 et 15 toutes les 3 sem Carboplatine dose de départ ASC 2 jours 1, 8 et 15 toutes les 3 sem Doxorubicine 60 mg/m² jour 1 toutes les 3 sem Cyclophosphamide 600 mg/m² j 1 toutes les 3 sem 3 -6 semaines Sélection ~28 jours Pembrolizumab 200 mg i. v. jour 1 toutes les 3 sem Cohorte E Paclitaxel 80 mg/m² i. v. jours 1, 8 et 15 toutes les 3 sem Carboplatine dose de départ ASC 5 jour 1 toutes les 3 sem Doxorubicine 60 mg/m² jour 1 toutes les 3 sem Cyclophosphamide 600 mg/m² j 1 toutes les 3 sem Pembrolizumab 200 mg i. v. jour 1 toutes les 3 sem Cohorte F Paclitaxel 80 mg/m² i. v. jours 1, 8 et 15 toutes les 3 sem Carboplatine dose de départ ASC 2 jours 1, 8 et 15 toutes les 3 sem Doxorubicine 60 mg/m² jour 1 toutes les 3 sem Cyclophosphamide 600 mg/m² j 1 toutes les 3 sem Pembrolizumab 200 mg i. v. jour 1 toutes les 3 sem ASC : aire sous la courbe (AUC La Lettre du Cancérologue ) SABCS 2018 - D’après Schmid P et al. , abstr. PD 5 -01, actualisé
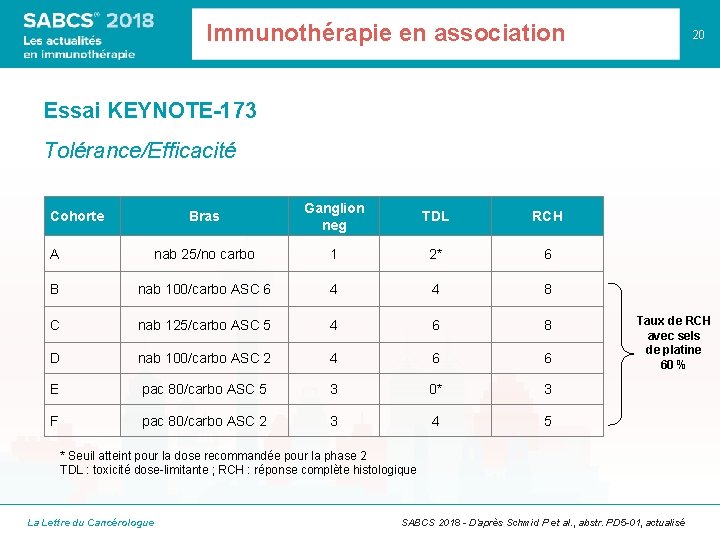
Immunothérapie en association 20 Essai KEYNOTE-173 Tolérance/Efficacité Bras Ganglion neg TDL RCH A nab 25/no carbo 1 2* 6 B nab 100/carbo ASC 6 4 4 8 C nab 125/carbo ASC 5 4 6 8 D nab 100/carbo ASC 2 4 6 6 E pac 80/carbo ASC 5 3 0* 3 F pac 80/carbo ASC 2 3 4 5 Cohorte Taux de RCH avec sels de platine 60 % * Seuil atteint pour la dose recommandée pour la phase 2 TDL : toxicité dose-limitante ; RCH : réponse complète histologique La Lettre du Cancérologue SABCS 2018 - D’après Schmid P et al. , abstr. PD 5 -01, actualisé
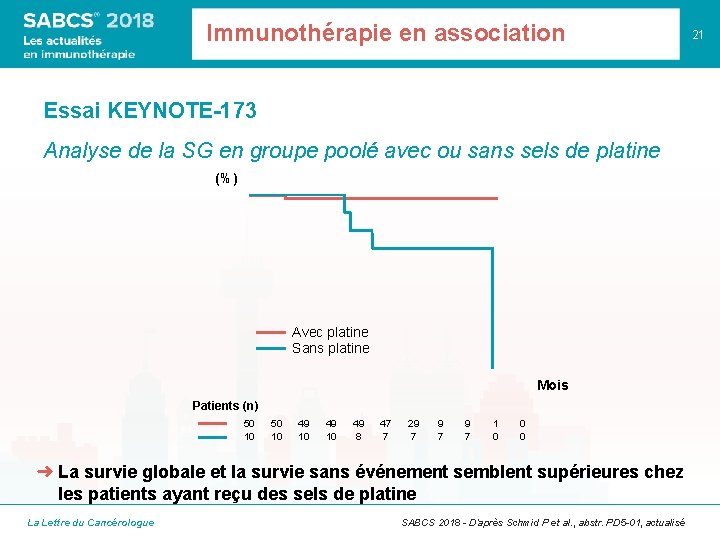
Immunothérapie en association Essai KEYNOTE-173 Analyse de la SG en groupe poolé avec ou sans sels de platine (%) Avec platine Sans platine Mois Patients (n) 50 10 49 8 47 7 29 7 9 7 1 0 0 0 ➜ La survie globale et la survie sans événement semblent supérieures chez les patients ayant reçu des sels de platine La Lettre du Cancérologue SABCS 2018 - D’après Schmid P et al. , abstr. PD 5 -01, actualisé 21
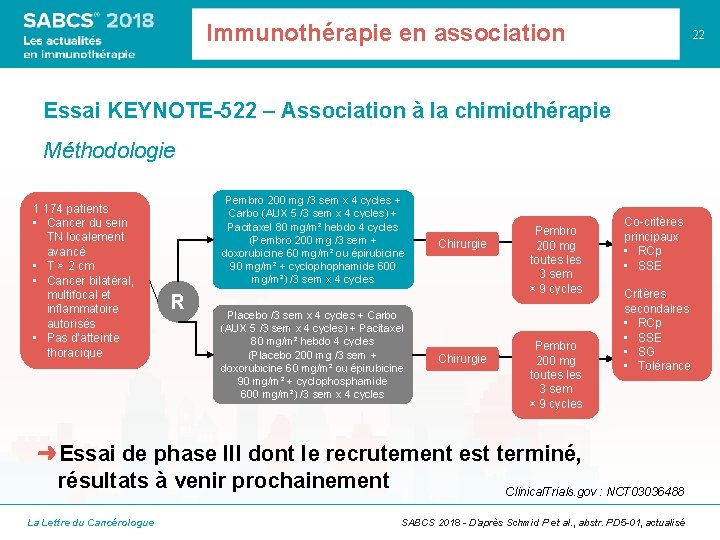
Immunothérapie en association 22 Essai KEYNOTE-522 – Association à la chimiothérapie Méthodologie 1 174 patients • Cancer du sein TN localement avancé • T > 2 cm • Cancer bilatéral, multifocal et inflammatoire autorisés • Pas d’atteinte thoracique Pembro 200 mg /3 sem x 4 cycles + Carbo (AUX 5 /3 sem x 4 cycles) + Pacitaxel 80 mg/m² hebdo 4 cycles (Pembro 200 mg /3 sem + doxorubicine 60 mg/m² ou épirubicine 90 mg/m² + cyclophophamide 600 mg/m²) /3 sem x 4 cycles R Placebo /3 sem x 4 cycles + Carbo (AUX 5 /3 sem x 4 cycles) + Pacitaxel 80 mg/m² hebdo 4 cycles (Placebo 200 mg /3 sem + doxorubicine 60 mg/m² ou épirubicine 90 mg/m² + cyclophosphamide 600 mg/m²) /3 sem x 4 cycles Chirurgie Pembro 200 mg toutes les 3 sem × 9 cycles Co-critères principaux • RCp • SSE Critères secondaires • RCp • SSE • SG • Tolérance ➜Essai de phase III dont le recrutement est terminé, résultats à venir prochainement Clinical. Trials. gov : NCT 03036488 La Lettre du Cancérologue SABCS 2018 - D’après Schmid P et al. , abstr. PD 5 -01, actualisé
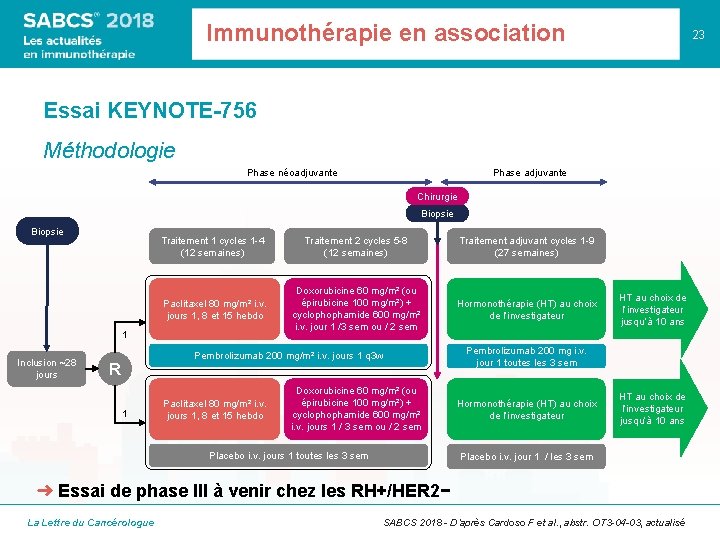
Immunothérapie en association 23 Essai KEYNOTE-756 Méthodologie Phase néoadjuvante Phase adjuvante Chirurgie Biopsie Traitement 1 cycles 1 -4 (12 semaines) Traitement 2 cycles 5 -8 (12 semaines) Traitement adjuvant cycles 1 -9 (27 semaines) Paclitaxel 80 mg/m² i. v. jours 1, 8 et 15 hebdo Doxorubicine 60 mg/m² (ou épirubicine 100 mg/m²) + cyclophophamide 600 mg/m² i. v. jour 1 /3 sem ou / 2 sem Hormonothérapie (HT) au choix de l’investigateur 1 Inclusion ~28 jours Pembrolizumab 200 mg/m² i. v. jours 1 q 3 w R 1 Paclitaxel 80 mg/m² i. v. jours 1, 8 et 15 hebdo Doxorubicine 60 mg/m² (ou épirubicine 100 mg/m²) + cyclophophamide 600 mg/m² i. v. jours 1 / 3 sem ou / 2 sem Placebo i. v. jours 1 toutes les 3 sem HT au choix de l’investigateur jusqu’à 10 ans Pembrolizumab 200 mg i. v. jour 1 toutes les 3 sem Hormonothérapie (HT) au choix de l’investigateur HT au choix de l’investigateur jusqu’à 10 ans Placebo i. v. jour 1 / les 3 sem ➜ Essai de phase III à venir chez les RH+/HER 2− La Lettre du Cancérologue SABCS 2018 - D’après Cardoso F et al. , abstr. OT 3 -04 -03, actualisé

Chapitre III Facteurs prédictifs de réponse Céline Rouger (Villejuif) La Lettre du Cancérologue
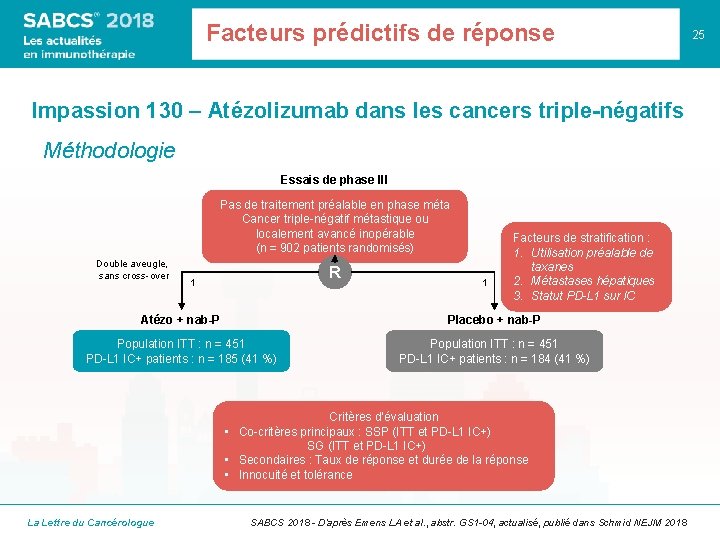
Facteurs prédictifs de réponse Impassion 130 – Atézolizumab dans les cancers triple-négatifs Méthodologie Essais de phase III Pas de traitement préalable en phase méta Cancer triple-négatif métastique ou localement avancé inopérable (n = 902 patients randomisés) Double aveugle, sans cross-over R 1 1 Facteurs de stratification : 1. Utilisation préalable de taxanes 2. Métastases hépatiques 3. Statut PD-L 1 sur IC Atézo + nab-P Placebo + nab-P Population ITT : n = 451 PD-L 1 IC+ patients : n = 185 (41 %) Population ITT : n = 451 PD-L 1 IC+ patients : n = 184 (41 %) Critères d’évaluation • Co-critères principaux : SSP (ITT et PD-L 1 IC+) SG (ITT et PD-L 1 IC+) • Secondaires : Taux de réponse et durée de la réponse • Innocuité et tolérance La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé, publié dans Schmid NEJM 2018 25
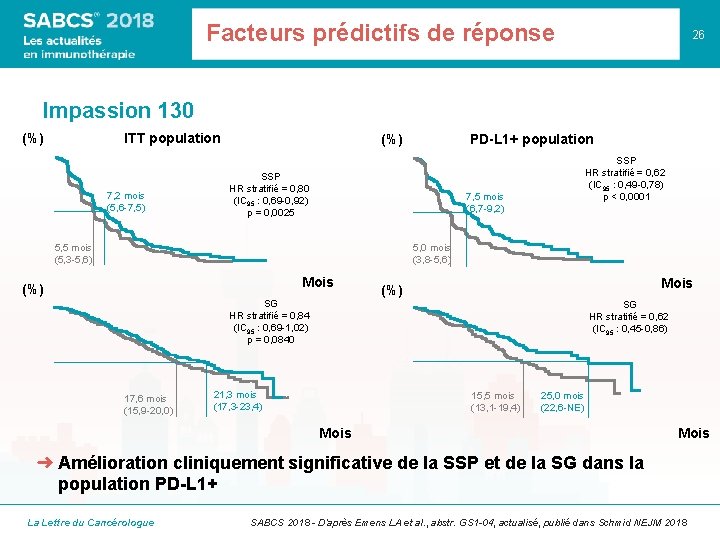
Facteurs prédictifs de réponse 26 Impassion 130 (%) ITT population 7, 2 mois (5, 6 -7, 5) (%) PD-L 1+ population SSP HR stratifié = 0, 80 (IC 95 : 0, 69 -0, 92) p = 0, 0025 SSP HR stratifié = 0, 62 (IC 95 : 0, 49 -0, 78) p < 0, 0001 7, 5 mois (6, 7 -9, 2) 5, 5 mois (5, 3 -5, 6) 5, 0 mois (3, 8 -5, 6) Mois (%) SG HR stratifié = 0, 84 (IC 95 : 0, 69 -1, 02) p = 0, 0840 17, 6 mois (15, 9 -20, 0) SG HR stratifié = 0, 62 (IC 95 : 0, 45 -0, 86) 21, 3 mois (17, 3 -23, 4) 15, 5 mois (13, 1 -19, 4) 25, 0 mois (22, 6 -NE) Mois ➜ Amélioration cliniquement significative de la SSP et de la SG dans la population PD-L 1+ La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé, publié dans Schmid NEJM 2018
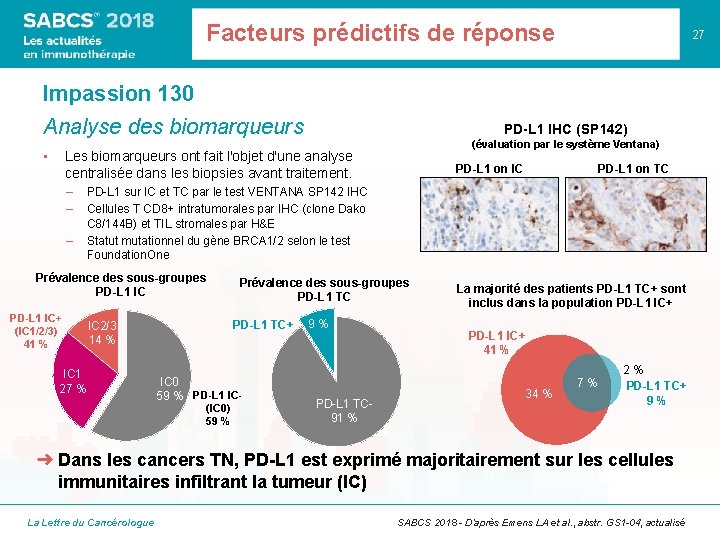
Facteurs prédictifs de réponse 27 Impassion 130 Analyse des biomarqueurs • PD-L 1 IHC (SP 142) (évaluation par le système Ventana) Les biomarqueurs ont fait l'objet d'une analyse centralisée dans les biopsies avant traitement. – – – PD-L 1 on TC PD-L 1 sur IC et TC par le test VENTANA SP 142 IHC Cellules T CD 8+ intratumorales par IHC (clone Dako C 8/144 B) et TIL stromales par H&E Statut mutationnel du gène BRCA 1/2 selon le test Foundation. One Prévalence des sous-groupes PD-L 1 IC+ (IC 1/2/3) 41 % PD-L 1 on IC PD-L 1 TC+ IC 2/3 14 % IC 1 27 % Prévalence des sous-groupes PD-L 1 TC IC 0 59 % PD-L 1 IC(IC 0) 59 % 9% PD-L 1 TC 91 % La majorité des patients PD-L 1 TC+ sont inclus dans la population PD-L 1 IC+ 41 % 34 % 7% 2% PD-L 1 TC+ 9% ➜ Dans les cancers TN, PD-L 1 est exprimé majoritairement sur les cellules immunitaires infiltrant la tumeur (IC) La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé
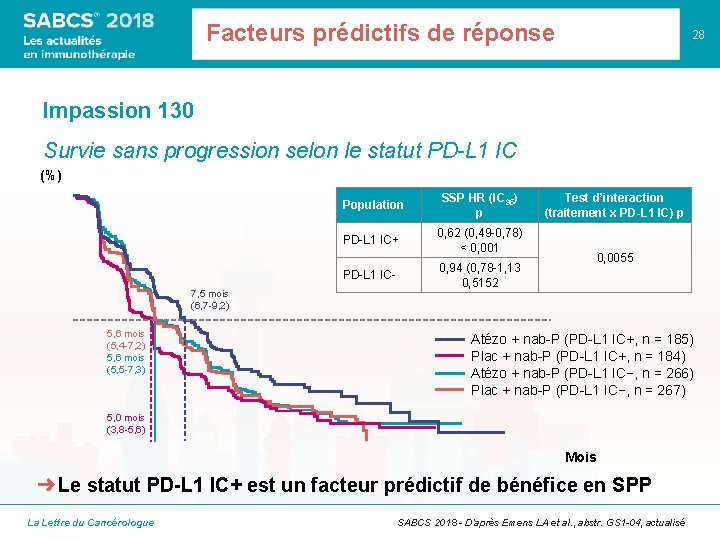
Facteurs prédictifs de réponse 28 Impassion 130 Survie sans progression selon le statut PD-L 1 IC (%) 7, 5 mois (6, 7 -9, 2) 5, 6 mois (5, 4 -7, 2) 5, 6 mois (5, 5 -7, 3) Population SSP HR (IC 95) p PD-L 1 IC+ 0, 62 (0, 49 -0, 78) < 0, 001 PD-L 1 IC- 0, 94 (0, 78 -1, 13 0, 5152 Test d’interaction (traitement x PD-L 1 IC) p 0, 0055 Atézo + nab-P (PD-L 1 IC+, n = 185) Plac + nab-P (PD-L 1 IC+, n = 184) Atézo + nab-P (PD-L 1 IC−, n = 266) Plac + nab-P (PD-L 1 IC−, n = 267) 5, 0 mois (3, 8 -5, 6) Mois ➜ Le statut PD-L 1 IC+ est un facteur prédictif de bénéfice en SPP La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé
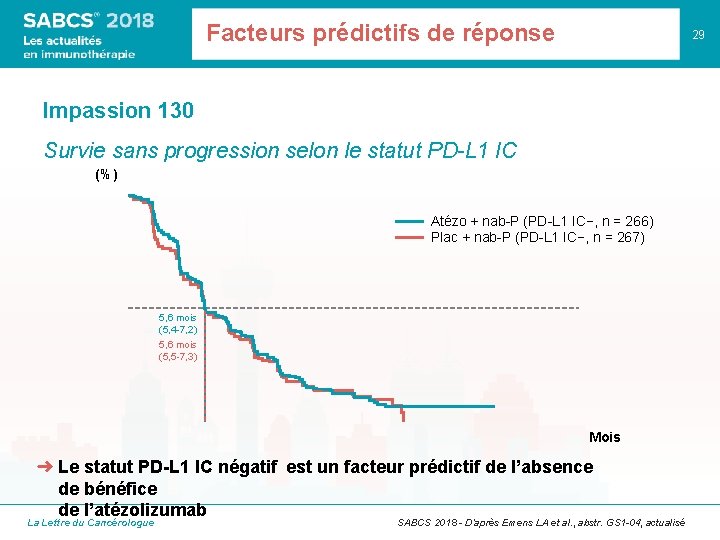
Facteurs prédictifs de réponse 29 Impassion 130 Survie sans progression selon le statut PD-L 1 IC (%) Atézo + nab-P (PD-L 1 IC−, n = 266) Plac + nab-P (PD-L 1 IC−, n = 267) 5, 6 mois (5, 4 -7, 2) 5, 6 mois (5, 5 -7, 3) Mois ➜ Le statut PD-L 1 IC négatif est un facteur prédictif de l’absence de bénéfice de l’atézolizumab La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé
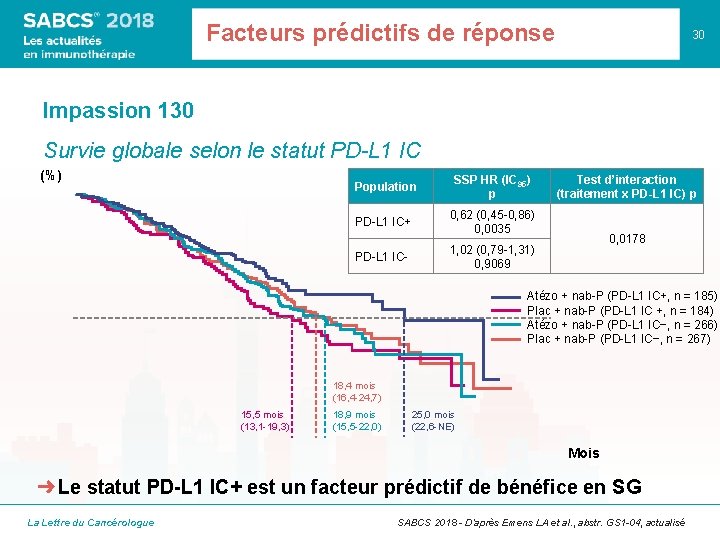
Facteurs prédictifs de réponse 30 Impassion 130 Survie globale selon le statut PD-L 1 IC (%) Population SSP HR (IC 95) p PD-L 1 IC+ 0, 62 (0, 45 -0, 86) 0, 0035 PD-L 1 IC- 1, 02 (0, 79 -1, 31) 0, 9069 Test d’interaction (traitement x PD-L 1 IC) p 0, 0178 Atézo + nab-P (PD-L 1 IC+, n = 185) Plac + nab-P (PD-L 1 IC +, n = 184) Atézo + nab-P (PD-L 1 IC−, n = 266) Plac + nab-P (PD-L 1 IC−, n = 267) 18, 4 mois (16, 4 -24, 7) 15, 5 mois (13, 1 -19, 3) 18, 9 mois (15, 5 -22, 0) 25, 0 mois (22, 6 -NE) Mois ➜ Le statut PD-L 1 IC+ est un facteur prédictif de bénéfice en SG La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé

Facteurs prédictifs de réponse 31 Impassion 130 Analyse des biomarqueurs PD-L 1 IC+ 44 % CD 8 -/PD-L 1 IC+ (n = 37) HR (IC 95) p SSP 0, 33 (0, 13 -0, 87) 0, 03 SG 0, 25 (0, 06 -1, 02) 0, 05 5% CD 8+ 69 % 31 % 39 % CD 8+/PD-L 1 IC- (n = 220) HR (IC 95) p SSP 0, 89 (0, 66 -1, 20) 0, 45 OS 0, 77 (0, 50 -1, 17) 0, 21 CD 8+/PD-L 1 IC+ (n = 280) HR (IC 95) p SSP 0, 61 (0, 46 -0, 80) ≤ 0, 005 SG 0, 55 (0, 38 -0, 80) ≤ 0, 005 ➜ Les patients CD 8+ bénéficient de l’atézolizumab uniquement si leur tumeur est aussi PD-L 1 positive La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé
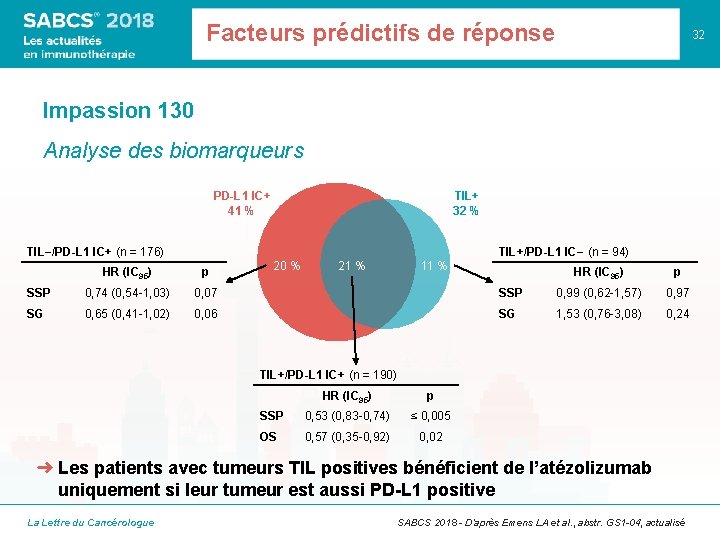
Facteurs prédictifs de réponse 32 Impassion 130 Analyse des biomarqueurs PD-L 1 IC+ 41 % TIL+ 32 % TIL−/PD-L 1 IC+ (n = 176) TIL+/PD-L 1 IC− (n = 94) HR (IC 95) p SSP 0, 74 (0, 54 -1, 03) 0, 07 SG 0, 65 (0, 41 -1, 02) 0, 06 20 % 21 % 11 % HR (IC 95) p SSP 0, 99 (0, 62 -1, 57) 0, 97 SG 1, 53 (0, 76 -3, 08) 0, 24 TIL+/PD-L 1 IC+ (n = 190) HR (IC 95) p SSP 0, 53 (0, 83 -0, 74) ≤ 0, 005 OS 0, 57 (0, 35 -0, 92) 0, 02 ➜ Les patients avec tumeurs TIL positives bénéficient de l’atézolizumab uniquement si leur tumeur est aussi PD-L 1 positive La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé

Facteurs prédictifs de réponse Impassion 130 Conclusions • L’expression de PD-L 1 sur les cellules immunitaires est un biomarqueur prédictif de bénéfice clinique pour l’atézolizumab + nab-paclitaxel en première ligne. • Il n’y a pas de bénéfice supplémentaire retrouvé chez les patientes exprimant PD-L 1 sur les cellules tumorales. • Le statut TIL positif ou CD 8 positif n’a de valeur que si la tumeur était aussi PD-L 1 positive. • Le bénéfice en SG et SSP est retrouvé quel que soit le statut BRCA • Les patientes avec un cancer TN métastatique ou localement avancé devraient être testées pour leur statut PD-L 1 IC afin de déterminer si elles peuvent bénéficier ou non d’une immunothérapie La Lettre du Cancérologue SABCS 2018 - D’après Emens LA et al. , abstr. GS 1 -04, actualisé 33
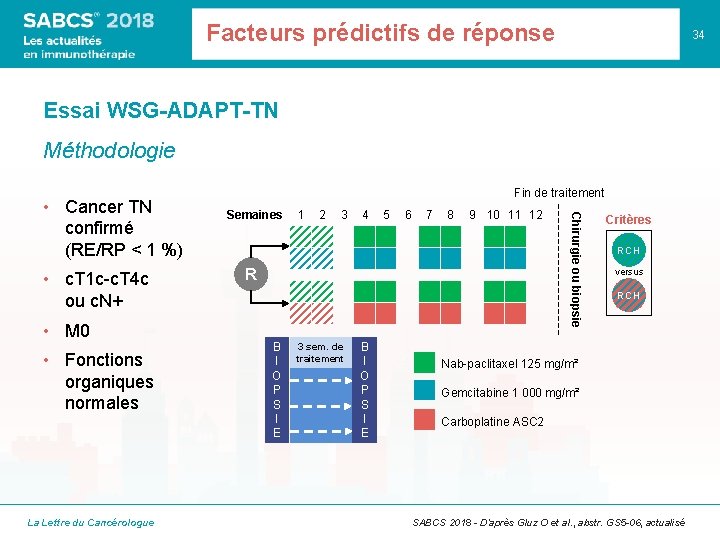
Facteurs prédictifs de réponse 34 Essai WSG-ADAPT-TN Méthodologie • c. T 1 c-c. T 4 c ou c. N+ • M 0 • Fonctions organiques normales La Lettre du Cancérologue Semaines 1 2 3 4 5 6 7 8 9 10 11 12 R B I O P S I E 3 sem. de traitement B I O P S I E Chirurgie ou biopsie • Cancer TN confirmé (RE/RP < 1 %) Fin de traitement Critères RCH versus RCH Nab-paclitaxel 125 mg/m² Gemcitabine 1 000 mg/m² Carboplatine ASC 2 SABCS 2018 - D’après Gluz O et al. , abstr. GS 5 -06, actualisé
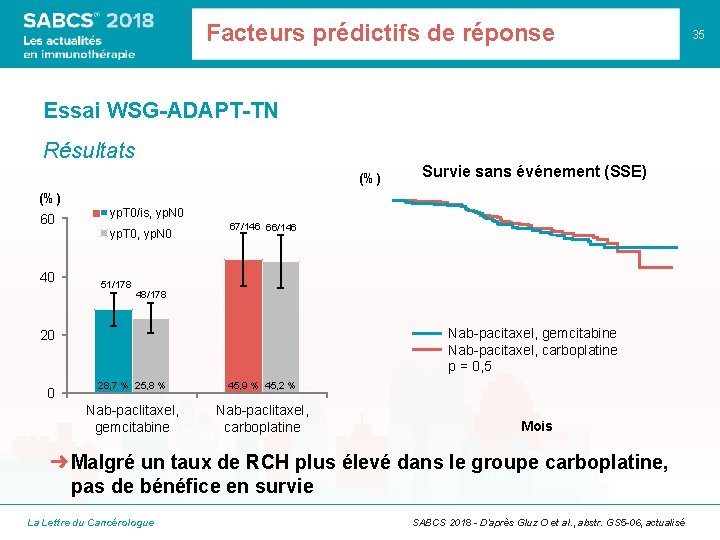
Facteurs prédictifs de réponse Essai WSG-ADAPT-TN Résultats (%) Survie sans événement (SSE) (%) 60 yp. T 0/is, yp. N 0 yp. T 0, yp. N 0 40 51/178 67/146 66/146 48/178 Nab-pacitaxel, gemcitabine Nab-pacitaxel, carboplatine p = 0, 5 20 0 28, 7 % 25, 8 % 45, 9 % 45, 2 % Nab-paclitaxel, gemcitabine Nab-paclitaxel, carboplatine Mois ➜ Malgré un taux de RCH plus élevé dans le groupe carboplatine, pas de bénéfice en survie La Lettre du Cancérologue SABCS 2018 - D’après Gluz O et al. , abstr. GS 5 -06, actualisé 35

Facteurs prédictifs de réponse 36 Essai WSG-ADAPT-TN Effet d’une chimiothérapie adjuvante additionnelle selon le statut PD-1 chez les patients avec une RCH (%) expression PD-1 < médiane (%) 4 x EC Pas de CT p = 0, 05 expression PD-1 ≥ médiane 4 x EC Pas de CT p = NS Mois ➜ Les patientes présentant à la fois une réponse complète et une signature "high immune" (définie ici par PD-1) présentaient une excellente SSE à 3 ans et pourraient être candidates à une désescalade de traitement La Lettre du Cancérologue SABCS 2018 - D’après Gluz O et al. , abstr. GS 5 -06, actualisé
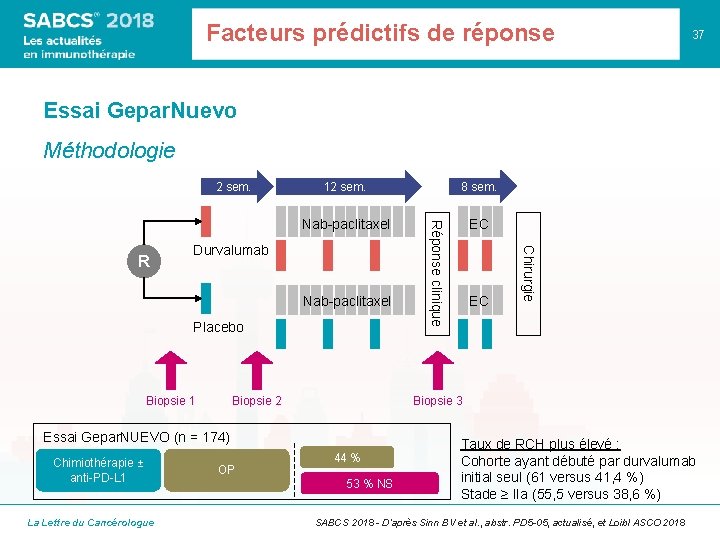
Facteurs prédictifs de réponse 37 Essai Gepar. Nuevo Méthodologie 2 sem. 8 sem. Nab-paclitaxel EC Nab-paclitaxel Placebo Biopsie 1 Biopsie 2 Biopsie 3 Essai Gepar. NUEVO (n = 174) Chimiothérapie ± anti-PD-L 1 La Lettre du Cancérologue OP EC Chirurgie Durvalumab Réponse clinique R 12 sem. 44 % 53 % NS Taux de RCH plus élevé : Cohorte ayant débuté par durvalumab initial seul (61 versus 41, 4 %) Stade ≥ IIa (55, 5 versus 38, 6 %) SABCS 2018 - D’après Sinn BV et al. , abstr. PD 5 -05, actualisé, et Loibl ASCO 2018
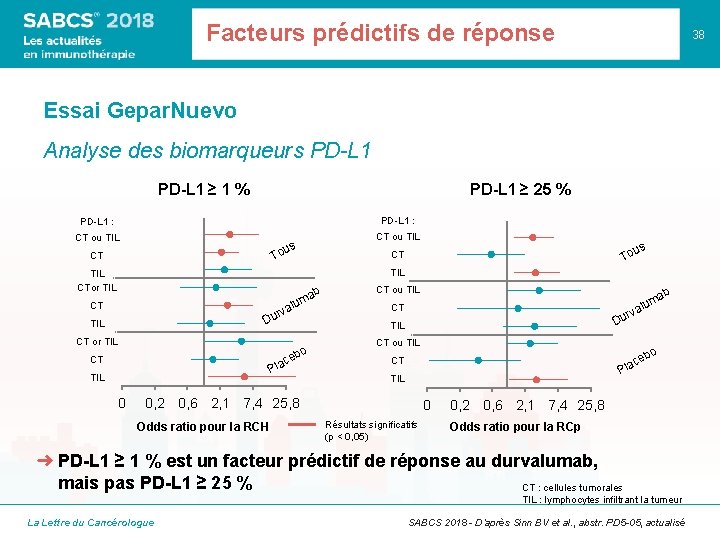
Facteurs prédictifs de réponse 38 Essai Gepar. Nuevo Analyse des biomarqueurs PD-L 1 ≥ 1 % PD-L 1 ≥ 25 % PD-L 1 : CT ou TIL s ou us To CT TIL TIL CTor TIL ab m alu v r u CT D TIL CT or TIL o eb c la CT P TIL 0 CT ou TIL o eb CT c Pla TIL 0, 2 0, 6 2, 1 7, 4 25, 8 Odds ratio pour la RCH b ma u l rva Du CT 0 Résultats significatifs (p < 0, 05) 0, 2 0, 6 2, 1 7, 4 25, 8 Odds ratio pour la RCp ➜ PD-L 1 ≥ 1 % est un facteur prédictif de réponse au durvalumab, mais pas PD-L 1 ≥ 25 % CT : cellules tumorales TIL : lymphocytes infiltrant la tumeur La Lettre du Cancérologue SABCS 2018 - D’après Sinn BV et al. , abstr. PD 5 -05, actualisé
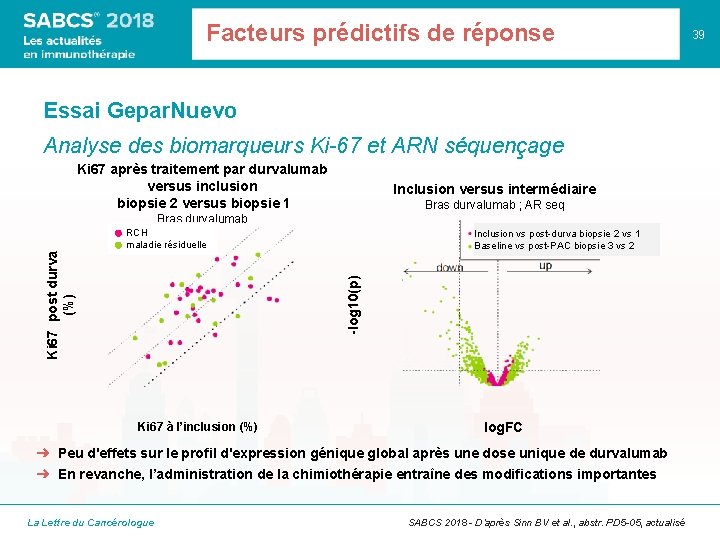
Facteurs prédictifs de réponse Essai Gepar. Nuevo Analyse des biomarqueurs Ki-67 et ARN séquençage Ki 67 après traitement par durvalumab versus inclusion biopsie 2 versus biopsie 1 Inclusion versus intermédiaire Bras durvalumab ; AR seq Bras durvalumab Inclusion vs post-durva biopsie 2 vs 1 Baseline vs post-PAC biopsie 3 vs 2 -log 10(p) Ki 67 post durva (%) RCH maladie résiduelle Ki 67 à l’inclusion (%) log. FC ➜ Peu d'effets sur le profil d'expression génique global après une dose unique de durvalumab ➜ En revanche, l’administration de la chimiothérapie entraîne des modifications importantes La Lettre du Cancérologue SABCS 2018 - D’après Sinn BV et al. , abstr. PD 5 -05, actualisé 39

Chapitre IV Biomarqueurs Céline Rouger (Villejuif) La Lettre du Cancérologue
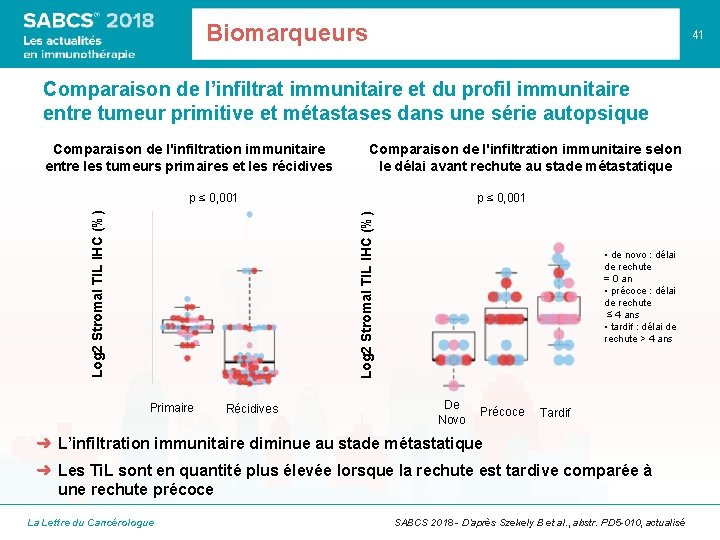
Biomarqueurs 41 Comparaison de l’infiltrat immunitaire et du profil immunitaire entre tumeur primitive et métastases dans une série autopsique Comparaison de l'infiltration immunitaire entre les tumeurs primaires et les récidives Comparaison de l'infiltration immunitaire selon le délai avant rechute au stade métastatique p ≤ 0, 001 Log 2 Stromal TIL IHC (%) p ≤ 0, 001 Primaire Récidives • de novo : délai de rechute = 0 an • précoce : délai de rechute ≤ 4 ans • tardif : délai de rechute > 4 ans De Novo Précoce Tardif ➜ L’infiltration immunitaire diminue au stade métastatique ➜ Les Ti. L sont en quantité plus élevée lorsque la rechute est tardive comparée à une rechute précoce La Lettre du Cancérologue SABCS 2018 - D’après Szekely B et al. , abstr. PD 5 -010, actualisé
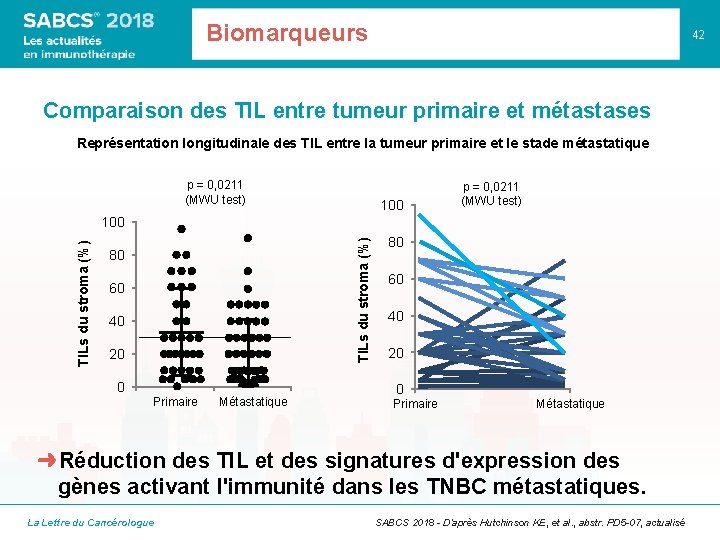
Biomarqueurs 42 Comparaison des TIL entre tumeur primaire et métastases Représentation longitudinale des TIL entre la tumeur primaire et le stade métastatique p = 0, 0211 (MWU test) 100 p = 0, 0211 (MWU test) TILs du stroma (%) 100 80 60 40 20 0 Primaire Métastatique ➜Réduction des TIL et des signatures d'expression des gènes activant l'immunité dans les TNBC métastatiques. La Lettre du Cancérologue SABCS 2018 - D’après Hutchinson KE, et al. , abstr. PD 5 -07, actualisé

Chapitre V Concept d’immunomodulation Céline Rouger (Villejuif) La Lettre du Cancérologue
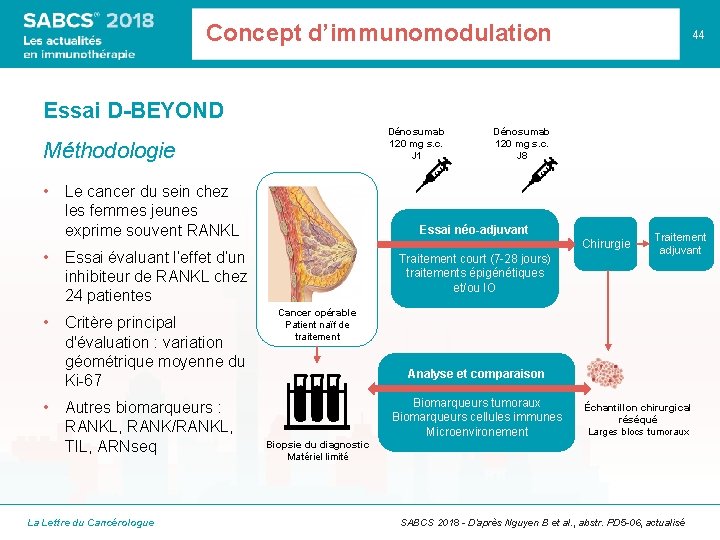
Concept d’immunomodulation 44 Essai D-BEYOND Dénosumab 120 mg s. c. J 1 Méthodologie • Le cancer du sein chez les femmes jeunes exprime souvent RANKL Essai néo-adjuvant Chirurgie • Essai évaluant l’effet d’un inhibiteur de RANKL chez 24 patientes • Critère principal d'évaluation : variation géométrique moyenne du Ki-67 • Autres biomarqueurs : RANKL, RANK/RANKL, TIL, ARNseq La Lettre du Cancérologue Dénosumab 120 mg s. c. J 8 Traitement court (7 -28 jours) traitements épigénétiques et/ou IO Traitement adjuvant Cancer opérable Patient naïf de traitement Analyse et comparaison Biomarqueurs tumoraux Biomarqueurs cellules immunes Microenvironement Échantillon chirurgical réséqué Larges blocs tumoraux Biopsie du diagnostic Matériel limité SABCS 2018 - D’après Nguyen B et al. , abstr. PD 5 -06, actualisé
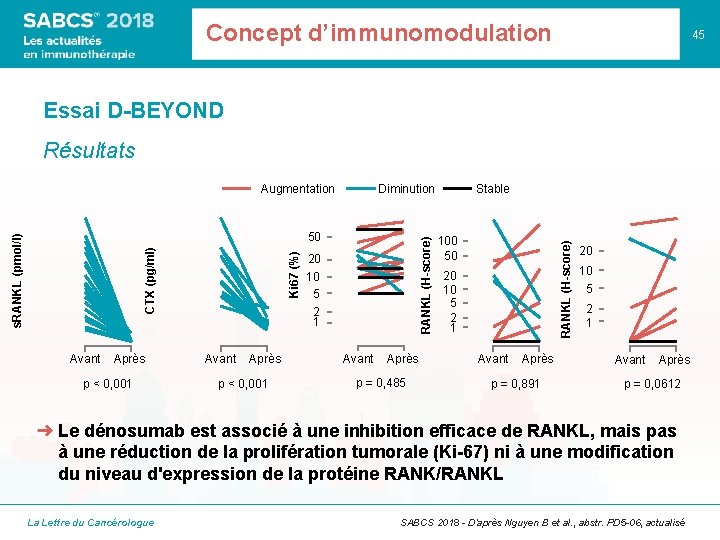
Concept d’immunomodulation 45 Essai D-BEYOND Résultats Diminution Avant Après p < 0, 001 RANKL (H-score) Ki 67 (%) CTX (pg/ml) s. RANKL (pmol/l) 50 20 10 5 2 1 Avant Après p < 0, 001 Avant Après p = 0, 485 Stable 100 50 RANKL (H-score) Augmentation 20 10 5 2 1 Avant Après p = 0, 891 20 10 5 2 1 Avant Après p = 0, 0612 ➜ Le dénosumab est associé à une inhibition efficace de RANKL, mais pas à une réduction de la prolifération tumorale (Ki-67) ni à une modification du niveau d'expression de la protéine RANK/RANKL La Lettre du Cancérologue SABCS 2018 - D’après Nguyen B et al. , abstr. PD 5 -06, actualisé

Concept d’immunomodulation Essai D-BEYOND Résultats s. TIL (1, 75, IC 95 : 1, 28 -2, 39) ; p = 0, 001 post-pre CD 8 (1, 59, IC 95 : 1, 14 -2, 21) ; p = 0, 008 CD 3 (1, 68, IC 95 : 1, 18 -2, 4) ; p = 0, 006 post-pre FOXP 3 (0, 63, IC 95 : 0, 49 -0, 83) ; p = 0, 002 Ki 67 + s. TILs (1, 33, IC 95 : 0, 92 -1, 92) ; p = 0, 125 post-pre CD 20 (1, 62, IC 95 : 1, 09 -2, 4) ; p = 0, 019 ➜ Le dénosumab induit une immunomodulation du microenvironnement tumoral avec une augmentation des TIL, lymphocytes T, B et T cytotoxiques et une réduction des Treg. La Lettre du Cancérologue SABCS 2018 - D’après Nguyen B et al. , abstr. PD 5 -06, actualisé 46

Concept d’immunomodulation Essai D-BEYOND Conclusions • Un traitement de courte durée par le dénosumab n'a pas réduit le taux de prolifération tumorale. • Cependant, le traitement par dénosumab montre une augmentation significative des TIL et des lymphocytes T cytotoxiques CD 8, tandis que l'infiltration de Treg a diminué. • Ces résultats suggèrent que le dénosumab joue un rôle immunomodulateur dans le traitement du cancer du sein chez les jeunes femmes et que son utilisation en association pourrait accroître l'efficacité de l'immunothérapie. La Lettre du Cancérologue SABCS 2018 - D’après Nguyen B et al. , abstr. PD 5 -06, actualisé 47
- Slides: 48